18. 草酸亚铁晶体(FeC
2O
4•2H
2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,某化学兴趣小组设计实验验证草酸亚铁晶体热分解的气体产物,并用热重法(TG)确定其分解后所得固体产物的组成,探究过程如下:
【查阅资料】
①硫酸铜晶体(CuSO
4•5H
2O)受热时会发生如下反应:CuSO
4•5H
2O
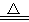
CuSO
4+5H
2O草酸亚铁晶体(FeC
2O
4•2H
2O)也能发生类似的反应;
②草酸亚铁晶体热分解的气体产物是H
2O,CO,CO
2;
③白色的无水CuSO
4遇水蒸气会变成蓝色;
④浓硫酸具有吸水性,是常用的气体干燥剂;
⑤浓的氢氧化钠溶液易吸收大量的二氧化碳气体,比石灰水吸收效果好。
【实验设计】
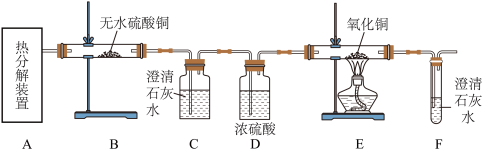
(1)从环保角度考虑,该套实验装置的明显缺陷是
___ 。
(2)可选择以下实验装置中的
__ (选填“甲”或“乙”)作为虚线中的“热分解装置”。

【问题讨论】
(3)实验过程中如果观察到以下现象:B中白色无水CuSO
4变成蓝色,
__ ,E中黑色粉末变成红色,则可证明草酸亚铁晶体热分解的气体产物是H
2O,CO,CO
2;写出F装置中所发生反应的化学方程式
___ 。
(4)该兴趣小组进行上述实验时,应先点燃
__ 处(填“A”或“E”)的酒精灯,原因是
__ 。
(5)若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产物中有CO,则需对实验设计方案进行改进,请说出你的改进措施
___ 。
【数据分析】
(6)称取3.60g草酸亚铁晶体(FeC
2O
4•2H
2O,相对分子质量是180)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示,请分析该图回答下列问题:
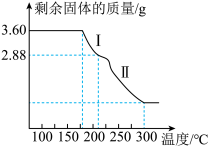
①过程Ⅰ发生反应的化学方程式为
____ 。
②已知:300℃时草酸亚铁晶体完全分解后剩余固体只有一种且是铁的氧化物。通过计算可确定该氧化物为
_____ (填名称)。(请写出计算过程)