江苏省射阳县第二中学2019届九年级下学期第一次阶段检测化学试题
江苏
九年级
阶段练习
2019-04-28
251次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、化学与社会发展、化学实验、物质构成的奥秘
一、选择题 添加题型下试题
| A.海水晒盐 | B.太阳能光解水制氢气 | C.光合作用 | D.生石灰吸水 |
【知识点】 化学变化与物理变化判断解读
| A.加过量膨大剂,使西瓜个大汁鲜 | B.用福尔马林(甲醛溶液)保鲜鱼虾 |
| C.用小苏打(碳酸氢钠)发酵面粉做面包 | D.牛奶中添加三聚氰胺,提高含氮量 |
【知识点】 碳酸氢钠、碳酸钠、碳酸钙解读 对人体健康危害的物质解读
| A.用明矾溶液可以区分硬水和软水 |
| B.用98%浓硫酸配制20%的稀硫酸的配制步骤是:计算—称量—溶解—保存 |
| C.浓硫酸不慎沾到皮肤上,立即用大量水冲洗,然后再涂上3%-5%的氢氧化钠溶液 |
| D.中和反应广泛应用于工农业生产中,如农业上用熟石灰改良酸性土壤 |
【知识点】 浓溶液稀释配制一定质量分数溶液解读 中和反应的实际应用解读
A.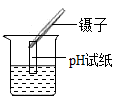 测量溶液的pH 测量溶液的pH | B.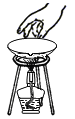 移走蒸发皿 移走蒸发皿 |
C.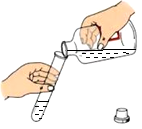 倾倒液体 倾倒液体 | D.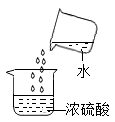 稀释浓硫酸 稀释浓硫酸 |
【知识点】 基本实验操作
| A.在汽油中加入少量高锰酸钾,高锰酸钾溶解呈紫红色 |
| B.硫在氧气中燃烧产生蓝紫色火焰 |
| C.加热饱和石灰水,出现白色浑浊 |
| D.把洁净的铜丝放入硝酸银溶液中,溶液由无色逐渐变蓝色 |
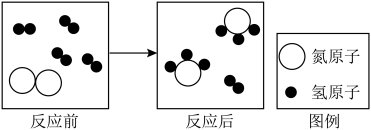
| A.两种反应物都是单质 |
| B.该反应为化合反应 |
| C.生成物中氮元素化合价为-3价 |
| D.该反应的化学方程式中A、B、C前的化学计量数之比为4∶1∶2 |
【知识点】 微粒图像的分析及应用解读 化学式图示的分析解读
| A.麻黄碱的相对分子质量为165 |
| B.麻黄碱中含有10个碳原子 |
C.麻黄碱中氢元素的质量分数最大 |
| D.麻黄碱中氮元素和氧元素的质量比为1:1 |
| A.滤渣中一定有Fe粉 | B.滤渣中一定有Ag粉 |
| C.滤液中一定有Fe2+ | D.滤液中一定有Ag+、Cu2+ |
| A.物质与氧气发生的反应都是氧化反应,则氧化反应一定要有氧气参加 |
| B.单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质 |
| C.中和反应生成盐和水,生成盐和水的反应一定是中和反应 |
| D.碱性溶液能使酚酞溶液变红,能使酚酞溶液变红的溶液一定呈碱性 |
| A.Zn粉(ZnO):加入足量稀硫酸充分反应后过滤 |
| B.CaCO3(Na2CO3):加足量水溶解,过滤,滤液蒸发结晶 |
| C.Na2SO4(H2SO4):加入适量的Ba(OH)2溶液充分反应后过滤 |
| D.Zn(NO3)2(AgNO3):加入过量Zn粉充分反应后过滤 |
| A.Na+、K+、Cl−、CO32− | B.H+、Na+、CO32−、SO42− |
| C.NH4+、K+、NO3−、Cl− | D.Cu2+、Ca2+、Cl−、NO3− |
【知识点】 复分解反应的实质与应用解读 溶液中物质是否共存相关判断解读

| A.在t2℃时,将65g溶液倒出去32.5g |
| B.将65g溶液蒸发掉32.5g的水,再冷却到t2℃ |
| C.在t2℃时,向65g溶液中加入15g KNO3固体并充分溶解 |
| D.将65g溶液的温度从t2℃降低到t1℃ |
【知识点】 固体溶解度曲线的应用解读 固体溶解度的影响因素解读
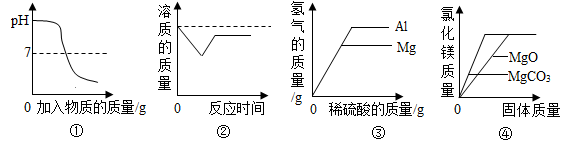
| A.图①是向久置空气中的NaOH溶液中加入盐酸,溶液的pH与加入盐酸质量的关系 |
| B.图②是向室温下的饱和石灰水中加入生石灰,溶液中的溶质质量与时间的关系(氢氧化钙溶解度随温度升高减小) |
| C.图③是向等质量的金属镁和铝中加入足量且质量分数相等的稀硫酸,生成氢气的质量与加入稀硫酸质量的关系 |
| D.图④是分别向同质量、同质量分数的稀盐酸中不断加入碳酸镁和氧化镁固体,加入固体质量与生成氯化镁的质量关系 |
【知识点】 强碱露置在空气中的变质解读 生石灰的性质及用途解读
二、多选题 添加题型下试题
| A.既无氯化铁,也无碳酸钠 | B.只有氯化镁,没有氯化钠 |
| C.肯定有氯化镁,可能有氯化钠 | D.肯定有氯化镁,也肯定有氯化钠 |
【知识点】 化学方程式有关计算 盐类参与的反应解读 几种常见阴、阳离子的鉴别解读
三、填空与简答 添加题型下试题
①葡萄糖的化学式为
②四个碳酸根离子
③标出氨气中氮元素的化合价
④碘酒中的溶剂
(2)用于制作航天飞船的合金材料中含有金属钼,如图是钼元素的部分信息,请回答下列问题:

①钼元素的相对原子质量为
②钼元素的原子易
四、实验题 添加题型下试题

(1)写出图中有标号的仪器的名称:①
(2)甲同学用一定质量的高锰酸钾制取氧气并测量生成气体的体积,反应的方程式为
(3)实验过程中,甲同学观察到E装置中的水变为紫红色,为了防止试验过程中出现上述现象,相应的改进措施是
(4)小明同学用G装置验证二氧化碳的性质。试管①用来检验二氧化碳是否与水反应,试管中应盛放的药品是
【知识点】 二氧化碳制取的综合考查解读 二氧化碳的检验、验满及净化解读
五、科学探究题 添加题型下试题
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是
(2)铁钉在初中化学实验中多次出现,下图展示了光亮铁钉的一系列变化。

(ⅰ)变化②中,铁钉主要与空气中的
(ⅱ)变化③中除去铁锈的化学方程式为
(ⅲ)如果用a、b分别代表光亮的铁钉和无锈铁钉,则它们的质量关系
A a<b B a>b C a=b D 无法比较
(3)为探究锌、铁、铜三种金属的活动性,以及他们和氢元素的位置关系,小明设计了如下实验,你认为不需要进行的实验是
A 将铁粉放入硫酸锌溶液中 B 将铁粉放入稀硫酸中
C 将铁粉放入硫酸铜溶液中 D 将铜片放入稀硫酸中
(4)该同学查阅资料得知,铜锈的主要成分是碱式碳酸铜【Cu2(OH)2CO3】,他以铜锈为原料设计并完成如下实验(杂质不与稀硫酸反应,且不含铜元素。图中部分物质略去)。Mr(碱式碳酸铜)=222

①无色气体A是
②在蓝色溶液B中加入铁粉时,发生反应的化学方程式为
③已知铜锈样品的质量是10g,固体F的质量是3.2g,则铜锈中含Cu2(OH)2CO3的质量分数是
【知识点】 金属与盐溶液反应 金属与酸反应原理解读 金属活动性强弱的探究解读
六、综合应用题 添加题型下试题
【提出猜想】猜想一:只有CaCl2; 猜想二:
【实验探究】为了验证猜想,该兴趣小组的同学设计了如下实验方案。
| 方案编号 | 方案1 | 方案2 |
| 实验操作 (分别取少量实验后的溶液于试管中) | 加入几滴紫色的石蕊试液 | 滴加硝酸银溶液 |
| 实验现象 | —— | 产生白色沉淀。 |
| 实验结论 | 猜想二成立。 | |
【评价反思】(1)方案1观察到的实验现象
(2)有同学提出方案2是错误的,原因是
(3)该兴趣小组的小华同学观察到石灰石和稀盐酸反应后容器内有少量固体剩余,得出溶液中肯定没有盐酸的结论,其他同学认为小华的说法不合理,其理由是
(4)请你设计一个与上述不同的实验方案(说出实验步骤和现象)
【拓展延伸】石灰石的主要成分碳酸钙可用作补钙剂。某补钙药剂说明书的部分信息如图所示。现将100g盐酸分成5等份,逐次加到用25片该药剂制成的粉末中(其他成分不与盐酸反应,也不溶于水),得到图像如下。请根据有关信息回答问题。

①该品牌补钙药剂中CaCO3的质量分数是

②当加入盐酸和25片该药剂完全反应时,求所得溶液中溶质的质量分数
试卷分析
试卷题型(共 19题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.94 | 碳酸氢钠、碳酸钠、碳酸钙 对人体健康危害的物质 | 单选题 |
| 3 | 0.65 | 浓溶液稀释配制一定质量分数溶液 中和反应的实际应用 | 单选题 |
| 4 | 0.65 | 基本实验操作 | 单选题 |
| 5 | 0.85 | 硫在氧气中燃烧及其实验 溶解性相关的实验探究 固体溶解度的影响因素 盐类参与的反应 | 单选题 |
| 6 | 0.65 | 微粒图像的分析及应用 化学式图示的分析 | 单选题 |
| 7 | 0.65 | 化学式、分子式及涵义 根据化学式计算相对分子质量 根据化学式计算元素质量比 根据化学式计算元素质量分数 | 单选题 |
| 8 | 0.4 | 金属与盐溶液反应 金属与酸反应原理 应用金属活动性解释相关现象 | 单选题 |
| 9 | 0.65 | 氧化反应 单质和化合物的判断 酸碱指示剂的应用 中和反应的概念及微观本质 | 单选题 |
| 10 | 0.4 | 盐类参与的反应 常见酸碱盐的溶解性 | 单选题 |
| 11 | 0.65 | 复分解反应的实质与应用 溶液中物质是否共存相关判断 | 单选题 |
| 12 | 0.65 | 固体溶解度曲线的应用 固体溶解度的影响因素 | 单选题 |
| 13 | 0.4 | 强碱露置在空气中的变质 生石灰的性质及用途 | 单选题 |
| 二、多选题 | |||
| 14 | 0.15 | 化学方程式有关计算 盐类参与的反应 几种常见阴、阳离子的鉴别 | |
| 三、填空与简答 | |||
| 15 | 0.65 | 元素周期表信息示意图 化学式书写及读法 常用化合价规律 | 填空题 |
| 四、实验题 | |||
| 16 | 0.65 | 二氧化碳制取的综合考查 二氧化碳的检验、验满及净化 | |
| 五、科学探究题 | |||
| 17 | 0.4 | 金属与盐溶液反应 金属与酸反应原理 金属活动性强弱的探究 | |
| 六、综合应用题 | |||
| 18 | 0.4 | 溶质质量分数结合化学方程式的计算 盐类参与的反应 设计实验探究物质的成分 | |



