山东省泰安市新泰市石莱学校2019-2020学年九年级上学期9月月考化学试题
山东
九年级
阶段练习
2019-10-16
166次
整体难度:
适中
考查范围:
身边的化学物质、化学实验、物质构成的奥秘、物质的化学变化
一、选择题 添加题型下试题
| A.豆浆 | B.牛奶 | C.矿泉水 | D.果酱 |
【知识点】 溶液、溶质和溶剂概念解读 溶液的基本特征解读
| A.升高温度到30℃ | B.温度不变,蒸发掉少量溶剂 |
| C.降低温度到10℃ | D.温度不变,加入少量氧化钙固体 |
【知识点】 饱和溶液和不饱和溶液判断解读 固体溶解度的影响因素解读


| A.所得溶液是20℃时乙的饱和溶液 |
B.从20℃降温到 ,甲、乙两物质的溶解度相等,溶质的质量分数甲比乙小 ,甲、乙两物质的溶解度相等,溶质的质量分数甲比乙小 |
| C.升高温度可使试管中甲、乙溶液的溶质质量分数均增大 |
| D.乙中混有少量甲,可用降温结晶法提纯乙 |
【知识点】 饱和溶液和不饱和溶液的转换解读 固体溶解度曲线的应用解读
| A.量筒 | B.玻璃棒 | C.酒精灯 | D.烧杯 |
【知识点】 配制一定质量分数溶液的仪器解读
| A.溶液是由溶质和溶剂组成的混合物 |
| B.向100g溶质质量分数为30%的硝酸钾溶液中加入20mL水,溶液的溶质质量分数变为25% |
| C.试剂瓶中的溶液在使用时不慎洒出一部分,剩余溶液的溶质质量分数减小 |
| D.溶液加水稀释前后,溶质的质量不变 |
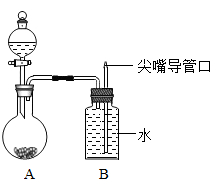
| A.硝酸铵和水 | B.二氧化锰和过氧化氢溶液 |
| C.氯化钠和水 | D.铜和稀盐酸 |
| A.某物质的饱和溶液变为不饱和溶液,溶质的质量分数一定变小 |
| B.在一定温度下,同一物质的饱和溶液一定比不饱和溶液溶质的质量分数大 |
| C.任何物质的饱和溶液,当温度降低时一定会析出溶质 |
| D.饱和溶液析出晶体后,剩余溶液中溶质的质量分数一定变小 |
| A.9.1% | B.11.8% | C.13.3% | D.15.3% |
| A.一定是浓溶液 | B.一定是稀溶液 |
| C.一定是饱和溶液 | D.无法确定 |
| A.升高温度 | B.降低温度 | C.加入溶质 | D.倒出溶剂 |
【知识点】 饱和溶液和不饱和溶液的转换解读
| A.汽水 | B.盐酸 | C.碘酒 | D.生理盐水 |
【知识点】 溶液、溶质和溶剂概念解读
| A.碘溶于水得到碘酒 |
| B.溶液是均一的、稳定的混合物 |
| C.洗涤剂去油污的原理是溶解 |
| D.植物油加入水中可得溶液 |
【知识点】 溶液、溶质和溶剂概念解读 悬浊液、乳浊液解读
| A.实验步骤:计算、量取、溶解、装瓶、贴签 |
| B.量取水时,用规格为50mL的量筒 |
| C.实验过程中玻璃棒搅拌的作用是散热 |
| D.若在量取水时俯视读数量取,则配制溶液的溶质质量分数小于6% |
【知识点】 固体配制一定质量分数溶液解读

| A.t2℃时,溶溶解度:a=b>c |
| B.随温度的升高,c物质的溶解度减小 |
| C.t3℃℃时,将30克a加入50克水中可以得到80克溶液 |
| D.t1℃时,a的饱和溶液和c的饱和溶液的溶质质量分数相等 |
A. 测定溶液pH 测定溶液pH | B. 配制溶液 配制溶液 |
C. 称量固体 称量固体 | D. 稀释浓硫酸 稀释浓硫酸 |
| A.打开盛放浓盐酸的试剂瓶盖,瓶口出现白雾 |
| B.用洗洁精洗去餐具上的油污属于乳化 |
C.可以用水来区别 固体和 固体和 固体 固体 |
| D.饱和的氯化钠溶液一定比不饱和氯化钠溶液浓 |
| A橱 | B橱 | C橱 | D橱 |
| 盐酸 硫酸 | 食盐 硫酸铜 | 氢氧化钠 氢氧化钙 | 氧化铁 氧化钙 |
| A.A | B.B | C.C | D.D |
| 混合物 | 酸 | 碱 | 盐 | 氧化物 | 单质 | |
| A | 冰水混合物 | 硫酸 | 氢氧化钠 | 硫酸钡 | 干冰 | 氦气 |
| B | 天然气 | 硝酸 | 氢氧化钙 | 碳酸氢钙 | 四氧化三铁 | 24k金 |
| C | 生铁 | 盐酸 | 碱式碳酸铜 | 氯化银 | 一氧化碳 | 液氧 |
| D | 石灰石 | 醋酸 | 氢氧化钡 | 碳酸钙 | 氯化钾 | 富勒烯 |
| A.A | B.B | C.C | D.D |
| A.变大 | B.变小 | C.不变 | D.无法确定 |

| A.蒸发40g水,改变温度至t1℃ |
| B.蒸发50g水,改变温度至t2℃ |
| C.加入20g溶质,改变温度至t2℃ |
| D.加入65g溶质,改变温度至t3℃ |
二、填空与简答 添加题型下试题
(1)实验室配制50g溶质质量分数为6%的氯化钠溶液,需要氯化钠的质量为
(2)实验室用浓硫酸(溶质质量分数为98%、密度是1.84g•mL﹣1)配制稀硫酸时,需要用到水。其主要步骤有:计算、混匀、冷却至室温、装入试剂瓶并贴好标签。若要配制10%的稀硫酸200g,还需加水的体积是
(1)氯化钠晶体是由
(2)四个硫酸根离子
(3)在氧化铁中铁元素显+3价
(4)溶于水使溶液温度显著降低的是

(1)20℃时,欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是A
(2)要在不改变溶质的质量分数的前提下使50℃时C的饱和溶液成为不饱和溶液,可采用的方法是
(3)将50℃时三种物质的饱和溶液分别都降温到20℃,此时溶液中溶质的质量分数从大到小是
(4)甲、乙两烧杯中分别装有50℃的100克和200克A的饱和溶液,若将两份溶液都降低到20℃,析出晶体质量的关系是甲
(5)欲从混有少量A的B物质的饱和溶液中得到纯净的B晶体,应该采用的方法是
【知识点】 固体溶解度曲线的应用解读 固体溶解度的影响因素解读
三、实验题 添加题型下试题

(1)上图中多处操作用到玻璃棒,其中操作③玻璃棒的作用是
(2)要完成“配制100 g 5%的氯化钠溶液”的实验:
①主要进行的实验步骤依次是计算、称量、量取、
②溶解过程中用到的仪器有
③实际配制的溶液中溶质的质量分数小于5%,其原因可能有
A 氯化钠固体不纯 B 固体倒入烧杯时洒落
C 配制时烧杯不干燥 D 装瓶时有液体溅出
(3)若要完成“粗盐中的难溶性杂质的去除”的实验,需要进行的操作步骤依次是
①蒸发结晶 ②过滤 ③溶解
四、科学探究题 添加题型下试题
提出问题:酸中的什么粒子使石蕊溶液变红色?
查阅资料:酸在溶液中以离子形式存在。如:稀盐酸中含H+、Cl-、H2O三种粒子。
猜想假设:H+使石蕊溶液变红色;
设计实验方案并进行实验:
| 实验步骤 | 现象 | 结论 |
| 往试管中加入2mL蒸馏水,再滴入几滴石蕊溶液 | 紫色石蕊试剂不变色 | 水分子不能使石蕊变红色 |
| 往试管中加入2mL NaCl溶液,再滴入几滴石蕊溶液 | Cl- | |
| 往试管中加入2mL稀HCl, 再 | H+ |
【知识点】 酸碱指示剂的应用解读 常见的酸碱指示剂及其变色情况解读
五、计算题 添加题型下试题

请计算:
(1)该大理石样品中碳酸钙的质量分数是_____;
(2)计算所用稀盐酸的溶质质量分数;_____
试卷分析
试卷题型(共 26题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 溶液、溶质和溶剂概念 溶液的基本特征 | 单选题 |
| 2 | 0.85 | 饱和溶液和不饱和溶液判断 固体溶解度的影响因素 | 单选题 |
| 3 | 0.65 | 饱和溶液和不饱和溶液的转换 固体溶解度曲线的应用 | 单选题 |
| 4 | 0.94 | 配制一定质量分数溶液的仪器 | 单选题 |
| 5 | 0.85 | 溶液、溶质和溶剂概念 溶液的基本特征 有关溶液浓缩、稀释的计算 | 单选题 |
| 6 | 0.65 | 过氧化氢制取氧气实验 金属与酸反应原理 溶解时能量的变化 | 单选题 |
| 7 | 0.65 | 饱和溶液和不饱和溶液判断 饱和溶液和不饱和溶液的转换 | 单选题 |
| 8 | 0.4 | 饱和溶液和不饱和溶液的转换 固体溶解度概念 溶解度的相关计算 溶质质量分数概念 | 单选题 |
| 9 | 0.85 | 溶液浓稀与溶液饱和的关系 饱和溶液和不饱和溶液的转换 | 单选题 |
| 10 | 0.85 | 饱和溶液和不饱和溶液的转换 | 单选题 |
| 11 | 0.85 | 溶液、溶质和溶剂概念 | 单选题 |
| 12 | 0.94 | 溶液、溶质和溶剂概念 悬浊液、乳浊液 | 单选题 |
| 13 | 0.85 | 固体配制一定质量分数溶液 | 单选题 |
| 14 | 0.4 | 固体溶解度概念 固体溶解度曲线的应用 固体溶解度的影响因素 溶解度的相关计算 | 单选题 |
| 15 | 0.4 | 固体配制一定质量分数溶液 浓硫酸的稀释 溶液的酸碱性的判断与pH的测定 托盘天平的正确使用方法和注意事项 | 单选题 |
| 16 | 0.65 | 溶解时能量的变化 乳化现象及应用 盐酸的物理性质 | 单选题 |
| 17 | 0.85 | 酸的定义 碱的定义 盐的定义 氧化物的定义 | 单选题 |
| 18 | 0.65 | 纯净物和混合物的判断 单质和化合物的判断 碱的定义 盐的定义 | 单选题 |
| 19 | 0.85 | 溶液的酸碱性的判断与pH的测定 溶液酸碱性及pH相关关系 | 单选题 |
| 20 | 0.15 | 固体溶解度曲线的应用 溶解度的相关计算 有关溶液浓缩、稀释的计算 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.85 | 浓溶液稀释配制一定质量分数溶液 配制一定溶质质量分数的计算 | 填空题 |
| 22 | 0.94 | 物质化学性质的决定因素 离子符号的含义及书写 常见元素、原子团的化合价 溶解时能量的变化 | 填空题 |
| 23 | 0.4 | 固体溶解度曲线的应用 固体溶解度的影响因素 | 填空题 |
| 三、实验题 | |||
| 24 | 0.85 | 配制一定质量分数溶液的仪器 固体配制一定质量分数溶液 | |
| 四、科学探究题 | |||
| 25 | 0.65 | 酸碱指示剂的应用 常见的酸碱指示剂及其变色情况 | |
| 五、计算题 | |||
| 26 | 0.4 | 不含杂质的化学方程式计算 含杂质的化学方程式计算 化学方程式与实验的计算 | |



