黑龙江省哈尔滨市平房区2019-2020学年九年级上学期期末化学试题
黑龙江
九年级
期末
2020-01-23
304次
整体难度:
适中
考查范围:
化学与社会发展、物质的化学变化、化学实验、身边的化学物质、物质构成的奥秘
一、选择题 添加题型下试题
A. 乘坐地铁出行,减缓温室效应增强 乘坐地铁出行,减缓温室效应增强 |
B. 秸秆全面禁烧,减少空气污染 秸秆全面禁烧,减少空气污染 |
C. 使用生物可降解塑料,减少白色污染 使用生物可降解塑料,减少白色污染 |
D. 用水雾喷洒室内种植 的蔬菜,防治水体污染 用水雾喷洒室内种植 的蔬菜,防治水体污染 |
A.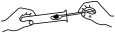 用药匙将粉末送至试管口,然后直立试管 用药匙将粉末送至试管口,然后直立试管 | B.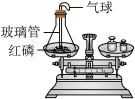 化学变化前质量的测定 化学变化前质量的测定 |
C.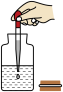 用滴管取液体 用滴管取液体 | D.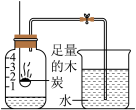 测定空气中氧气的含量 测定空气中氧气的含量 |
| A.用聚乙烯保鲜膜包装生鲜食品 |
| B.利用活性炭的过滤和吸附作用将硬水软化 |
| C.电线短路引起的火灾用水扑灭 |
| D.用食盐水长时间浸泡铁锅以防止其生锈 |
【知识点】 硬水的危害及软化方法解读
| A.红磷燃烧:红色固体燃烧,发出耀眼白光,产生白雾 |
| B.水通直流电:两个电极附近产生气泡,最终正负两极所得氧气和氢气的体积比约为1:2 |
| C.一氧化碳还原氧化铁:(玻璃管里的)粉末由红棕色逐渐变为银白色 |
| D.向硫酸铜溶液中加入过量氯化钡溶液:产生白色沉淀,溶液仍为蓝色 |
| A.农药有毒,使用不当会带来对人体健康的危害 |
| B.不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,再涂上碳酸钠溶液中和 |
| C.青少年缺少常量元素钙会发育不良 |
| D.食用滋生黄曲霉菌的大米和花生会损害肝脏 |
【知识点】 酸碱的腐蚀性及安全使用解读 某些元素的缺乏症解读
| A.除去银屑中的镁 Mg + H2SO4 =H2↑+ MgSO4 置换反应 |
B.工业上用高锰酸钾制取氧气 2KMnO2 K2MnO4+ MnO2+O2↑ 分解反应 K2MnO4+ MnO2+O2↑ 分解反应 |
| C.小苏打治疗胃酸过多 2NaHCO3+2HCl=2NaCl+H2O + CO2 ↑ 复分解反应 |
D.碳与二氧化碳反应 C + CO2 2CO 还原反应 2CO 还原反应 |

| A.麻黄碱由碳、氢、氧、氮四种元素构成 |
| B.麻黄碱是有机高分子化合物,其水溶液能使紫色石蕊溶液变蓝 |
| C.麻黄碱分子中的质子与电子的数目相等 |
| D.麻黄碱分子中氮、氧元素原子的质量比为1:1 |
【知识点】 化学式、分子式及涵义解读 根据化学式计算元素质量比解读
| A.空气是一种宝贵的资源,其中氮气的体积分数约占21% |
| B.陆地淡水约占全球水储量的2.53%,海水淡化目前可以作为应对淡水短缺的重要途径 |
| C.人们正在利用和开发的其他能源有乙醇、可燃冰和太阳能等 |
| D.人类每年从自然界提取量最大的金属是铁,防止铁腐蚀是保护它的有效途径之一 |
【知识点】 绿色能源的开发及利用解读 水资源的现状解读
| 选项 | 事 实 | 解 释 |
| A | 液化石油气压缩到钢瓶中 | 液化石油气分子间间隔随压强的增大而减小 |
| B | 硫酸和氢氧化钾溶液都能导电 | 溶液中存在自由移动的阴、阳离子 |
| C | 金刚石和石墨的硬度不同 | 碳原子的排列方式不同 |
| D | 冰水混合物是纯净物 | 由同种分子构成 |
| A.A | B.B | C.C | D.D |
| 选项 | A | B | C | D |
| 需区分的物质 | 一氧化碳和氧气 | 二氧化锰和铁粉 | 硫酸钾和氯化铵 | 羊毛制品和腈纶制品 |
| 方案一 | 燃着的木条 | 过氧化氢溶液 | 加入硝酸银溶液 | 用手触摸 |
| 方案二 | 闻气味 | 用磁铁吸引 | 加熟石灰,研磨 | 观察颜色 |
| A.A | B.B | C.C | D.D |
【知识点】 羊毛、合成纤维、棉的鉴别解读

| A.t1℃时,甲、乙两物质的饱和溶液中溶质的质量相等 |
| B.甲中含有少量乙可采用蒸发溶剂的方法提纯甲 |
| C.t2℃时,c点甲溶液加入10g甲,一定能变成a点甲溶液 |
| D.t1℃时,20g乙加入50 g水中,升温至t2℃恰好得到70g乙的饱和溶液 |
| 选项 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | 氢氧化钠 | 纯碱 | 适量盐酸 | 溶解、蒸发、结晶 |
| B | 水 | 悬浮物 | 明矾 | 吸附 |
| C | 碘 | 高锰酸钾 | 足量水 | 溶解、过滤、洗涤、干燥 |
| D | 氯化钙溶液 | 氢氧化钙 | 通入过量的二氧化碳 | 过滤 |
| A.A | B.B | C.C | D.D |
[提示: Cu2(OH)2CO3
 2CuO +CO2↑+H2O]
2CuO +CO2↑+H2O]| A.4.8% | B.9.6% | C.50% | D.51.2% |
二、填空与简答 添加题型下试题

(1)配料表中的“肉”富含的营养素主要是
(2)使用的淀粉
(3)用于红肠调味的食盐的主要成分还是一种重要的化工原料,其水溶液在通电条件下生成火碱、氯气和氢气,该反应的化学方程式为
(1)2019年度100大最佳发明之一的折叠屏笔记本,可在平板电脑和笔记本间自由转换。制造笔记本外壳使用的(工程)塑料属于

A 合成有机高分子材料 B 复合材料 C 金属材料
(2)制造折叠屏的技术核心“铰链”使用的不锈钢的主要成分是
(3)使用石墨烯制造有机发光二极管显示屏,主要是因为其具有优异的透光性和
(4)锂离子电池体积小、容量大和无记忆效应等性能,使电子产品的轻薄、便携与持久续航成为可能。因此成就,2019年诺贝尔化学奖授予了对锂离子电池的研究有突出贡献的三位科学家。笔记本电脑利用锂电池供电使用过程中想要实现的能量转化是
【知识点】 金属材料和非金属材料解读

(1)在C图中将相关粒子图形补充完整,使之正确
(2)由A→B变化的微观实质是:在点燃的条件下,
(3)生成物均是化合物中的
(4)此变化过程中不变的三种元素位于周期表同一周期的是
【知识点】 质量守恒定律的微观解释解读 微粒图像的分析及应用解读
三、实验题 添加题型下试题
(1)化学实验改进或创新的目的主要是使实验变得更加“简化”(减少实验步骤)、“节约药品”或“环保”等。据此可将下列实验中的
| 硫在氧气中燃烧 | 铁锈蚀条件的探究 | 燃烧条件的探究 | 二氧化碳的性质 |
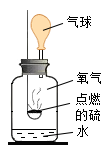 |  |  |  |
| A | B | C | D |
(2)下图是氮元素的价态图。氮元素显示F、G点的+5价与氮原子的

【知识点】 测定空气中氧气含量实验的改进解读
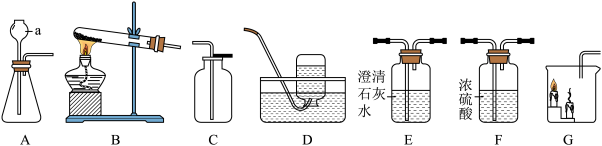
(1)不增加其他用品,用上述药品及装置在实验室制取氧气的化学方程式为
(2)实验室制取二氧化碳需补充的药品是
四、填空与简答 添加题型下试题
 ”“
”“ ”或“
”或“ ”表示两种物质能单向或双向转化,用“
”表示两种物质能单向或双向转化,用“ ”表示两种物质既能单向转化又能反应。部分反应物、生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质。)
”表示两种物质既能单向转化又能反应。部分反应物、生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质。)
(1)写出D、F(或主要成分)的化学式: D
(2)C
 A的实验现象是
A的实验现象是(3)A
 B的化学方程式是
B的化学方程式是【知识点】 根据酸的通性推断物质的性质解读 各类物质间反应的总结解读
五、综合应用题 添加题型下试题

(1)上述实验过程中发生反应的化学方程式为
(2)根据已知条件列出求解A烧杯中参加反应的金属质量 (X)的比例式为
(3)所得固体混合物中铜、铁元素质量的最简比为
(4)用16%的硫酸铜溶液配制上述实验中所用的硫酸铜溶液,需加水的体积为
(5)将D中滤液蒸发7.2g水,最终所得不饱和溶液中溶质的质量分数为
(6)冶炼60t上述所得固体混合物中的铁,需要含杂质20%的赤铁矿的质量为
【知识点】 不含杂质的化学方程式计算解读 化学方程式与实验的计算解读
六、科学探究题 添加题型下试题
【提出问题】酸与碱能否发生反应?

【实验与结论】秦思和石建分别选了不同的酸碱进行实验A、B。A中产生现象的原因是
【证据与解释】裘臻进行实验D,向氢氧化钠溶液中多次滴加稀盐酸,测定溶液pH,绘制溶液pH随加入的稀盐酸变化的曲线图E。得出与C相同的实验结论的依据是

【反思与分析】实验A、C与D,通过不同的证据,都能证明酸与碱能发生反应。通过比较,崇湜发现从
【归纳提炼】通过上述实验可知,探究酸碱之间能否发生反应的实验设计思路是:通过明显现象,证明
【知识点】 无明显现象的中和反应的判断解读
试卷分析
试卷题型(共 23题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 空气污染及其保护 水体的污染及保护 | 单选题 |
| 2 | 0.85 | 实验探究质量守恒定律 胶头滴管的正确使用方法和注意事项 固体药品的取用 | 单选题 |
| 3 | 0.85 | 乳化现象及应用 | 单选题 |
| 4 | 0.65 | 空气中各成分的用途 | 单选题 |
| 5 | 0.65 | 硬水的危害及软化方法 | 单选题 |
| 6 | 0.65 | 盐类参与的反应 | 单选题 |
| 7 | 0.65 | 酸碱的腐蚀性及安全使用 某些元素的缺乏症 | 单选题 |
| 8 | 0.65 | 化学方程式的书写 | 单选题 |
| 9 | 0.65 | 化学式、分子式及涵义 根据化学式计算元素质量比 | 单选题 |
| 10 | 0.65 | 绿色能源的开发及利用 水资源的现状 | 单选题 |
| 11 | 0.65 | 微粒的观点解释现象 | 单选题 |
| 12 | 0.65 | 羊毛、合成纤维、棉的鉴别 | 单选题 |
| 13 | 0.65 | 固体溶解度概念 固体溶解度曲线的应用 溶解度的相关计算 | 单选题 |
| 14 | 0.65 | 盐类参与的反应 | 单选题 |
| 15 | 0.15 | 用质量守恒定律确定物质组成 不含杂质的化学方程式计算 | 单选题 |
| 二、填空与简答 | |||
| 16 | 0.65 | 蛋白质 维生素的组成与作用 | 填空题 |
| 17 | 0.65 | 金属材料和非金属材料 | 填空题 |
| 18 | 0.65 | 质量守恒定律的微观解释 微粒图像的分析及应用 | 填空题 |
| 21 | 0.15 | 根据酸的通性推断物质的性质 各类物质间反应的总结 | 推断题 |
| 三、实验题 | |||
| 19 | 0.65 | 测定空气中氧气含量实验的改进 | |
| 20 | 0.65 | 氯酸钾制取氧气 制取二氧化碳的原理 二氧化碳制取的综合考查 | |
| 四、综合应用题 | |||
| 22 | 0.4 | 不含杂质的化学方程式计算 化学方程式与实验的计算 | |
| 五、科学探究题 | |||
| 23 | 0.4 | 无明显现象的中和反应的判断 | |

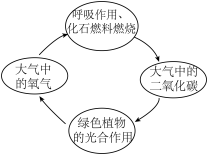 自然界的碳、氧循环
自然界的碳、氧循环 分子运动现象
分子运动现象 洗涤剂除油污
洗涤剂除油污 煤制成煤气
煤制成煤气 氮气用于磁悬浮列车
氮气用于磁悬浮列车 锰钢主要用于制造飞机
锰钢主要用于制造飞机 液氦冷冻机
液氦冷冻机 碳酸钙做补钙剂
碳酸钙做补钙剂

