2019年山东省济南市市中区中考一模化学试题
山东
九年级
一模
2020-01-23
244次
整体难度:
适中
考查范围:
物质的化学变化、化学与社会发展、身边的化学物质、化学实验、物质构成的奥秘
一、选择题 添加题型下试题
A. 高温炼铁 高温炼铁 | B. 海水晒盐 海水晒盐 |
C. 煤气中毒 煤气中毒 | D. 火箭发射 火箭发射 |
【知识点】 化学变化与物理变化判断解读
| A.我市全面禁止燃放烟花爆竹 |
| B.生活中提倡垃圾分类回收 |
| C.家离学校较近的同学徒步上学 |
| D.购物多用塑料袋盛放物品 |
【知识点】 有机材料对环境的影响及应对措施解读 空气污染及其保护解读
| A.干冰用作环保型制冷剂 |
| B.青少年应大量服用保健品 |
| C.学生适量吸烟有利于身体健康 |
| D.变质的食物加工后可以放心食用 |
【知识点】 二氧化碳的用途解读 对人体健康危害的物质解读
A.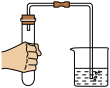 气密性的检查 气密性的检查 | B.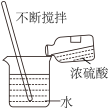 浓硫酸的稀释 浓硫酸的稀释 |
C.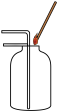 二氧化碳的验满 二氧化碳的验满 | D.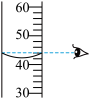 液体的量取 液体的量取 |
| A.久未开启的地窖CO2含量高,若冒然进入,易发生窒息 |
| B.在化粪池等有沼气的井盖口燃放鞭炮,易引起爆炸 |
| C.用煤炉取暖时,可在屋里洒些石灰水,以防煤气中毒 |
| D.室内煤气泄露时,若立即打开排气扇通风,易引起爆炸 |

| A.原子核内有17个质子 |
| B.该粒子属于非金属元素 |
| C.该粒子是阴离子 |
| D.在发生化学反应时易得到电子 |
| 食物 | 葡萄汁 | 苹果汁 | 牛奶 | 鸡蛋清 |
| pH | 3.5~4.5 | 2.9~3.3 | 6.3~6.6 | 7.6~8.0 |
其中酸性最强的是
| A.葡萄汁 | B.苹果汁 | C.牛奶 | D.鸡蛋清 |
【知识点】 溶液酸碱性及pH相关关系解读
| A.H3SbO4 | B.SbO3 | C.SBO2 | D.Sb2O3 |
【知识点】 用质量守恒定律确定物质组成解读 根据方程式推测化学式解读
| A.品红分子在热水中的运动速率比在冷水中快 |
| B.品红分子在热水中比在冷水中容易分解 |
| C.热水中水分子间有间隔,冷水中水分子间无间隔 |
| D.热水中品红分子变大了,冷水中品红分子变小了 |
| A.水的天然循环是通过其三态变化实现的 |
| B.物质的酸碱性对生命活动具有重要意义 |
| C.凡是生成盐和水的反应一定是中和反应 |
| D.在化学变化中,原子核是不变的,发生改变的只是原子核外的电子 |
【知识点】 中和反应与复分解反应的关系解读 水资源的现状解读

| A.参加反应的物质甲、乙的分子个数比为1:1 |
| B.该反应既属于化合反应,也属于氧化反应 |
| C.该反应前后各原子的数目发生了改变 |
| D.该化学反应不遵守质量守恒定律 |
【知识点】 质量守恒定律的微观解释解读 化学式图示的分析解读
| 试管中盛放物质 | 碳酸钠溶液 | 硝酸钡溶液 | 氯化钠溶液 |
| 现象 | 有气泡冒出 | 有白色沉淀 | 无明显现象 |
| A.稀硫酸 | B.MgSO4溶液 | C.KOH溶液 | D.稀盐酸 |
| A.滤液一定是无色溶液 |
| B.滤液中一定含有MgCl2、FeCl2、CuCl2 |
| C.加入镁粉的质量一定小于a克 |
| D.滤渣一定是Mg、Fe、Cu三种单质的混合物 |
【知识点】 金属与盐溶液反应 金属与酸反应原理解读 物质鉴别——选用试剂鉴别解读
| 选项 | 物质 | 杂质 | 除杂质所用试剂和方法 |
| A | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| B | CaO固体 | CaCO3 | 加水,溶解,过滤 |
| C | Na2SO4溶液 | Na2CO3溶液 | 加入过量稀硫酸 |
| D | CO2 | HCl | 将混合气体通入足量NaOH溶液,干燥 |
| A.A | B.B | C.C | D.D |
| A.生成CO2为4.4g |
| B.原固体混合物中钠元素为9.2g |
| C.所得溶液中溶质的质量为23.4g |
| D.所加稀盐酸的溶质质量分数为7.3% |
【知识点】 含杂质的化学方程式计算解读 溶液和化学方程式的综合计算解读
二、填空与简答 添加题型下试题
①一种金属单质
②一种氧化物
③一种可作干燥剂的酸
④一种难溶性的碱
⑤一种可溶性的盐
三、计算题 添加题型下试题
①三聚氰胺属于_____(填“有机物”“无机物”“氧化物”之一)。
②三聚氰胺由_____种元素组成。
③一个三聚氰胺分子中含有_____个原子。
④甲醛中所含碳元素的质量分数为_____。
⑤在三聚氰胺和甲醛中,所含碳元素的质量分数前者_____后者(填“大于”、“等于”、“小于”之一)。
四、填空与简答 添加题型下试题
①碳酸氢钠受热分解生成碳酸钠、水和二氧化碳。请写出此反应的化学方程式
②下列有关碳酸氢钠和碳酸钠的叙述中,不正确的是
A 碳酸氢钠是医疗上治疗胃酸过多的药剂之一
B 碳酸氢钠在食品工业上是发酵粉的主要成分
C 碳酸钠是小苏打和纯碱的主要成分
D 碳酸氢钠是制造饮料时的一种常用原料
【知识点】 常见盐的俗名、用途解读 碳酸氢钠、碳酸钠、碳酸钙解读

①t1℃时,Na2CO3的溶解度为
②t1℃时,将Na2CO3的饱和溶液升温到t2℃,Na2CO3溶液的溶质质量分数将
③t2℃时,Na2CO3溶液中溶质质量分数
【知识点】 固体溶解度曲线的应用解读
五、实验题 添加题型下试题

(1)若以石灰石和稀盐酸为原料在实验室中制备并收集干燥的二氧化碳。
①所选仪器的连接顺序为
②生成二氧化碳时,所发生反应的化学方程式为
③若将二氧化碳通入澄清石灰水中,石灰水的pH将
(2)欲用纯净的一氧化碳气体,测定某不纯氧化铜样品的纯度(CuO+CO
 Cu+CO2,杂质不反应),并验证气体生成物的性质。某同学所选仪器装置的连接顺序为:纯净的一氧化碳→B→F→C。
Cu+CO2,杂质不反应),并验证气体生成物的性质。某同学所选仪器装置的连接顺序为:纯净的一氧化碳→B→F→C。①连接仪器装置C的目的是
②若氧化铜样品质量为30g,反应后B装置的质量减少5g,则该氧化铜样品中氧化铜的质量为
【知识点】 制取二氧化碳的原理解读 一氧化碳还原氧化铜实验解读
六、填空与简答 添加题型下试题

试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B是
(2)溶液E中,一定存在的酸根离子是
(3)写出实验过程④中可能发生的一个化学方程式
(4)此NH4NO3化肥样品中,一定混入的物质是
(1)制取少量氢氧化钠可以用如图的流程:

①步骤①属于
②写出步骤③的化学方程式
③氢氧化钠在空气中会吸收
④氢氧化钠有很强的腐蚀性,如果不小心沾到皮肤上,要立即用大量的水冲洗,然后涂上
A 硼酸溶液 B 3﹣5%的碳酸氢钠溶液 C 稀硫酸 D 石灰水
【知识点】 强碱露置在空气中的变质解读 碱的通性解读
七、计算题 添加题型下试题

①当滴入氢氧化钠溶液40g时(即图中A点),烧杯中溶液里含的溶质为(写化学式)_____。
②该反应过程中,观察到的一个明显反应现象是_____。
③当滴入10%氢氧化钠溶液80g时(即图中B点),恰好完全反应,试通过计算,求此时所得不饱和溶液的质量(计算结果精确到0.1g)。
【知识点】 溶液和化学方程式的综合计算解读 碱的通性解读
试卷分析
试卷题型(共 23题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.85 | 有机材料对环境的影响及应对措施 空气污染及其保护 | 单选题 |
| 3 | 0.85 | 二氧化碳的用途 对人体健康危害的物质 | 单选题 |
| 4 | 0.85 | 浓硫酸的稀释 量筒的正确使用方法和注意事项 气密性检测 | 单选题 |
| 5 | 0.85 | 二氧化碳物理性质及实验 一氧化碳的毒性及安全使用 甲烷 爆炸、燃烧、缓慢氧化与自燃 | 单选题 |
| 6 | 0.65 | 原子核外电子的分层排布认识 原子结构示意图含义及应用 | 单选题 |
| 7 | 0.85 | 溶液酸碱性及pH相关关系 | 单选题 |
| 8 | 0.85 | 用质量守恒定律确定物质组成 根据方程式推测化学式 | 单选题 |
| 9 | 0.85 | 微粒的观点解释现象 | 单选题 |
| 10 | 0.65 | 中和反应与复分解反应的关系 水资源的现状 | 单选题 |
| 11 | 0.65 | 质量守恒定律的微观解释 化学式图示的分析 | 单选题 |
| 12 | 0.65 | 盐类参与的反应 常见酸碱盐的溶解性 物质鉴别——选用试剂鉴别 几种常见阴、阳离子的鉴别 | 单选题 |
| 13 | 0.4 | 金属与盐溶液反应 金属与酸反应原理 物质鉴别——选用试剂鉴别 | 单选题 |
| 14 | 0.65 | 金属与盐溶液反应 除杂 | 单选题 |
| 15 | 0.4 | 含杂质的化学方程式计算 溶液和化学方程式的综合计算 | 单选题 |
| 二、填空与简答 | |||
| 16 | 0.65 | 浓硫酸做干燥剂 其他常见的盐 常见酸碱盐的溶解性 | 填空题 |
| 18 | 0.65 | 常见盐的俗名、用途 碳酸氢钠、碳酸钠、碳酸钙 | 简答题 |
| 19 | 0.65 | 固体溶解度曲线的应用 | 填空题 |
| 21 | 0.4 | 常见酸碱盐的溶解性 铵根离子的验证 常见物质的颜色 常见物质的溶解性 | 推断题 |
| 22 | 0.4 | 强碱露置在空气中的变质 碱的通性 | 流程题 |
| 三、计算题 | |||
| 17 | 0.65 | 有机物定义和常见的有机物 根据化学式计算元素质量分数 | |
| 23 | 0.4 | 溶液和化学方程式的综合计算 碱的通性 | |
| 四、实验题 | |||
| 20 | 0.65 | 制取二氧化碳的原理 一氧化碳还原氧化铜实验 | |



