江西省南昌市东湖区江西育华学校2019-2020学年九年级下学期中考化学专题分类突破-计算题
江西
九年级
专题练习
2020-04-24
591次
整体难度:
适中
考查范围:
身边的化学物质、物质的化学变化、物质构成的奥秘
江西省南昌市东湖区江西育华学校2019-2020学年九年级下学期中考化学专题分类突破-计算题
江西
九年级
专题练习
2020-04-24
591次
整体难度:
适中
考查范围:
身边的化学物质、物质的化学变化、物质构成的奥秘
一、计算题 添加题型下试题
计算题
|
困难(0.15)
真题
1. 小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。操作过程如下:请计算:
(2)反应后所得滤液中氢氧化钠的质量分数为多少?__________(写出计算过程)
(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水__________g.

(2)反应后所得滤液中氢氧化钠的质量分数为多少?__________(写出计算过程)
(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水__________g.
【知识点】 溶质质量分数结合化学方程式的计算解读
您最近一年使用:0次
2019-01-30更新
|
1716次组卷
|
17卷引用:2016年初中毕业升学考试(江西卷)化学
2016年初中毕业升学考试(江西卷)化学(已下线)2016年初中毕业升学考试(江西南昌卷)化学江西省2018届九年级中考模拟(二)化学试题人教版(江西专版)2018届九年级下册化学:中考模拟卷(二)(已下线)2年中考1年模拟 专题20 化学综合计算(已下线)专题16 综合计算(中考题)-决胜2018中考化学压轴题全揭秘精品江苏省宿迁市泗洪县明德学校2017届九年级中考模拟测试化学试题江西省南昌市南昌县2018-2019学年九年级下学期期中化学试题专题三 身边的化学物质 二 水与常见的溶液-专题练江西省南昌市东湖区江西育华学校2019-2020学年九年级下学期中考化学专题分类突破-计算题2016年广东省肇庆市四会市中考模拟化学试题2020年广东省汕头市潮阳区铜盂镇九年级学业水平质量检测化学试题2020年广东省清远市清新区中考专题三 空气、水与常见的溶液(已下线)【万唯原创】2017年山西省中考化学面对面卷练习册九年级第九单元(已下线)【万唯原创】2017年山西省中考化学试题研究卷讲解册九年级重点题专题突破专题十一(已下线)题型08 综合计算题-备战2021年中考化学热点题型专项训练2021年山东省滨州市博兴县湖滨镇寨郝中学中考三模化学试题
计算题
|
较易(0.85)
2. 做电解水实验时,常向水中加入稀硫酸以增强导电性,但硫酸并未参加反应。
(1)小明量取40 mL溶质质量分数为34%的硫酸溶液(密度为1.25 g/mL),其中溶质的质量为________g。
(2)将(1)中量取的硫酸溶液加水稀释成5%的稀硫酸,应加入水的质量为__________g。
(3)取90 g 5%的稀硫酸做电解水实验,通电一段时间后,收集到氢气的质量为2 g,求此时溶液中溶质的质量分数_______。
(1)小明量取40 mL溶质质量分数为34%的硫酸溶液(密度为1.25 g/mL),其中溶质的质量为________g。
(2)将(1)中量取的硫酸溶液加水稀释成5%的稀硫酸,应加入水的质量为__________g。
(3)取90 g 5%的稀硫酸做电解水实验,通电一段时间后,收集到氢气的质量为2 g,求此时溶液中溶质的质量分数_______。
您最近一年使用:0次
计算题
|
适中(0.65)
3. 有一道作业题:取100 g溶质质量分数为8%的氢氧化钠溶液倒入烧杯中,向其中加入100 g 19.6%的稀硫酸,充分反应后,求所得溶液中硫酸钠的质量分数。批改时老师发现两种答案:
请你分析并回答问题:
(1)氢氧化钠与硫酸反应时的质量比为________。
(2)请判断哪个结果是正确的______。(写出计算过程)
(3)反应前后钠元素的质量________(填“增大”“减小”或“不变”)。
| 结果编号 | ① | ② |
| 计算结果 | 14.2% | 7.1% |
请你分析并回答问题:
(1)氢氧化钠与硫酸反应时的质量比为________。
(2)请判断哪个结果是正确的______。(写出计算过程)
(3)反应前后钠元素的质量________(填“增大”“减小”或“不变”)。
您最近一年使用:0次
计算题
|
较难(0.4)
真题
4. 某地一辆满载浓硫酸的罐车翻到,导致25t溶质的质量分数为98%的浓硫酸泄漏,并向路基两边蔓延,接到报警后消防官兵立即赶来并用石灰浆(主要成分为氢氧化钙)中和硫酸解除了险情。请回答:
(1)25t溶质的质量分数为98%的浓硫酸中含H2SO4的质量为_______ ;
(2)计算:中和泄漏的硫酸,理论上需要多少吨氢氧化钙_______ ;
(3)处理一定量的硫酸,理论上既可用m1吨的氢氧化钙粉末,也可选用m2吨的氧化钙粉末,还可用m3吨碳酸钙粉末,则m1、m2、 m3的数值大小关系为_______________ 。
(1)25t溶质的质量分数为98%的浓硫酸中含H2SO4的质量为
(2)计算:中和泄漏的硫酸,理论上需要多少吨氢氧化钙
(3)处理一定量的硫酸,理论上既可用m1吨的氢氧化钙粉末,也可选用m2吨的氧化钙粉末,还可用m3吨碳酸钙粉末,则m1、m2、 m3的数值大小关系为
您最近一年使用:0次
2016-11-28更新
|
392次组卷
|
5卷引用:2011年初中毕业升学考试(江西南昌卷)化学
(已下线)2011年初中毕业升学考试(江西南昌卷)化学(已下线)2011年全国中考化学试题分类汇编考点24 中和反应及其应用(包括溶液的酸碱度)(已下线)2012届江苏省盐城市明达中学九年级下学期期中考试化学试卷江西省南昌市东湖区江西育华学校2019-2020学年九年级下学期中考化学专题分类突破-计算题广西玉林市博白县2015-2016学年九年级下学期期中化学试题
计算题
|
较难(0.4)
名校
5. 江西省积极落实化肥减量增效示范项目,并对在售的化肥提出明确的质量要求。某兴趣小组对市售的某钾肥进行了检测,称取5.0g样品放入烧杯中,加入适量的水溶解后,逐滴加入13%的BaCl2溶液产生沉淀的质量与所加入BaCl2溶液质量的关系如图所示(假定杂质不参加反应)。已知K2SO4+BaCl2=BaSO4↓+2KCl。

(1)恰好反应时,所用BaCl2溶液中所含溶质的质量为_____g。
(2)通过计算判断该钾肥中K2SO4的质量分数是否符合如图的包装说明_____?(写出计算过程)
(3)加入6gBaCl2溶液时溶液中K+和Cl﹣的个数比为_____。

(1)恰好反应时,所用BaCl2溶液中所含溶质的质量为_____g。
(2)通过计算判断该钾肥中K2SO4的质量分数是否符合如图的包装说明_____?(写出计算过程)
(3)加入6gBaCl2溶液时溶液中K+和Cl﹣的个数比为_____。
【知识点】 溶液和化学方程式的综合计算解读
您最近一年使用:0次
2019-04-21更新
|
246次组卷
|
3卷引用:【市级联考】江西省南昌市2019届九年级下学期4月中考模拟化学试题
计算题
|
适中(0.65)
真题
6. 建造“南昌舰”的特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验;取20g赤铁矿石样品,逐渐加入稀盐酸,充分反应。实验相关数据如图所示(假设杂质不溶于水,也不与酸反应)。
(3)该样品中铁元素的质量分数为_______,由此判断出该赤铁矿石______(填“属于”或“不属于”)富铁矿石。
(4)计算试验中所用稀盐酸溶质的质量分数______(写出计算过程)

(3)该样品中铁元素的质量分数为_______,由此判断出该赤铁矿石______(填“属于”或“不属于”)富铁矿石。
(4)计算试验中所用稀盐酸溶质的质量分数______(写出计算过程)
您最近一年使用:0次
2019-06-22更新
|
619次组卷
|
6卷引用:江西省2019年中考化学试题
计算题
|
适中(0.65)
7. 为测定粗锌样品中锌的质量分数,称取20 g粗锌样品(杂质不溶于水也不参加反应)与足量的稀盐酸反应。所加稀盐酸的质量与产生气体的质量关系如图所示。求:

(1)此过程中产生气体的最大质量是________g。
(2)粗锌样品中金属锌的质量分数为_______?(写出计算过程)
(3)若用36.5%的浓盐酸配制200 g该实验所用稀盐酸,需要水的质量为________。

(1)此过程中产生气体的最大质量是________g。
(2)粗锌样品中金属锌的质量分数为_______?(写出计算过程)
(3)若用36.5%的浓盐酸配制200 g该实验所用稀盐酸,需要水的质量为________。
您最近一年使用:0次
计算题
|
较难(0.4)
真题
8. 为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,该溶液总质量与反应时间的变化关系如图。
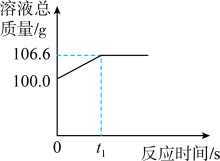
(1)上述反应产生二氧化碳的质量为多少克?
(2)计算该赤铁矿石中氧化铁的质量分数为多少?(写出计算过程)
(3)若上述反应后剩余固体质量为mg,写出计算该赤铁矿石中氧化铁质量分数的表达式(用m表示)。

(1)上述反应产生二氧化碳的质量为多少克?
(2)计算该赤铁矿石中氧化铁的质量分数为多少?(写出计算过程)
(3)若上述反应后剩余固体质量为mg,写出计算该赤铁矿石中氧化铁质量分数的表达式(用m表示)。
【知识点】 含杂质的化学方程式计算解读
您最近一年使用:0次
2016-11-28更新
|
2414次组卷
|
9卷引用:2012年初中毕业升学考试(江西卷)化学
计算题
|
适中(0.65)
9. 我市某玻璃厂排放的废水中含有碳酸钠,易造成环境污染。化学兴趣小组根据该厂设计的废水处理方案进行了如下实验:取过滤后的水样100 g,逐滴加入稀盐酸至恰好不再产生气体为止。反应过程中生成气体与所加稀盐酸的质量关系如图所示。请回答下列问题(不考虑水样中杂质的影响)。

(1)反应生成CO2气体的质量是______________。
(2)100 g水样中碳酸钠的质量是______________?(写出计算过程)
(3)加入稀盐酸的质量为a g时,溶液中的钠元素的质量是__________g。

(1)反应生成CO2气体的质量是______________。
(2)100 g水样中碳酸钠的质量是______________?(写出计算过程)
(3)加入稀盐酸的质量为a g时,溶液中的钠元素的质量是__________g。
【知识点】 溶液和化学方程式的综合计算解读 盐类参与的反应解读
您最近一年使用:0次
计算题
|
适中(0.65)
10. 向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示。

(1)反应生成沉淀的质量为_____克。
(2)镁粉完全溶解后所得溶液中的溶质成分为_____。
(3)计算氢氧化钠溶液的溶质质量分数_____(要求写出计算过程)。

(1)反应生成沉淀的质量为_____克。
(2)镁粉完全溶解后所得溶液中的溶质成分为_____。
(3)计算氢氧化钠溶液的溶质质量分数_____(要求写出计算过程)。
【知识点】 溶质质量分数结合化学方程式的计算解读 碱的通性解读
您最近一年使用:0次
2019-12-21更新
|
148次组卷
|
3卷引用:江西省南昌市东湖区育华学校2016-2017学年九年级下学期期中化学试题
计算题
|
适中(0.65)
11. 为测定某敞口放置的氢氧化钠溶液的变质情况。某同学实验并记录如图:

(1)配制上述实验所用的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是________;
(2)根据已知条件求样品溶液中碳酸钠质量是多少?_____________(写出计算过程)
(3)C烧杯溶液中溶质的化学式为___________________。(填写化学式)。

(1)配制上述实验所用的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是________;
(2)根据已知条件求样品溶液中碳酸钠质量是多少?_____________(写出计算过程)
(3)C烧杯溶液中溶质的化学式为___________________。(填写化学式)。
您最近一年使用:0次
2019-09-27更新
|
153次组卷
|
2卷引用:江西省南昌市东湖区江西育华学校2019-2020学年九年级下学期中考化学专题分类突破-计算题
计算题
|
适中(0.65)
12. 实验室有甲、乙两瓶久置的氢氧化钠固体,某学习小组为了研究其变质情况,进行了如下实验:(电子秤示数单位为g)

(1)上述实验中产生的二氧化碳气体质量为__________g。
(2)计算甲瓶固体样品中碳酸钠的质量分数_______。
(3)滴入紫色石蕊溶液后溶液为红色,说明反应后溶液呈______性。

(1)上述实验中产生的二氧化碳气体质量为__________g。
(2)计算甲瓶固体样品中碳酸钠的质量分数_______。
(3)滴入紫色石蕊溶液后溶液为红色,说明反应后溶液呈______性。
【知识点】 不含杂质的化学方程式计算解读 盐类参与的反应解读
您最近一年使用:0次
计算题
|
较易(0.85)
解题方法
13. 某补钙剂的主要成分是碳酸钙。欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图所示的操作(假设其他成分可溶于水但不参与反应)。

(1)生成二氧化碳的质量为__________g。
(2)计算该补钙剂中碳酸钙的质量分数_________。
(3)该实验中,装置的气密性对测定结果______(填“有”或“无”)影响。

(1)生成二氧化碳的质量为__________g。
(2)计算该补钙剂中碳酸钙的质量分数_________。
(3)该实验中,装置的气密性对测定结果______(填“有”或“无”)影响。
【知识点】 不含杂质的化学方程式计算解读 制取二氧化碳的原理解读
您最近一年使用:0次
2020-04-23更新
|
208次组卷
|
5卷引用:江西省南昌市东湖区江西育华学校2019-2020学年九年级下学期中考化学专题分类突破-计算题
计算题
|
较难(0.4)
解题方法
14. 请根据如图所示的实验过程和提供的数据,回答下列问题:

(1)实验过程中,产生沉淀的质量为______g。
(2)最终所得溶液的溶质质量分数为多少?(写出计算过程)
(3)原固体混合物中钠元素的质量为______g。

(1)实验过程中,产生沉淀的质量为______g。
(2)最终所得溶液的溶质质量分数为多少?(写出计算过程)
(3)原固体混合物中钠元素的质量为______g。
您最近一年使用:0次
2019-08-09更新
|
236次组卷
|
2卷引用:青岛市初中学业水平考试热身模拟卷(三)
计算题
|
适中(0.65)
真题
解题方法
15. 2018年5月18日我国第一艘国产航母试海成功,航母的许多电子元件使用了黄铜。为测定某黄铜(假设合金中仅含铜,锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:
(1)黄铜粉末完全反应生成氢气的总质量为_______g。
(2)该黄铜中铜的质量分数为多少____________? (写出计算过程)
(3)第三次实验中溶质的种类为________________。
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 |
| 烧杯中剩余物的质量(g) | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的总质量为_______g。
(2)该黄铜中铜的质量分数为多少____________? (写出计算过程)
(3)第三次实验中溶质的种类为________________。
您最近一年使用:0次
2018-06-21更新
|
3404次组卷
|
13卷引用:江西省2018年中考化学试题
江西省2018年中考化学试题(已下线)2018年中考试题分项版解析汇编【第一期】专题13-1综合计算【市级联考】四川省巴中市2019届九年级下学期中考模拟理综化学试题广东省深圳市光明区2019-2020学年九年级上学期期末化学试题河北省唐山市乐亭县2019-2020学年九年级上学期期末化学试题河南省周口市扶沟县2018-2019学年九年级上学期期末化学试题2019年山东省滨州市阳信县中考二模化学试题2019年山东省菏泽市郓城县中考四模化学试题江西省南昌市东湖区江西育华学校2019-2020学年九年级下学期中考化学专题分类突破-计算题2020年宁夏银川市第十三中学中考二模化学试题2019年湖南省株洲市攸县中考一模化学试题(已下线)第10讲 化学方程式计算-2022年中考化学一轮总复习基础通关2021年江西省赣州市初中化学教师素养大赛笔试试题
计算题
|
较难(0.4)
16. 小宇为了测定实验室中氯酸钾样品的纯度,取10g样品与1g二氧化锰混合,依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
试计算:
(1)完全反应后产生的氧气的总质量为_____________ g;
(2)样品中氯酸钾的纯度是____(写出计算过程)
(3)加热时间t1后,9.68g剩余固体中除杂质外还含有的物质为______________。
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 9.68 | 9.04 | 7.16 | 7.16 |
试计算:
(1)完全反应后产生的氧气的总质量为_____________ g;
(2)样品中氯酸钾的纯度是____(写出计算过程)
(3)加热时间t1后,9.68g剩余固体中除杂质外还含有的物质为______________。
【知识点】 化学方程式与实验的计算解读
您最近一年使用:0次
2019-03-31更新
|
332次组卷
|
4卷引用:【区级联考】江西省上饶市广丰区2019届九年级下学期第一次月考化学试题
计算题
|
较易(0.85)
解题方法
17. 为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图所示标签相符,小林取一定量该氮肥样品于烧杯中配成溶液,与足量氯化钡溶液反应,记录有关数据如下表:

[反应的化学方程式为(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl,其他成分能溶于水但不参加反应]
(1)反应共生成BaSO4的质量为____________g。
(2)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中硫酸铵的纯度是否与标签相符________。(请写出计算过程)
(3)反应前后,溶液中硫元素的质量________(选填“不变”“增大”或“减小”)。

| 反应前 | 反应后 | |
| 烧杯和样品 溶液总质量 | 氯化钡溶 液质量 | 过滤后烧杯和溶液总质量 (滤液的损失忽略不计) |
| 45 g | 55 g | 76.7 g |
[反应的化学方程式为(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl,其他成分能溶于水但不参加反应]
(1)反应共生成BaSO4的质量为____________g。
(2)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中硫酸铵的纯度是否与标签相符________。(请写出计算过程)
(3)反应前后,溶液中硫元素的质量________(选填“不变”“增大”或“减小”)。
【知识点】 含杂质的化学方程式计算解读
您最近一年使用:0次
计算题
|
适中(0.65)
18. 为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),称取40 g石灰石样品分为4等份进行实验。所得数据如下表所示:
(1)石灰石的纯度是__________。
(2)计算所用稀盐酸的溶质质量分数_______。(写出计算过程)
(3)表中m的值________(填“大于”“小于”或“等于”)100 g。
| 实验编号 | ① | ② | ③ | ④ |
| 稀盐酸的质量/g | 25 | 50 | m | 150 |
| 剩余固体的质量/g | 7.5 | 5 | 2 | 2 |
(1)石灰石的纯度是__________。
(2)计算所用稀盐酸的溶质质量分数_______。(写出计算过程)
(3)表中m的值________(填“大于”“小于”或“等于”)100 g。
您最近一年使用:0次
2020-04-23更新
|
126次组卷
|
3卷引用:江西省南昌市东湖区江西育华学校2019-2020学年九年级下学期中考化学专题分类突破-计算题
试卷分析
整体难度:适中
考查范围:身边的化学物质、物质的化学变化、物质构成的奥秘
试卷题型(共 18题)
题型
数量
计算题
18
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、计算题 | |||
| 1 | 0.15 | 溶质质量分数结合化学方程式的计算 | |
| 2 | 0.85 | 电解水原理 有关溶液浓缩、稀释的计算 溶质质量分数结合化学方程式的计算 | |
| 3 | 0.65 | 溶液和化学方程式的综合计算 酸的通性 中和反应相关实验与计算 | |
| 4 | 0.4 | 不含杂质的化学方程式计算 含杂质的化学方程式计算 溶质质量分数结合化学方程式的计算 | |
| 5 | 0.4 | 溶液和化学方程式的综合计算 | |
| 6 | 0.65 | 不含杂质的化学方程式计算 根据化学式计算元素质量分数 计算混合物中物质或元素的质量分数 | |
| 7 | 0.65 | 金属与酸反应原理 有关溶液浓缩、稀释的计算 溶液和化学方程式的综合计算 | |
| 8 | 0.4 | 含杂质的化学方程式计算 | |
| 9 | 0.65 | 溶液和化学方程式的综合计算 盐类参与的反应 | |
| 10 | 0.65 | 溶质质量分数结合化学方程式的计算 碱的通性 | |
| 11 | 0.65 | 含杂质的化学方程式计算 二氧化碳与碱的反应及实验 常见的酸碱指示剂及其变色情况 中和反应相关实验与计算 | |
| 12 | 0.65 | 不含杂质的化学方程式计算 盐类参与的反应 | |
| 13 | 0.85 | 不含杂质的化学方程式计算 制取二氧化碳的原理 | |
| 14 | 0.4 | 含杂质的化学方程式计算 化学方程式与实验的计算 溶质质量分数结合化学方程式的计算 盐类参与的反应 | |
| 15 | 0.65 | 化学方程式与实验的计算 金属与酸反应原理 金属活动顺序理解和判断 | |
| 16 | 0.4 | 化学方程式与实验的计算 | |
| 17 | 0.85 | 含杂质的化学方程式计算 | |
| 18 | 0.65 | 制取二氧化碳的原理 溶质质量分数结合化学方程式的计算 | |



