2017年广东省中考模拟化学试题
广东
九年级
模拟预测
2020-05-09
215次
整体难度:
适中
考查范围:
物质构成的奥秘、身边的化学物质、化学实验、物质的化学变化、化学与社会发展
一、选择题 添加题型下试题
| A.LiCoO4 | B.LiCoO3 | C.LiCoO2 | D.LiCoO |
【知识点】 化合价代数和的计算与应用解读
| A.增大空气与水的接触面积,可以增大氧气的溶解度 | B.析出晶体后的溶液是不饱和溶液 |
| C.用汽油洗去衣服上的油渍是乳化作用的结果 | D.溶液中可以含有多种溶质 |
A. 读出液体的体积 读出液体的体积 | B. 过滤 过滤 |
C. 熄灭酒精灯 熄灭酒精灯 | D. 稀释浓硫酸 稀释浓硫酸 |
| A.NaOH 氢氧化钠 烧碱 | B.CaO 氢氧化钙 生石灰 |
| C.Na2CO3 碳酸钠 纯碱 | D.NaCl 氯化钠 食盐 |
【知识点】 常见酸、碱的俗称及化学式解读 常见盐的俗名、用途解读

| A.a处产生白色物质 |
| B.b处生成蓝色沉淀 |
| C.c处发生复分解反应 |
| D.d处产生气泡 |
| A.NH4NO3 | B.KCl | C.NH4H2PO3 | D.KNO3 |
【知识点】 常见化肥的种类及性质解读
| 物质 | 酱油 | 厕所清洁剂 | 血浆 | 牙膏 | 肥皂水 | 橘子汁 | 草木灰水 | 柠檬汁 |
| pH | 4.8 | 1.7 | 7.4 | 8.2 | 9.2 | 3.5 | 10.6 | 2.5 |
| A.柠檬汁、食盐水、厕所清洁剂 | B.牙膏、蒸馏水、肥皂水 |
| C.草木灰水、蒸馏水、柠檬汁 | D.橘子汁、食盐水、草木灰水 |
【知识点】 常见的酸碱指示剂及其变色情况解读
| A.H2SO4、Na2CO3、NaCl |
| B.Ca(OH)2、HCl、Na2SO4 |
| C.NaOH、H2CO3、NaCl |
| D.H2SO4、NaOH、Na2CO3 |
| A.滤液中一定含Ag+、Cu2+、Zn2+、Fe2+ |
| B.滤液中一定含Fe2+,可能含Zn2+ |
| C.滤液中一定含Fe2+,Zn2+,不含Cu2+,Ag+ |
| D.滤液中一定含Zn2+、Fe2+,可能含Cu2+ |
【知识点】 金属与盐溶液反应 金属活动顺序理解和判断解读
| A.用NaOH溶液洗涤石油产品中的残余硫酸 | B.用熟石灰和硫酸铜配制波尔多液 |
| C.服用含Al(OH)3的药物治疗胃酸过多 | D.施用熟石灰改良酸性土壤 |
| A.NaNO3、HCl、Na2SO4 |
| B.NaNO3、NaCl、CuSO4 |
| C.NaCl、Na2SO4、Na2CO3 |
| D.NaOH、BaCl2、Na2SO4 |
【知识点】 复分解反应发生的条件解读 溶液中物质是否共存相关判断解读
| A.②③①④ | B.①②③④ | C.①③②④ | D.②①③④ |
①浓盐酸 ②浓硫酸 ③烧碱 ④食盐 ⑤生石灰 ⑥稀硫酸
| A.①⑥ | B.②③⑤ | C.③⑤ | D.②③④ |
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO气体 | CO2 | 通过足量氢氧化钠溶液,并干燥 |
| B | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| C | CaO固体 | CaCO3 | 加水溶解,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入足量锌粒,充分反应,过滤 |
| A.A | B.B | C.C | D.D |
二、填空与简答 添加题型下试题
(1)在生活中,我们使用的化石燃料有煤、天然气和
(2)电线外面包了一层绝缘体,它的成分是聚氯乙烯它属于
(3)常用于净水作絮凝剂的是
(4)小明家菜地里的蔬菜叶子发黄了,妈妈叫他去买化肥碳酸氢铵(NH4HCO3)来施用,当他到化肥商店时,碳酸氢铵刚好缺货,你建议他买
【知识点】 常见化肥的种类及性质解读 塑料、合成橡胶、合成纤维解读
①氖气 ②水 ③硫酸 ④葡萄糖 ⑤碳酸钠 ⑥氢氧化钙
请选择适当物质的序号填空:
(1)最常用的溶剂是
(2)可用于制造霓虹灯的是
(3)可用于金属表面除锈的是
(4)可用于造纸、纺织工业的盐是
(5)可用于改良酸性土壤的是
(6)能提供人体活动所需能量的是
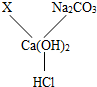
(1)若X是与其它三种不同类别的化合物,则X可以是
(2)根据图所示的物质间关系,写出其中两个化学方程式:
①
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)20℃时,把40gKNO3放入小烧杯中,然后再加100g水不断搅拌,形成溶液的质量为
(3)如图所示,把上述(2)中的小烧杯放到盛水的大烧杯中。若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,能够使小烧杯中的KNO3溶液溶质的质量分数增大的是

①浓硫酸 ②硝酸铵 ③氢氧化钠 ④冰
【知识点】 饱和溶液和不饱和溶液判断解读 固体溶解度曲线的应用解读
| 错误观点 | 否定例证 | |
| ① | 含有氧元素的化合物一定是氧化物 | |
| ② | 生成盐和水的反应一定是中和反应 |
【知识点】 氧化物的定义解读 中和反应的概念及微观本质解读
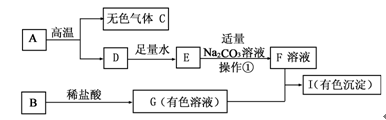
(1)写出下列物质的化学式:A.
(2)得到F溶液的操作①的名称为:
(3)若I是红褐色沉淀,则G+F→I的化学方程式为:
(4)若I是蓝色沉淀,则B+稀盐酸→G的化学方程式为:

(1)操作I的名称为
(2)石灰乳的作用是①
三、科学探究题 添加题型下试题
【猜想】猜想①:该化肥是NH4Cl,
猜想②:该化肥是
猜想③:该化肥是NH4HCO3,
猜想④:该化肥是尿素。
【实验探究】
(1)取少量样品在研钵中与熟石灰研磨,有刺激性气味的气体放出,证明猜想
(2)如(图1),另取少量样品于试管中,滴加适量水振荡,再选(图2)中

(3)在步骤(2)的试管中再滴入(图2)中的

(1)假设你是丁同学,请你也提出一个与甲、乙、丙同学不同的猜想,把猜想写在对话框中
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中, | 自己的猜想成立 |
(3)甲同学针对自己的猜想进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气体产生 | 甲的猜想不成立 |
【知识点】 碳酸根离子的验证解读 设计实验探究物质的成分解读
四、计算题 添加题型下试题
超市销售的一种加碘盐标签上的部分文字说明.请回答下列问题:

(1)碘酸钾中钾、碘、氧三种元素质量比为___________________.
(2)每袋该食盐中碘元素的质量________mg.
(3)中国营养学会推荐:一个18岁的青年每天摄入碘元素的质量为0.15mg.假设碘的来源仅靠这种加碘食盐,该青年每天摄入这种食盐应为__________g.

(1)生成的BaSO4质量为 ;
(2)氢氧化钡溶液的溶质质量分数。
【知识点】 中和反应相关实验与计算解读
试卷分析
试卷题型(共 25题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化合价代数和的计算与应用 | 单选题 |
| 2 | 0.94 | 乳化现象及应用 溶液浓稀与溶液饱和的关系 气体溶解度的影响因素 | 单选题 |
| 3 | 0.65 | 浓硫酸的稀释 量筒的正确使用方法和注意事项 酒精灯的正确使用方法和注意事项 | 单选题 |
| 4 | 0.94 | 常见酸、碱的俗称及化学式 常见盐的俗名、用途 | 单选题 |
| 5 | 0.85 | 金属与盐溶液反应 中和反应的概念及微观本质 盐类参与的反应 碳酸根离子的验证 | 单选题 |
| 6 | 0.94 | 常见化肥的种类及性质 | 单选题 |
| 7 | 0.94 | 常见的酸碱指示剂及其变色情况 | 单选题 |
| 8 | 0.85 | 酸的定义 碱的定义 盐的定义 | 单选题 |
| 9 | 0.65 | 金属与盐溶液反应 金属活动顺序理解和判断 | 单选题 |
| 10 | 0.94 | 中和反应的实际应用 | 单选题 |
| 11 | 0.85 | 复分解反应发生的条件 溶液中物质是否共存相关判断 | 单选题 |
| 12 | 0.65 | 盐类参与的反应 常见酸碱盐的溶解性 常见物质的颜色 | 单选题 |
| 13 | 0.85 | 浓酸敞口放置的变化和现象 强碱露置在空气中的变质 盐类参与的反应 | 单选题 |
| 14 | 0.65 | 金属与盐溶液反应 酸的通性 碱的通性 气体净化、干燥 | 单选题 |
| 二、填空与简答 | |||
| 15 | 0.94 | 常见化肥的种类及性质 塑料、合成橡胶、合成纤维 | 填空题 |
| 16 | 0.65 | 常见几种酸的用途 几种常见碱的物理性质及用途 常见盐的俗名、用途 糖类的组成与作用 | 填空题 |
| 17 | 0.85 | 根据碱的性质推断其他物质的性质 各类物质间反应的总结 | 推断题 |
| 18 | 0.85 | 饱和溶液和不饱和溶液判断 固体溶解度曲线的应用 | 填空题 |
| 19 | 0.94 | 氧化物的定义 中和反应的概念及微观本质 | 填空题 |
| 20 | 0.65 | 酸的通性 生石灰的性质及用途 碳酸氢钠、碳酸钠、碳酸钙 盐类参与的反应 | 推断题 |
| 21 | 0.4 | 酸的通性 碱的通性 盐类参与的反应 | 流程题 |
| 三、科学探究题 | |||
| 22 | 0.4 | 化学方程式的书写 盐类参与的反应 碳酸根离子的验证 铵根离子的验证 | |
| 23 | 0.65 | 碳酸根离子的验证 设计实验探究物质的成分 | |
| 四、计算题 | |||
| 24 | 0.65 | 根据化学式计算元素质量比 根据化学式计算元素质量分数 计算混合物中物质或元素的质量分数 | |
| 25 | 0.85 | 中和反应相关实验与计算 | |



