广东省广州市第二中学2019-2020学年九年级下学期第一次网上联考化学试题
广东
九年级
阶段练习
2020-08-20
283次
整体难度:
容易
考查范围:
物质的化学变化、身边的化学物质、化学实验、物质构成的奥秘、化学与社会发展
一、选择题 添加题型下试题
| A.利用稀有气体做电光源 | B.干冰用于人工降雨 |
| C.用活性炭去除水中异味 | D.在厨房清洁剂中加入氢氧化钠去除油污 |
A.量筒读数 | B.测 pH 值 |
C.干燥 O2气 | D.稀释浓硫酸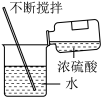 |
| A.属于复合肥料的有③⑦⑧ | B.属于有机合成材料的有①④⑩ |
| C.属于金属材料的是④⑤ | D.属于碱的有②⑥⑦⑨ |
| A.维生素多数在人体内不能合成 | B.医疗上硫酸钡可用做钡餐透视 |
| C.可以用低浓度的甲醛溶液来保鲜鱼类 | D.氯化钠可作调味品和防腐剂 |
【知识点】 常见盐的俗名、用途解读 对人体健康危害的物质解读 维生素的来源
| A.钢的含碳量很低,所以是很纯的铁 |
| B.金属Al 在空气中放置会生成致密的Al2O3 薄膜,所以金属 Al 的防腐蚀性能好 |
| C.用铜而不用银做导线,是因为铜的导电性比银好 |
| D.合金的熔点一般都高于其组分金属 |
【知识点】 金属的物理通性与用途解读 合金的认识解读
| A.80g | B.300g | C.120g | D.100g |
【知识点】 溶质质量分数的涵义解读 有关溶液浓缩、稀释的计算解读
A. 等质量、等溶质质量分数的稀硫酸中分别加入足量的镁粉和锌粉 等质量、等溶质质量分数的稀硫酸中分别加入足量的镁粉和锌粉 |
B. 向 pH=2 的H2SO4 溶液中不断加水 向 pH=2 的H2SO4 溶液中不断加水 |
C. 一定温度时,向一定量的饱和石灰水中加入生石灰 一定温度时,向一定量的饱和石灰水中加入生石灰 |
D.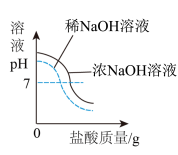 将相同溶质质量分数的稀盐酸分别滴入等体积不同溶质质量分数的NaOH 溶液 将相同溶质质量分数的稀盐酸分别滴入等体积不同溶质质量分数的NaOH 溶液 |
| A.硝酸铵是盐,溶于水吸收大量的热,食盐也是盐,所以溶于水也吸收大量的热 |
| B.氮肥氯化铵与熟石灰研磨可放出氨气,氮肥尿素与熟石灰研磨也能放出氨气 |
| C.实验室用盐酸与块状石灰石反应制取 CO2,则稀硫酸也能与块状石灰石反应制取 CO2 |
| D.氢气与空气混合点燃可能爆炸,CO 与空气混合点燃也可能爆炸 |
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | N2 | O2 | 将气体缓缓通过足量的灼热的炭 |
| B | CO2 | HCl | 通入NaOH 溶液中 |
| C | CaCl2溶液 | HCl 溶液 | 加入过量的熟石灰,过滤 |
| D | FeCl2溶液 | CuCl2溶液 | 加入过量的铁粉, 过滤 |
| A.A | B.B | C.C | D.D |
| A.CaO | B.BaCl2 | C.Na2CO3 | D.Ca(OH)2 |
【知识点】 常见的酸碱指示剂及其变色情况解读
| A.锌粒和盐酸 | B.锈铁钉和稀硫酸 | C.二氧化碳气体和石灰水 | D.盐酸和氢氧化钠溶液 |
【知识点】 酸的通性解读 无明显现象的中和反应的判断解读
| 实验图示 | 实验设计与结论 | |
| A | 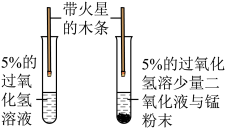 | 在 A、B 两支试管中分别加入等量 5%的过氧化氢溶液,并在 B 试管中加入少许二氧化锰粉末, 然后分别往试管中伸入带火星的木条。证明二氧化锰能促进过氧化氢分解。 |
| B | 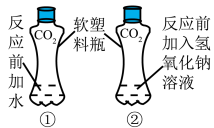 | 在体积相同并充满等量 CO2的软塑料瓶中加入等量的水(瓶①)和 NaOH 溶液(瓶②),盖好瓶盖,根据塑料瓶变瘪的程度证明 CO2与NaOH 溶液中的溶质发生了反应。 |
| C | 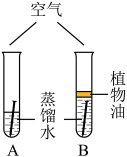 | 在 A、B 两根试管中加入少量蒸馏水,放入光亮的铁钉,并在 B 试管中加入少量植物油。该实验可得出铁生锈的条件是:铁需要同时与水、空气接触。 |
| D | 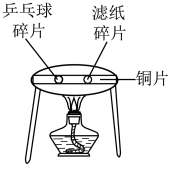 | 在铜片上分别放置乒乓球碎片和滤纸碎片,并用酒精灯加热,可得出燃烧的条件之一是:温度必须达到可燃物的着火点。 |
| A.A | B.B | C.C | D.D |
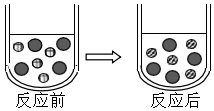
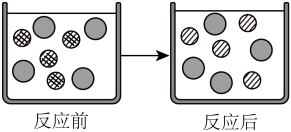
A. 表示氢离子 表示氢离子 | B. 表示硫酸根离子 表示硫酸根离子 |
C. 表示铁离子 表示铁离子 | D.若用稀盐酸代替稀硫酸,则 表示氯离子 表示氯离子 |
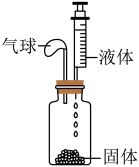
| A.固体:硝酸铵;液体:水 | B.固体:氢氧化钠;液体:水 |
| C.固体:二氧化锰;液体:双氧水 | D.固体:氯化钠;液体:水 |
【知识点】 过氧化氢制取氧气实验解读 溶解时能量的变化解读
| A.Fe | B.CuO | C.Ag | D.Fe2O3 |
【知识点】 应用金属活动性解释相关现象解读 酸的通性解读
二、填空与简答 添加题型下试题
(1)用洗涤剂去除油污,是利用洗涤剂的
(2)农村地区的生活用水多是硬水,生活中常用
(3)不锈钢主要成分是铁、铬(Cr)、镍(Ni)。其中,铬常见化合价是+2、+3 和+6,铬的+6 价的氧化物的化学式是
(4)现有①稀硫酸 ②盐酸 ③硝酸 ④醋酸 ⑤烧碱 ⑥熟石灰 ⑦生石灰 ⑧小苏打,请从中选择适当的物质,用化学用语回答以下问题:
⑤⑥中共同含有的离子是
(5)目前广州使用主要燃气是天然气,燃烧时热量高且产物都是无毒气体。它燃烧的化学方程式是
(6)通常用胃舒平[主要含氢氧化铝]治疗胃酸过多的反应方程式
三、综合应用题 添加题型下试题
(1)海水晒盐是海水在常温下蒸发得到氯化钠的过程,实验室用氯化钠溶液模拟该过程:

根据上图所示现象,与B 溶液中溶质质量相等的溶液是
(2)氯化钠、硝酸钾、硫酸钠的溶解度曲线如图所示。40℃时,在三个各盛有 100g 水的容器中分别加入甲、乙、丙三种纯净物(不含结晶水,不与水反应)各 55g,充分溶解后,情况如下表:
| 物质 | 甲 | 乙 | 丙 |
| 未溶解固体的质量/g | 19 | 5 | 0 |
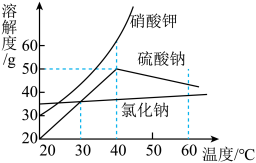
则 40℃时甲物质的溶解度是
(3)为了除去氯化钠固体中混有的少量硫酸钠杂质,我们可以先把固体放入适量的水中全部溶解, 然后进行下列选项中的操作
A 加热蒸发至出现较多固体时,停止加热,利用余热使液体蒸干
B 加热蒸发至剩余少量液体
C 过滤后取滤液
D 过滤后取滤渣
(4)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁。若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度。某研究小组在控制反应温度是 20~25℃和浓海水质量为 1109g 不变的条件下,进行下述对比实验, 数据如下:
| 实验 | 碳酸钠加入量/g | 搅拌速度. r/min | 反应时间/h | 钙除去率/% |
| a | 1.78 | 200 | 3 | 44.8 |
| b | 2.32 | 200 | 3 | 60.2 |
| c | 2.32 | 125 | 4 | 55.1 |
| d | 2.32 | 200 | 4 | 64.6 |
②搅拌速率越快,反应时间越长,则消耗能源越多。为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件。在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是
A 200r/min,3.5h B 200r/min,4.5h C 175 r/min,4h D 175 r/min,3.5h
四、填空与简答 添加题型下试题
已知步骤 1 反应:2Al+2NaOH+2H2O= 2NaAlO2+3H2↑
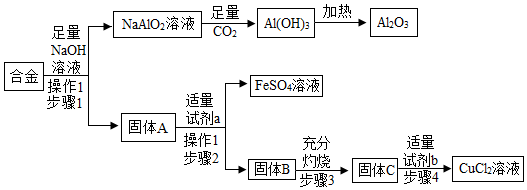
(1)操作 1 的名称是
(2)往 NaAlO2溶液中通入足量 CO2,可得到 Al(OH)3 沉淀和一种盐,此盐是焙制糕点所用的发酵粉的主要成分之一,医疗上,可用于治疗胃酸过多症。该反应的化学方程式是(提示:方程式配平后,各生成物化学式前的化学计量数均为 1)
(3)请写出步骤 3 的化学反应方程式
(4)若合金中铝占 30%,则 180g 合金最终可获得 Al2O3
(5)试剂 b 的化学式是
(6)若将足量铝片放入 CuCl2溶液中,可观察到现象为
【知识点】 金属活动顺序理解和判断解读
五、实验题 添加题型下试题
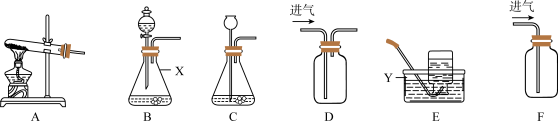
(1)写出图中标号仪器的名称:X
(2)CO2的制取方法有多种,若用加热碳酸氢钠固体制取 CO2,应选用的发生装置为
(3)经过研究,发现硫酸铜可以作过氧化氢制取氧气的催化剂,下列说法正确的是
A 反应前后,硫酸铜的质量和性质都不变 B 加入硫酸铜可提高制得氧气的质量
C 加入硫酸铜可加快过氧化氢分解制得氧气的速率 D 若不加硫酸铜,则过氧化氢不能分解制得氧气
(4)若选用KClO3来制取纯净的氧气,则反应的化学方程式是
(5)小佳欲制取硫化氢气体,查阅信息得知利用硫化亚铁固体与稀硫酸混合即可得到硫化氢,该化学变化属于
【知识点】 氯酸钾制取氧气解读 制取二氧化碳实验的改进解读
六、科学探究题 添加题型下试题
(1)步骤一:取少量白色粉末于试管中,加入足量蒸馏水,得无色透明溶液,由此可知,粉末中一定不含有
(2)步骤二:再取少量白色粉末于试管中,并滴加过量的稀盐酸,观察到
(3)请你根据该同学实验所得现象,推测这一粉末的可能组成。
推测一:碳酸钠 推测二:碳酸钠、氢氧化钠;
推测三:碳酸钠、硫酸钠 推测四:
(4)若要证明推测三成立(即该粉末由碳酸钠、硫酸钠组成),请你在该同学实验基础上设计后续实验,以确定这包粉末的组成。
| 实验操作 | 预期现象和必要结论 |
| 步骤.1:取少量该同学做的步骤二反应后的溶液于试管中,加入 | |
| 步骤2:重新取少量白色粉末于试管中,加足量蒸馏水溶解,加入 | |
| 步骤3:取少量 |
试卷分析
导出试卷题型(共 20题)
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学性质和物理性质 活性炭的吸附性 几种常见碱的物理性质及用途 | 单选题 |
| 2 | 0.85 | 浓硫酸的稀释 溶液的酸碱性的判断与pH的测定 量筒的正确使用方法和注意事项 | 单选题 |
| 3 | 0.85 | 碱的定义 常见化肥的种类及性质 常见物品质材的辨别 | 单选题 |
| 4 | 0.94 | 常见盐的俗名、用途 对人体健康危害的物质 维生素的来源 | 单选题 |
| 5 | 0.85 | 金属的物理通性与用途 合金的认识 | 单选题 |
| 6 | 0.85 | 溶质质量分数的涵义 有关溶液浓缩、稀释的计算 | 单选题 |
| 7 | 0.65 | 金属与酸反应的图像 图像分析溶质质量分数的变化 溶液酸碱性及pH相关关系 | 单选题 |
| 8 | 0.85 | 溶解时能量的变化 鉴别常见化肥 | 单选题 |
| 9 | 0.65 | 盐类参与的反应 常见酸碱盐的溶解性 除杂 | 单选题 |
| 10 | 0.85 | 常见的酸碱指示剂及其变色情况 | 单选题 |
| 11 | 0.65 | 酸的通性 无明显现象的中和反应的判断 | 单选题 |
| 12 | 0.4 | 催化剂的概念、性质与用途 二氧化碳与碱的反应及实验 控制变量法在实验设计中的应用 | 单选题 |
| 13 | 0.94 | 金属与酸反应原理 | 单选题 |
| 14 | 0.85 | 过氧化氢制取氧气实验 溶解时能量的变化 | 单选题 |
| 15 | 0.65 | 应用金属活动性解释相关现象 酸的通性 | 单选题 |
| 二、填空与简答 | |||
| 16 | 0.85 | 化学方程式的书写 常见几种酸的用途 几种常见碱的物理性质及用途 | 填空题 |
| 18 | 0.4 | 金属活动顺序理解和判断 | 流程题 |
| 三、综合应用题 | |||
| 17 | 0.4 | 固体溶解度曲线的应用 控制变量法在实验设计中的应用 海水晒盐原理及流程 粗盐提纯 | |
| 四、实验题 | |||
| 19 | 0.65 | 氯酸钾制取氧气 制取二氧化碳实验的改进 | |
| 五、科学探究题 | |||
| 20 | 0.65 | 化学方程式的书写 盐类参与的反应 几种常见阴、阳离子的鉴别 设计实验探究物质的成分 | |



