16. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(图1)
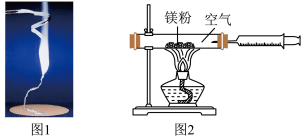
(1)镁跟氧气反应的化学方程式是
_____(2)小明通过称量发现:图1中石棉网上收集到产物的质量小于镁条的质量。你认为其原因可能是
____(3)小红按图2装置改进实验,验证质量守恒定律,她却发现产物中还有一些黄色固体。
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气反应生成黄色的氮化镁(Mg
3N
2)固体;
③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
【做出猜想】黄色固体为Mg
3N
2【实验探究】
| 实验操作 | 实验现象及结论 |
如图,取燃烧产物于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B
 | 现象______
结论:燃烧产物中含Mg3N2 |
【反思与交流】空气中N
2的含量远大于O
2的含量,而镁条在空气中燃烧生成的MgO却远多于,为什么呢?请给出合理的解释。
_______【拓展延伸】①如果用图2装置(气密性良好)和药品(足量)测定空气中氧气含量,该实验所测得的氧气体积分数
_______ (填:“大于”、“小于” 或“等于”) 1/5。
②有氧化镁和另一种金属氧化物组成的混合物共4g。经测定其中含有氧元素1.8g,则另一种金属氧化物是
( )A Al
2O
3 B CuO C CaO