湖北省黄冈市八校2020-2021学年九年级下学期3月联考化学试题
湖北
九年级
阶段练习
2021-04-13
318次
整体难度:
适中
考查范围:
身边的化学物质、化学与社会发展、物质的化学变化、物质构成的奥秘、化学实验、物化综合试题
湖北省黄冈市八校2020-2021学年九年级下学期3月联考化学试题
湖北
九年级
阶段练习
2021-04-13
318次
整体难度:
适中
考查范围:
身边的化学物质、化学与社会发展、物质的化学变化、物质构成的奥秘、化学实验、物化综合试题
一、选择题 添加题型下试题
选择题-单选题
|
容易(0.94)
解题方法
1. 下列垃圾归类不合理 的是
A | B | C | D | |
垃圾 | 废易拉罐 | 废矿泉水瓶 | 废荧光灯管 | 茶叶渣 |
垃圾分类 |
|
|
|
|
| A.A | B.B | C.C | D.D |
【知识点】 废弃金属对环境的影响及回收解读 垃圾分类(上海) 垃圾分类(北京)
您最近一年使用:0次
2020-12-19更新
|
89次组卷
|
2卷引用:北京市密云区2020-2021学年九年级上学期期中化学试题
选择题-单选题
|
适中(0.65)
解题方法
2. 美国化学会发布的2018年科研圈九件大事,其中一件就是气候变化持续导致全球范围内的洪灾和干旱等自然灾害的发生以及地球整体温度上升。科学家不断呼吁减少碳排放,并对可能造成的危害做出更多警示。为解决日益加剧的温室效应等问题,科学家正在研究建立如图所示的二氧化碳新循环体系,结合关系图,下列说法正确的是( )
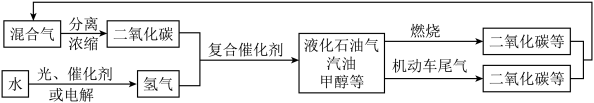
①化学变化中元素种类是守恒的 ②燃烧时化学能可以转化为热能和光能 ③二氧化碳也是种重要的资源 ④光能或电能可以转化为化学能 ⑤无机物和有机物可以相互转化

①化学变化中元素种类是守恒的 ②燃烧时化学能可以转化为热能和光能 ③二氧化碳也是种重要的资源 ④光能或电能可以转化为化学能 ⑤无机物和有机物可以相互转化
| A.①②③ | B.①②④⑤ | C.①④⑤ | D.①②③④⑤ |
您最近一年使用:0次
选择题-单选题
|
较易(0.85)
解题方法
3. 中国科学技术大学10级少年班校友、美国麻省理工学院“95后”博士生曹原,曾因发现让石墨烯实现超导的方法而被誉为“石墨烯的驾驭者”。石墨烯是目前世界上最薄的材料,只有一张A4纸厚度的十万分之一,一根头发丝直径的五十万分之一。石墨烯可看作将石墨的层状结构一层层的剥开得到的单层碳原子。电子在石墨烯中的运动速度达到光速的1300 ,手机充电可以实现“秒充”;用石墨烯代替硅,可提高电子芯片的性能;一定条件下,将氢气加入到石墨烯中可得到突破性的高分子新材料石墨烷(CH)n。

下列说法中,正确的是( )

下列说法中,正确的是( )
| A.石墨烯是一种绝缘材料 | B.石墨烷属于高分子化合物 |
| C.石墨烷中的 n 可以是 1 | D.石墨烷在氧气中完全燃烧的产物是 CO2 |
您最近一年使用:0次
选择题-单选题
|
较易(0.85)
解题方法
4. 下列粒子符号或文字化学式书写不正确的有( )
①3个甲烷分子3CH4②蔗糖C6H12O6③三个硫酸根离子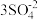 ④2个氯气分子2Cl⑤磷酸二氢铵NH4H2PO4⑥正二价的镁元
④2个氯气分子2Cl⑤磷酸二氢铵NH4H2PO4⑥正二价的镁元 ⑦氧化铁FeO ⑧烧碱Na2CO3
⑦氧化铁FeO ⑧烧碱Na2CO3
①3个甲烷分子3CH4②蔗糖C6H12O6③三个硫酸根离子
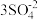 ④2个氯气分子2Cl⑤磷酸二氢铵NH4H2PO4⑥正二价的镁元
④2个氯气分子2Cl⑤磷酸二氢铵NH4H2PO4⑥正二价的镁元 ⑦氧化铁FeO ⑧烧碱Na2CO3
⑦氧化铁FeO ⑧烧碱Na2CO3| A.①②③⑤⑦ | B.②④⑤⑦⑧ | C.②③④⑦⑧ | D.③④⑤⑦⑧ |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
5. 化学反应前后物质所含元素化合价发生变化的反应叫做氧化还原反应。如下图所示各区所列错误的一项是( )
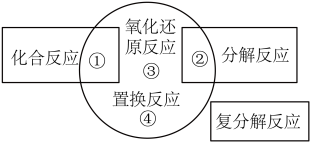

| A.③:Ba(OH)2+H2SO4=BaSO4↓+2H2O |
B.②:2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
C.①:S+O2 SO2 SO2 |
| D.④:Fe+H2SO4=FeSO4+H2↑ |
您最近一年使用:0次
选择题-单选题
|
困难(0.15)
真题
6. 在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物X.取一定质量的AgNO3固体充分光照,测得反应后生成Ag、O2、X的质量分别为21.6g、mg、9.2g。下列说法正确的是( )
| A.AgNO3固体应密封保存在无色细口瓶中 |
| B.m=3.2 |
| C.X的化学式为NO |
| D.该反应方程式中Ag与O2的化学计量数之比为3:2 |
您最近一年使用:0次
2018-07-30更新
|
1844次组卷
|
12卷引用:江苏省南通市2018年中考化学试题
江苏省南通市2018年中考化学试题【校级联考】江苏省扬州市高邮市2019届九年级上学期期末考试化学试题鲁教版九年级上册第五单元 第一节 化学反应中的质量守恒2019年山东省淄博市张店区中考二模化学试题(已下线)专题01 质量守恒定律(讲练)决胜2020年中考化学压轴题全揭秘(全国通用)2019年辽宁省本溪市中考三模化学试题江苏省镇江市丹徒区江心实验学校2019-2020学年九年级下学期4月月考化学试题湖北省黄冈市八校2020-2021学年九年级下学期3月联考化学试题江苏省无锡市惠山区八校2020-2021学年九年级上学期12月月考化学试题2020年江苏省苏州市新草桥中学中考二模化学试题山东省威海市乳山市2022-2023学年九年级下学期3月能力素养测试化学试题2019年四川省乐山市五通桥区中考二调化学试题
选择题-单选题
|
适中(0.65)
解题方法
7. 已知:焦性没食子酸的碱性溶液可吸收 O2,碘化亚铁(FeI2)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,实验室用如图装置制备 FeI2,下列说法错误的是( )


| A.空气的主要作用是将产生的 FeI2吹入收集器中 |
| B.冷水的作用是将升华的 FeI2凝华便于收集,使用粗玻璃管可以防止堵塞 |
| C.浓硫酸的作用是防止水蒸气进入收集器而引起 FeI2潮解 |
D.向 FeI2溶液中通入等少量的 Cl2,反应的化学方程式为: |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
名校
8. FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu═cCuCl2+dX.向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法不正确的是( )
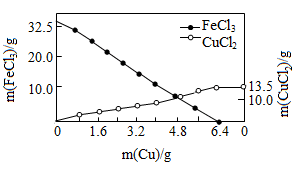

| A.方程式中a和c的比为1:2 |
| B.化学计量数d=2 |
| C.完全反应后,生成X的质量为25.4g |
| D.X为FeCl2 |
您最近一年使用:0次
2019-12-23更新
|
132次组卷
|
3卷引用:江苏省南通市海安市十校2019-2020学年九年级上学期12月月考化学试题
选择题-单选题
|
适中(0.65)
解题方法
9. A~E 是初中化学常见的物质,它们的相互转化关系如图中所示。“-”表示相互间能反应,“→”表示能转化。部分反应条件、反应物、生成物已略去。下列说法不正确的是( )


| A.如果A是常见的溶剂,则物质B和E用水可以鉴别 |
| B.图中所有转化和反应均可以通过复分解反应完成 |
| C.若D是黑色固体,A的溶液呈蓝色,则C的类别可能是盐或碱 |
| D.A、D、C 三种物质的类别可能相同 |
您最近一年使用:0次
选择题-单选题
|
较难(0.4)
名校
解题方法
10. 已知: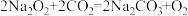 ,在密闭容器中,将6.6gCO2与一定量的Na2O2固体充分反应后,气体变为3.8g。下列说法错误的是( )
,在密闭容器中,将6.6gCO2与一定量的Na2O2固体充分反应后,气体变为3.8g。下列说法错误的是( )
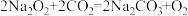 ,在密闭容器中,将6.6gCO2与一定量的Na2O2固体充分反应后,气体变为3.8g。下列说法错误的是( )
,在密闭容器中,将6.6gCO2与一定量的Na2O2固体充分反应后,气体变为3.8g。下列说法错误的是( )| A.反应后的固体是纯净物 |
| B.3.8g气体通过足量NaOH溶液后,气体减少2.2g |
| C.3.8g气体是CO2和O2的混合物 |
| D.生成Na2CO3的质量为15.9g |
【知识点】 不含杂质的化学方程式计算解读
您最近一年使用:0次
2021-04-08更新
|
447次组卷
|
3卷引用:湖北省黄冈市八校2020-2021学年九年级下学期3月联考化学试题
二、填空与简答 添加题型下试题
填空与简答-流程题
|
适中(0.65)
11. 工业上利用氟碳铈矿(主要成分为CeFCO3)提取CeCl3的一种工艺流程如下:
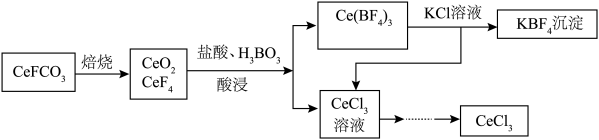
(1)流程中Ce(BF4)3转化成KBF4的基本反应类型是________________________ 。
(2)在足量氧气中高温焙烧CeFCO3,化学方程式为_______________________ 。
(3)流程涉及的化合物中,铈元素的化合价为______________________ 价。
(4)酸浸过程中,CeO2与盐酸反应有刺激性气味的气体单质生成,且化学方程式中CeO2与盐酸的化学计量数之比为1:4,则化学方程式为_______________________ 。

(1)流程中Ce(BF4)3转化成KBF4的基本反应类型是
(2)在足量氧气中高温焙烧CeFCO3,化学方程式为
(3)流程涉及的化合物中,铈元素的化合价为
(4)酸浸过程中,CeO2与盐酸反应有刺激性气味的气体单质生成,且化学方程式中CeO2与盐酸的化学计量数之比为1:4,则化学方程式为
您最近一年使用:0次
2020-07-28更新
|
808次组卷
|
6卷引用:云南省昆明市2020年中考化学试题
云南省昆明市2020年中考化学试题湖北省黄冈市八校2020-2021学年九年级下学期3月联考化学试题(已下线)必刷卷03-2021年中考化学考前信息必刷卷(云南专用)(已下线)必刷卷03-2021年中考化学考前信息必刷卷(临沂专用)(已下线)专题09 化学工艺流程图题(九)-2022年中考化学考前查漏补缺提分专题精练(全国通用)(已下线)2023年中考风向标+云南+工业流程
填空与简答-简答题
|
较难(0.4)
名校
解题方法
12. (1)根据初中化学知识,硫酸铜溶液与氢氧化钠溶液反应可得到蓝色沉淀,进一步将沉淀加热可生成黑色物质,请写出有关反应的化学方程式:
①________________ ,②________________ .
(2)小明做了这个实验.他在试管中倒入2mL CuSO4溶液,再加入一定量NaOH溶液,结果得到的沉淀并不是蓝色的,而是浅绿色的;将此浊液加热直至沸腾,观察不到有分解变黑生成CuO的迹象.这是为什么呢?小明通过查找资料得知,该浅绿色沉淀物可能是溶解度极小的碱式硫酸铜,其化学式为Cu4(OH)6SO4
①请帮小明写出生成浅绿色沉淀的有关反应的化学方程式______________ .
②请帮小明设计一个实验,证明该浅绿色沉淀中含有硫酸根.________________ .
①
(2)小明做了这个实验.他在试管中倒入2mL CuSO4溶液,再加入一定量NaOH溶液,结果得到的沉淀并不是蓝色的,而是浅绿色的;将此浊液加热直至沸腾,观察不到有分解变黑生成CuO的迹象.这是为什么呢?小明通过查找资料得知,该浅绿色沉淀物可能是溶解度极小的碱式硫酸铜,其化学式为Cu4(OH)6SO4
①请帮小明写出生成浅绿色沉淀的有关反应的化学方程式
②请帮小明设计一个实验,证明该浅绿色沉淀中含有硫酸根.
【知识点】 化学方程式的书写解读 设计实验探究物质的成分解读
您最近一年使用:0次
2019-09-03更新
|
104次组卷
|
3卷引用:2019年四川省绵阳市南山中学高中部自主招生模拟化学试题
填空与简答-填空题
|
适中(0.65)
解题方法
13. 如图为在浓度为 0.05%的 Ba(OH)2水溶液中逐渐滴加0.05%的稀H2SO4溶液的过程中,稀H2SO4的体积与混合溶液导电性的示意图。请回答下列问题:

(1)加入10mL时稀H2SO4溶液中存在最多的离子是______ 。
(2)Ba(OH)2与H2SO4反应的化学方程式为______ 。
(3)导电性最低时,溶液中存在最多的离子是______ ,因为______ 。
(4)加入25mL稀硫酸时,导电性最低的原因为______ 。

(1)加入10mL时稀H2SO4溶液中存在最多的离子是
(2)Ba(OH)2与H2SO4反应的化学方程式为
(3)导电性最低时,溶液中存在最多的离子是
(4)加入25mL稀硫酸时,导电性最低的原因为
【知识点】 酸碱溶液导电的原理解读 中和反应的概念及微观本质解读
您最近一年使用:0次
三、综合应用题 添加题型下试题
综合应用题
|
较难(0.4)
14. 天然气的主要成分是甲烷(CH4),作为一种洁净环保的优质能源。甲烷是一种无色、无味、密度比空气小、难溶于水的气体。甲烷在高温下可以分解为炭黑和氢气,炭黑可用来制造高级油墨。请阅读有关甲烷材料,完成下列各题:
(1)科研人员以纳米镍粒子为催化剂,用二氧化碳和氢气混合制造甲烷,下列说法中正确的是______ 。
①上述反应过程用化学方程可表示为: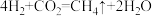
②该反应属于置换反应
③甲烷是天然气和沼气的主要成分
④纳米镍粒子在反应前后的质量不变
(2)实验室用加热无水醋酸钠与碱石灰固体混合物来制取并收集一瓶较为纯净的甲烷气体,则应选用如图中的______ 装置(填字母)。
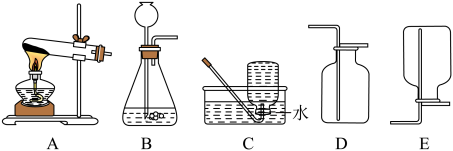
(3)甲烷分解的化学方程式为: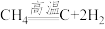 ,进行该反应必须使甲烷处于特别的环境中,你认为此处所指的特别环境是
,进行该反应必须使甲烷处于特别的环境中,你认为此处所指的特别环境是______ 。
(4)甲烷与氯气(Cl2)混合后在光照下可以发生下列反应:常温下,CH3Cl是气体,CH2Cl2、CHCl3、CCl4都是液体。CCl4可用于灭火,其原因是______ 。
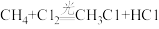
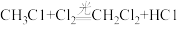


A CCl4是液体
B CCl4含有 Cl 元素
C CCl4中碳元素已经是最高的+4价,最稳定
D CCl4的相对分子质量最大
(5)把 CH3Cl 缓慢通入被加热的烧碱溶液中,发生的反应为: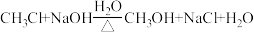 为了验证该反应的存在,某化学兴趣小组的同学做了下列实验:
为了验证该反应的存在,某化学兴趣小组的同学做了下列实验:
a把一定量的CH3Cl缓慢通入被稀硝酸酸化的AgNO3溶液中,无白色沉淀产生,CH3Cl全部从溶液中逸出。
b把一定量CH3Cl缓慢通入被加热的烧碱溶液中,有少部分CH3Cl从溶液中逸出。一段时间后停止加热,待溶液温度降到接近室温后,取少量反应后的混合液于另一试管中,滴加稀硝酸至溶液呈酸性,再滴入AgNO3溶液,发现有白色沉淀产生。
①该实验第 a 步的目的是______ ;
②该实验现象说明了什么?______ ;
③实验b中,滴加稀硝酸至溶液呈酸性的原因是______ 。
(6)如图是用模型表示出来的甲烷燃烧的过程。下列说法中正确的是______ 。
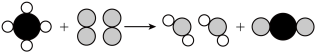
①反应过程中剩余气体为氧气;
②反应后生成物的总质量大于反应物的总质量;
③参加反应的甲烷和氧气的分子个数比为 1:2;
④反应前后分子的总数不变;
⑤反应前后原子的总数不变。
(7)在标准大气压下,在如图所示的1L容器中分别装满了氧气、甲烷和二氧化碳。下列对于气体的说法不正确的是______ 。

①分子个数相等;
②氧气的质量最大;
③甲烷的原子个数最多;
④二氧化碳的分子运动速度最快;
(1)科研人员以纳米镍粒子为催化剂,用二氧化碳和氢气混合制造甲烷,下列说法中正确的是
①上述反应过程用化学方程可表示为:
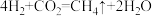
②该反应属于置换反应
③甲烷是天然气和沼气的主要成分
④纳米镍粒子在反应前后的质量不变
(2)实验室用加热无水醋酸钠与碱石灰固体混合物来制取并收集一瓶较为纯净的甲烷气体,则应选用如图中的

(3)甲烷分解的化学方程式为:
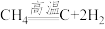 ,进行该反应必须使甲烷处于特别的环境中,你认为此处所指的特别环境是
,进行该反应必须使甲烷处于特别的环境中,你认为此处所指的特别环境是(4)甲烷与氯气(Cl2)混合后在光照下可以发生下列反应:常温下,CH3Cl是气体,CH2Cl2、CHCl3、CCl4都是液体。CCl4可用于灭火,其原因是
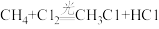
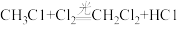


A CCl4是液体
B CCl4含有 Cl 元素
C CCl4中碳元素已经是最高的+4价,最稳定
D CCl4的相对分子质量最大
(5)把 CH3Cl 缓慢通入被加热的烧碱溶液中,发生的反应为:
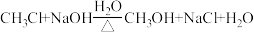 为了验证该反应的存在,某化学兴趣小组的同学做了下列实验:
为了验证该反应的存在,某化学兴趣小组的同学做了下列实验: a把一定量的CH3Cl缓慢通入被稀硝酸酸化的AgNO3溶液中,无白色沉淀产生,CH3Cl全部从溶液中逸出。
b把一定量CH3Cl缓慢通入被加热的烧碱溶液中,有少部分CH3Cl从溶液中逸出。一段时间后停止加热,待溶液温度降到接近室温后,取少量反应后的混合液于另一试管中,滴加稀硝酸至溶液呈酸性,再滴入AgNO3溶液,发现有白色沉淀产生。
①该实验第 a 步的目的是
②该实验现象说明了什么?
③实验b中,滴加稀硝酸至溶液呈酸性的原因是
(6)如图是用模型表示出来的甲烷燃烧的过程。下列说法中正确的是

①反应过程中剩余气体为氧气;
②反应后生成物的总质量大于反应物的总质量;
③参加反应的甲烷和氧气的分子个数比为 1:2;
④反应前后分子的总数不变;
⑤反应前后原子的总数不变。
(7)在标准大气压下,在如图所示的1L容器中分别装满了氧气、甲烷和二氧化碳。下列对于气体的说法不正确的是

①分子个数相等;
②氧气的质量最大;
③甲烷的原子个数最多;
④二氧化碳的分子运动速度最快;
您最近一年使用:0次
四、科学探究题 添加题型下试题
科学探究题
|
困难(0.15)
解题方法
15. 实验探究和证明推理是提升认知的重要手段。
某同学将氢氧化钠溶液加入到一定量的稀氯化铜溶液中,出现蓝绿色不溶于水的固体。该同学对生成蓝绿色固体而不是蓝色固体的现象产生了疑惑。
【查阅资料】
Ⅰ CuCl2溶液与NaOH溶液反应可生成蓝色固体(Cu(OH)2)。在氢氧化钠较少的情况下会生成蓝绿色固体——碱式氯化铜(Cu(OH)Cl)。碱式氯化铜不溶于水,能与酸反应。
Ⅱ Cu(OH)2在60℃开始分解生成两种氧化物,100℃分解完全,碱式氯化铜在300℃开始分解生成氧化铜、水和氯化氢,在400℃分解完全。
【提出猜想】
(1)蓝绿色固体可能是:①Cu(OH)2;②Cu(OH)Cl:③_________ ;
(2)猜想①的理由是:__________ (用化学方程式表示);
【进行实验】
(3)该同学取31.25g蓝绿色固体,加热至100℃出现黑色固体,则猜想________ 不正确。继续加热到400℃至质量不再改变,并使产生的气体全部缓缓通过如图所示装置(装置中药品足量)

已知实验所得数据
①最终得到剩余固体24.00g;
②与硝酸银溶液反应得到的沉淀经过滤、洗涤和低温烘干,得到固体14.35g。
完成下列问题:
(4)判断固体已洗净的方法是:取最后一次洗液,滴加含________ (填离子符号)的溶液,无现象;
(5)通过上述实验数据计算蓝绿色固体中铜元素和氯元素的质量比________ (填最简整数比);
【得出结论】猜想③成立
【拓展延伸】
(6)碱式氯化铜常作为动物饲料的添加剂,则该碱式氯化铜与胃液发生反应的化学方程式为________ ;
(7)如果欲使HCl和CuCl2的混合溶液中的溶质只有CuCl2,可向其中加入过量的_____ (填序号);
A CuO B Cu(OH)2 C Cu D Cu(NO3)2
(8)为使实验中生成蓝色固体,少出现蓝绿色固体,应作______ 改进(选填序号)。
A实验中将氯化铜溶液滴加到氢氧化钠溶液中
B实验中应提供足量、较浓的氢氧化钠溶液
C实验应该在80℃的水浴中进行
某同学将氢氧化钠溶液加入到一定量的稀氯化铜溶液中,出现蓝绿色不溶于水的固体。该同学对生成蓝绿色固体而不是蓝色固体的现象产生了疑惑。
【查阅资料】
Ⅰ CuCl2溶液与NaOH溶液反应可生成蓝色固体(Cu(OH)2)。在氢氧化钠较少的情况下会生成蓝绿色固体——碱式氯化铜(Cu(OH)Cl)。碱式氯化铜不溶于水,能与酸反应。
Ⅱ Cu(OH)2在60℃开始分解生成两种氧化物,100℃分解完全,碱式氯化铜在300℃开始分解生成氧化铜、水和氯化氢,在400℃分解完全。
【提出猜想】
(1)蓝绿色固体可能是:①Cu(OH)2;②Cu(OH)Cl:③
(2)猜想①的理由是:
【进行实验】
(3)该同学取31.25g蓝绿色固体,加热至100℃出现黑色固体,则猜想

已知实验所得数据
①最终得到剩余固体24.00g;
②与硝酸银溶液反应得到的沉淀经过滤、洗涤和低温烘干,得到固体14.35g。
完成下列问题:
(4)判断固体已洗净的方法是:取最后一次洗液,滴加含
(5)通过上述实验数据计算蓝绿色固体中铜元素和氯元素的质量比
【得出结论】猜想③成立
【拓展延伸】
(6)碱式氯化铜常作为动物饲料的添加剂,则该碱式氯化铜与胃液发生反应的化学方程式为
(7)如果欲使HCl和CuCl2的混合溶液中的溶质只有CuCl2,可向其中加入过量的
A CuO B Cu(OH)2 C Cu D Cu(NO3)2
(8)为使实验中生成蓝色固体,少出现蓝绿色固体,应作
A实验中将氯化铜溶液滴加到氢氧化钠溶液中
B实验中应提供足量、较浓的氢氧化钠溶液
C实验应该在80℃的水浴中进行
您最近一年使用:0次
2020-12-08更新
|
449次组卷
|
5卷引用:江苏省南通市如皋实验初中2018二模化学
试卷分析
整体难度:适中
考查范围:身边的化学物质、化学与社会发展、物质的化学变化、物质构成的奥秘、化学实验、物化综合试题
试卷题型(共 15题)
题型
数量
选择题
10
填空与简答
3
综合应用题
1
科学探究题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 废弃金属对环境的影响及回收 垃圾分类(上海) 垃圾分类(北京) | 单选题 |
| 2 | 0.65 | 质量守恒定律的微观解释 二氧化碳的用途 有机化合物 能量转化与化学变化的关系 | 单选题 |
| 3 | 0.85 | 石墨的相关知识 | 单选题 |
| 4 | 0.85 | 化学式书写及读法 化学符号周围数字的含义 常见元素、原子团的化合价 常见盐的俗名、用途 | 单选题 |
| 5 | 0.65 | 化合反应 分解反应 置换反应 复分解反应的定义 | 单选题 |
| 6 | 0.15 | 质量守恒定律的应用 有关质量守恒定律的计算 用质量守恒定律确定物质组成 | 单选题 |
| 7 | 0.65 | 化学方程式的书写 浓硫酸做干燥剂 | 单选题 |
| 8 | 0.65 | 用质量守恒定律确定物质组成 化学方程式含义 不含杂质的化学方程式计算 金属与盐溶液反应 | 单选题 |
| 9 | 0.65 | 盐类参与的反应 物质推断的综合应用 各类物质间反应的总结 | 单选题 |
| 10 | 0.4 | 不含杂质的化学方程式计算 | 单选题 |
| 二、填空与简答 | |||
| 11 | 0.65 | 复分解反应的定义 化学方程式的书写 化合价代数和的计算与应用 盐类参与的反应 | 流程题 |
| 12 | 0.4 | 化学方程式的书写 设计实验探究物质的成分 | 简答题 |
| 13 | 0.65 | 酸碱溶液导电的原理 中和反应的概念及微观本质 | 填空题 |
| 三、综合应用题 | |||
| 14 | 0.4 | 质量守恒定律的微观解释 中和反应的实际应用 气体制备实验的反应条件的控制 分子动理论(理综) | |
| 四、科学探究题 | |||
| 15 | 0.15 | 碱的通性 盐类参与的反应 设计实验探究物质的成分 实验的设计与评价 | |







