江苏省苏州市昆山市城北中学2020-2021学年九年级下学期3月月考化学试题
江苏
九年级
阶段练习
2021-04-20
392次
整体难度:
适中
考查范围:
身边的化学物质、物质构成的奥秘、化学与社会发展、物质的化学变化、化学实验
一、选择题 添加题型下试题
| A.NaHCO3俗称苏打 | B.Ca(OH)2俗称消石灰 |
| C.Na2CO3俗称火碱 | D.NaOH俗称纯碱 |
【知识点】 常见酸、碱的俗称及化学式解读 常见盐的俗名、用途解读
| A.烧碱作炉具清洁剂 | B.稀盐酸作除锈剂 |
| C.浓硫酸作干燥剂 | D.碳酸钙作补钙剂 |
| A.NH4HCO3 | B.KNO3 | C.Ca(H2PO4)2 | D.KCl |
【知识点】 常见化肥的种类及性质解读 鉴别常见化肥解读
| A.氢氧化铝 | B.氯化钠 | C.碳酸镁 | D.碳酸氢钠 |
| A.HNO3、Na2CO3、KCl | B.H2SO3、NaOH、Na2CO3 |
| C.MgSO4、Mg(OH)2、NaCl | D.Ca(OH)2、HCl、Na2SO4 |
| A.氢氧化钠固体溶于水后溶液温度升高,所以氢氧化钠固体溶于水属于放热反应 |
| B.硝酸铵固体溶于水后溶液随温度降低,所以硝酸铵固体溶于水属于吸热反应 |
| C.生石灰与水反应后溶液温度升高,燃烧放热,酸碱中和反应放热等等,所以化学反应都是放热反应 |
| D.化学变化中都伴随着能量的变化 |
| A.溶液的质量均减小 |
| B.溶液中溶质的质量分数均减小 |
| C.溶质的质量均减小 |
| D.溶剂的质量均增大 |
【知识点】 浓酸敞口放置的变化和现象解读
| 物质 | 厕所清洁剂 | 牙膏 | 肥皂 | 厨房清洁剂 |
| pH | 2 | 8 | 10 | 12 |
上述物质中,最容易直接腐蚀铁制下水管道的是( )
| A.厕所清洁剂 | B.牙膏 | C.肥皂 | D.厨房清洁剂 |
【知识点】 酸的通性解读 溶液酸碱性及pH相关关系解读
| A.二氧化锰 | B.氢氧化钙 | C.氯化钠 | D.硫酸 |
| A.烧碱和纯碱 | B.盐酸和铁粉 |
| C.生石灰和铁粉 | D.熟石灰和金属银 |
【知识点】 保护和利用金属资源的有效途径解读 中和反应的实际应用解读
| A.CO32- | B.Fe3+ |
| C.H+ | D.NO3- |
【知识点】 复分解反应的实质与应用解读 溶液中物质是否共存相关判断解读
| A.Na2CO3溶液 | B.MgCl2溶液 | C.KNO3溶液 | D.酚酞试液 |
| A.滤渣的质量小于加入镁粉的质量 | B.滤渣中一定有镁粉 |
| C.滤液中一定有Mg2+ | D.滤液的颜色为无色 |
【知识点】 金属与盐溶液反应 置换反应中的质量变化解读

| A.转化①的现象是黑色固体逐渐消失,溶液变成蓝色 |
| B.转化②发生的是复分解反应 |
| C.转化③可加入MgCl2溶液实现 |
| D.转化④如果加入Fe,则溶液质量减小 |
| A.Fe→Cu | B.KNO3→NaNO3 | C.Mg→MgO | D.H2SO4→HCl |
| A.小木棍蘸取浓硫酸一段时间后,蘸取部位变黑 |
| B.铁锈放入盛有稀盐酸的试管内,溶液变浅绿色 |
| C.氢氧化钠固体久置于表面皿上,固体表面会变潮湿 |
| D.打开盛放浓盐酸的试剂瓶的瓶盖,可见到瓶口冒白雾 |

| A.若盐为BaCl2溶液,则硫酸与氯化钡溶液反应时有白色沉淀生成 |
| B.若碱为NaOH溶液,可以在NaOH 溶液中滴加酚酞试液,证明硫酸和氢氧化钠溶液发生了中和反应 |
| C.若金属氧化物为铁锈的主要成分( Fe2O3),可以利用硫酸与金属氧化物反应的这一性质除去铁锈 |
| D.若金属为Mg和Zn,将质量相等的两种金属分别与足量的稀硫酸完全反应,产生的H2质量相等 |
| 选项 | 问题 | 分析与设计 |
| A | 为何变质 | 2NaOH + CO2 = Na2CO3 + H2O |
| B | 是否变质 | 取样,加入足量稀盐酸,观察是否产生气泡 |
| C | 是否全部变质 | 取样,加入足量氯化钙溶液,观察产生沉淀多少 |
| D | 如何除去杂质 | 取样,加入适量氢氧化钙溶液,过滤 |
| A.A | B.B | C.C | D.D |
| 序号 | 物质 | 杂质 | 除去杂质的方法 |
| A | NaOH 溶液 | Na2CO3 | 加入适量稀盐酸至不再产生气泡 |
| B | KCl 固体 | MnO2 | 加入足量水,溶解、过滤、洗涤、干燥 |
| C | CaCl2 溶液 | 稀盐酸 | 加入过量碳酸钙粉末,过滤 |
| D | KC1 溶液 | K2SO4 | 加入适量 Ba(NO3)2 溶液,过滤 |
| A.A | B.B | C.C | D.D |
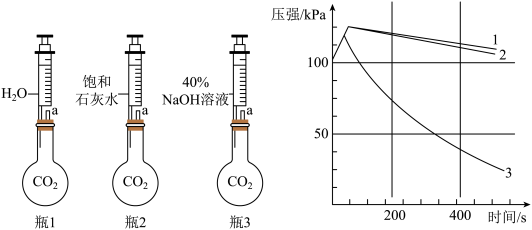
| A.由于注入液体压缩了瓶内的气体,所以三个实验的起始阶段压强都快速增大 |
| B.对比曲线 1 和 2 可知,二氧化碳和水一定发生了化学反应 |
| C.对比曲线 1 和 3 可知,二氧化碳和氢氧化钠一定发生了化学反应 |
| D.对比曲线 2 和 3 可知,40% NaOH 溶液比饱和石灰水更适合吸收二氧化碳 |
【知识点】 二氧化碳与水的反应及实验解读 二氧化碳与碱的反应及实验解读
二、填空与简答 添加题型下试题
(1)某麦片中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的铁元素,反应的化学方程式为
(2)还原铁粉,灰色或黑色粉末,又称“双吸剂”,它能够吸收空气中的
(3)为防止铁生锈,可对铁制品进行“发蓝”处理,使其表面生成致密氧化物保护膜(其中Fe、O元素质量比为21:8),该氧化物的化学式为
(4)我国劳动人民是湿法冶金术的先驱,在世界化学史上占有光辉的一页,湿法炼铜的化学方程式
(5)生铁脆不能锻压,应用程度较为局限:钢制品其有强度高、韧性好、耐高温、耐腐蚀等优良物化应用性能,因此被广泛利用,生铁和钢性能差异较大的原因
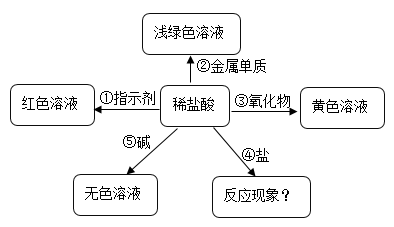
(1)编号①反应的指示剂是
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是
(3)请你写出符合编号③反应的化学方程式
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是
消毒是饮用水处理中的重要环节之一。常用的消毒剂有氯气(Cl2)、二氧化氯(ClO2)等,二氧化氯是世界卫生组织推荐的饮用水消毒剂。
二氧化氯是一种黄绿色、有刺激性气味的气体,极易溶于水,受光照、振动或加热等影响可发生爆炸,但在水溶液中无危险性。自来水厂以亚氯酸钠(NaClO2)和盐酸为原料,用二氧化氯发生器现场制二氧化氯,再投加到水中进行消毒。
研究人员发现:1.0 mg/L氯气与0.5mg/L 二氧化氯的消毒能力相当,氯气和二氧化氯消毒过程中都会产生三氯甲烷(有毒副产物)。某研究小组采集了同一水源的水样,在40℃时,对两种消毒剂的浓度与产生三氯甲烷的浓度关系进行了对比实验。得出的数据如图1和图2所示。

上述实验表明:氯气和二氧化氯在消毒能力相当的情况下,使用二氧化氯做消毒剂比用氯气更安全。通过不断完善制备与应用技术,二氧化氯在净水领域中的作用将越来越大。依据短文内容,回答下列问题。
(1)写出二氧化氯的一条物理性质:
(2)需要现场制二氧化氯的原因是
(3)完成化学反应方程式:5NaClO2+
(4)下列说法正确的是
A. 浓度相同时,氯气和二氧化氯的消毒能力相当
B. 40℃时 4.0 mg/L 的氯气在0~20 h内产生的三氯甲烷明显增多
C. 40℃时0.8 mg/L的二氧化氯在0~20 h内产生的三氯甲烷明显增多
(5)对比图1和图2,找出能说明“氯气和二氧化氯在消毒能力相当的情况下,二氧化氯比氯气更安全”的依据:
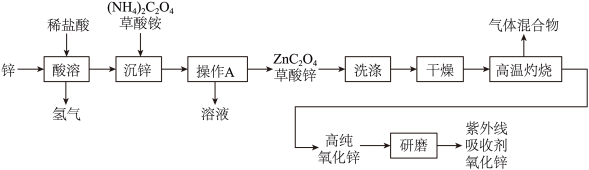
(1)推测草酸的化学式是
(2)“沉锌”过程中发生复分解反应,反应的化学方程式是
(3) “操作A”的名称是
(4)“高温灼烧”时草酸锌分解,反应的化学方程式是
三、科学探究题 添加题型下试题
【查阅资料】碳酸钾与纯碱具有相似的化学性质。
【实验探究】
| 探究过程 | K2CO3 | (NH4)2SO4 | 结论及化学方程式 |
| (1)分别取碳酸钾和硫酸铵固体,加入足量水溶解,分别向两溶液中滴入紫色石蕊试液,观察溶液颜色变化 | 变蓝 | 碳酸钾溶液显 | |
| (2)另取两种溶液分别加入足量 | 产生气泡 | 无明显现象 | 产生气泡的化学方程式 |
| (3)再取两种溶液分别加入Ba(OH)2溶液,观察现象 | 产生白色沉淀 | (NH4)2SO4与Ba(OH)2反应方程式 |
【讨论与反思】
(4)草木灰与硫酸铵能否混合使用?
【拓展与延伸】
(5)某农民家中化肥硫酸铵(NH4)2SO4和尿素CO(NH2)2都是白色固体,易混淆,请你设计一种方案,帮助这位农民加以鉴别(写出操作、现象及结论)
【实验操作】(1)向试管中加入5粒石灰石,倾倒约试管体积1/3的稀盐酸(1:1);观察不到气泡后,仍有固体剩余;将试管静置。
(2)取上层清液,用pH试纸测得溶液pH=2,说明溶液显
pH测定中,“上层清液滴到试纸上”的后一步操作是
【实验思考Ⅰ】反应剩余液中有哪些物质?其中能使溶液pH=2的有哪些?
【实验探究Ⅰ】(1)甲同学通过实验排除了CaCl2的可能性。简述其实验方案
(2)乙同学将CO2通入蒸馏水中至饱和,测得pH>5,。
(3)综合甲、乙两同学实验,得出的结论是:剩余液中还含有
【实验思考Ⅱ】试管中剩余固体是否仍含有CaCO3?
【实验探究Ⅱ】小组同学向试管中继续加入稀盐酸(1:1),又有大量气泡产生。
(1)由此得出的结论是
(2)比较稀盐酸加入前后的实验现象,解释“又有大量气泡产生”的原因:
【拓展延伸】(1)反应剩余液放置一段时间后,溶液pH增大,其主要原因是
(2)假如用100g14.6%的稀盐酸和足量的石灰石反应,看不到气泡产生时,停止收集气体。收集到的CO2质量
【查阅资料】
Ⅰ.20℃时,几种物质在水中的溶解度见下表:
| 物质 | Na2CO3 | NaHCO3 | Ca(OH)2 | Ba(OH)2 |
| 溶解度/g | 21.5 | 9.6 | 0.165 | 3.89 |
【实验探究】
(1)实验一:小雨取一充满CO2的矿泉水瓶,加入一定量的水,立即拧紧瓶盖,振荡,发现瓶子变瘪,小雨另取一相同的充满CO2的矿泉水瓶,向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X,此时观察到的现象是
(2)实验二:为检验CO2与NaOH溶液反应的产物,小亮取实验一所得溶液X少许,向其中滴加BaCl2溶液,有白色沉淀产生,该反应的化学方程式为
(3)实验三:小华取实验一所得溶液X少许,向其中加入过量的BaCl2溶液,振荡,静置,取上层清液,滴入1滴酚酞试液,发现溶液呈
(4)实验四:兴趣小组将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中溶液的pH和温度变化,结果如图1、图2所示。
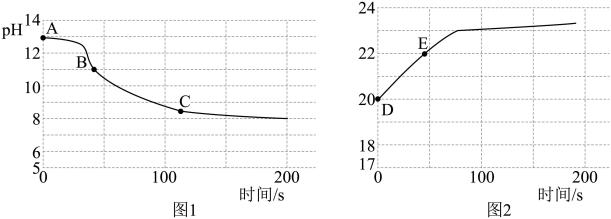
图1中,BC段发生反应的化学方程式为
图2中,DE段温度变化的原因是
【反思感悟】
(5)实验从CO2减少、NaOH减少,Na2CO3生成等物质的变化,以及
四、综合应用题 添加题型下试题

请根据图回答:
(1)向锥形瓶中缓慢滴入稀盐酸,能说明稀盐酸与氢氧化钠溶液发生化学反应的现象是
(2)当两者恰好完全反应时,溶液的pH位于曲线的
(3)下列说法是同学们在分析实验数据时得出的结论,你认为正确的是
A.实验过程中氢氧化钠的质量不断变小直至为0
B.实验过程中使用磁力搅拌器的目的是吸收热量
C.实验过程中氯化钠的质量分数一直在不断增大
D.实验过程中也可以选用pH试纸验证反应的发生
(4)兴趣小组同学对实验中使用的标有质量分数为16%的盐酸(图3)的实际质量分数产生质疑,为了测定,小明配制了20%的氢氧化钠溶液100g,然后在烧杯中加入一定量配得的氢氧化钠溶液,再逐滴加入该盐酸,恰好完全反应时测得剩余物总量为45g,整个实验过程用pH测定仪测定滴加过程中溶液的pH,图4为测定仪打印出的滴加盐酸的质量与溶液pH的关系图。请以此次测定的数据,列式计算该盐酸的实际质量分数?(请写出详细的计算过程)

(5)该盐酸的实际质量分数与标签上标出的质量分数不一致的可能原因
【知识点】 中和反应相关实验与计算解读 无明显现象的中和反应的判断解读
试卷分析
试卷题型(共 28题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 常见酸、碱的俗称及化学式 常见盐的俗名、用途 | 单选题 |
| 2 | 0.85 | 常见几种酸的用途 几种常见碱的物理性质及用途 常见盐的俗名、用途 | 单选题 |
| 3 | 0.65 | 常见化肥的种类及性质 鉴别常见化肥 | 单选题 |
| 4 | 0.85 | 酸的通性 中和反应的实际应用 碳酸氢钠、碳酸钠、碳酸钙 | 单选题 |
| 5 | 0.65 | 酸的定义 碱的定义 盐的定义 | 单选题 |
| 6 | 0.85 | 溶解时能量的变化 中和反应过程中能量的变化 能量转化与化学变化的关系 | 单选题 |
| 7 | 0.85 | 浓酸敞口放置的变化和现象 | 单选题 |
| 8 | 0.65 | 酸的通性 溶液酸碱性及pH相关关系 | 单选题 |
| 9 | 0.65 | 过氧化氢制取氧气实验 酸的通性 碱的通性 氯化钠 | 单选题 |
| 10 | 0.65 | 保护和利用金属资源的有效途径 中和反应的实际应用 | 单选题 |
| 11 | 0.85 | 复分解反应的实质与应用 溶液中物质是否共存相关判断 | 单选题 |
| 12 | 0.65 | 复分解反应的实质与应用 常见的酸碱指示剂及其变色情况 盐类参与的反应 物质鉴别——选用试剂鉴别 | 单选题 |
| 13 | 0.4 | 金属与盐溶液反应 置换反应中的质量变化 | 单选题 |
| 14 | 0.65 | 复分解反应的定义 复分解反应发生的条件 根据化学方程式计算质量比 酸的通性 | 单选题 |
| 15 | 0.65 | 复分解反应发生的条件 金属与氧气反应 金属与盐溶液反应 盐类参与的反应 | 单选题 |
| 16 | 0.85 | 浓硫酸的物理、化学性质 盐酸的物理性质 酸的通性 强碱露置在空气中的变质 | 单选题 |
| 17 | 0.65 | 酸不足--金属性质的计算 酸的通性 无明显现象的中和反应的判断 盐类参与的反应 | 单选题 |
| 18 | 0.65 | 强碱露置在空气中的变质 盐类参与的反应 碳酸根离子的验证 | 单选题 |
| 19 | 0.65 | 酸的通性 盐类参与的反应 除杂 | 单选题 |
| 20 | 0.4 | 二氧化碳与水的反应及实验 二氧化碳与碱的反应及实验 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.65 | 常见合金 金属与酸反应原理 金属的防锈措施 | 填空题 |
| 22 | 0.65 | 金属与酸反应原理 酸的通性 盐类参与的反应 | 填空题 |
| 23 | 0.4 | 化学性质和物理性质 根据方程式推测化学式 自来水厂净化过程 | 科普阅读题 |
| 24 | 0.65 | 化学方程式的书写 酸的概念、组成 盐类参与的反应 过滤 | 流程题 |
| 三、科学探究题 | |||
| 25 | 0.65 | 常见的酸碱指示剂及其变色情况 盐类参与的反应 常见化肥的种类及性质 鉴别常见化肥 | |
| 26 | 0.4 | 溶液酸碱性及pH相关关系 碳酸根离子的验证 设计实验探究物质的成分 | |
| 27 | 0.65 | 二氧化碳与碱的反应及实验 常见的酸碱指示剂及其变色情况 碳酸根离子的验证 化学反应中能量变化的实际应用 | |
| 四、综合应用题 | |||
| 28 | 0.4 | 中和反应相关实验与计算 无明显现象的中和反应的判断 | |



