为了测定大理石样品中钙元素的质量分数(杂质不含钙元素,不溶于水,也不与其他物质发生反应),进行了如下实验。请回答下列问题。
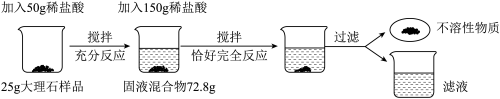
(1)上述实验过程中发生反应的化学方程式为____________________ 。
(2)根据已知条件列出求解第一次所加的稀盐酸中溶质的质量(x)的比例式__________________ 。
(3)此大理石样品中钙元素的质量分数__________________ 。
(4)用36.5%的浓盐酸配制200g上述稀盐酸,所需盐酸的质量为__________________ 。
(5)若将反应后的滤液蒸发11.2g水,无晶体析出,所得溶液中溶质的质量分数为______________ 。
(6)现有上述大理石样品500t,可以制得含杂质的生石灰的质量为__________________ 。

(1)上述实验过程中发生反应的化学方程式为
(2)根据已知条件列出求解第一次所加的稀盐酸中溶质的质量(x)的比例式
(3)此大理石样品中钙元素的质量分数
(4)用36.5%的浓盐酸配制200g上述稀盐酸,所需盐酸的质量为
(5)若将反应后的滤液蒸发11.2g水,无晶体析出,所得溶液中溶质的质量分数为
(6)现有上述大理石样品500t,可以制得含杂质的生石灰的质量为
19-20九年级下·黑龙江哈尔滨·阶段练习 查看更多[4]
(已下线)6.2 溶液的组成 (拓展培优)-2022-2023学年九年级化学下册课后培优分级练(沪教版)黑龙江省哈尔滨市宾县2020-2021学年九年级上学期期末化学试题2020年黑龙江省哈尔滨市南岗区中考二模化学试题黑龙江省哈尔滨市南岗区第十七中学2019-2020学年九年级下学期3月月考化学试题
更新时间:2020-04-20 21:18:12
|
相似题推荐
计算题
|
困难
(0.15)
真题
【推荐1】实验室有一瓶硫酸铵(含杂质氯化镁)样品。化学兴趣小组的同学为了测定该样品中氯化镁的含量,取该样品17.95g全部溶于152.35g水中,向所得溶液中滴加溶质质量分数为10%的氢氧化钠溶液,实验数据如表所示:
求:
(1)表中m的值为___________。
(2)该样品中氯化镁的质量分数(写出计算过程,结果精确到0.1%)。
(3)当恰好完全反应时所得溶液中硫酸钠的质量分数(写出计算过程)。
| 时间/s | 30 | 60 | 90 | 120 | 150 |
| 产生沉淀的质量/g | 0.725 | m | 2.175 | 2.9 | 2.9 |
求:
(1)表中m的值为___________。
(2)该样品中氯化镁的质量分数(写出计算过程,结果精确到0.1%)。
(3)当恰好完全反应时所得溶液中硫酸钠的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
困难
(0.15)
名校
【推荐2】某实验小组用石灰石样品与相同浓度的稀盐酸反应,将三次实验所得的相关数据记录如下:(杂质不溶于水也不与稀盐酸反应)
请根据上表数据计算:(结果保留一位小数)
(1)石灰石样品中碳酸钙的质量分数;
(2)第 3 次反应后所得溶液中溶质的质量分数。
| 物质质量 | 第1次 | 第2次 | 第3次 |
| 石灰石样品的质量/g | 15 | 15 | 25 |
| 所用稀盐酸的质量/g | 100 | 120 | 100 |
| 充分反应后,剩余物总质量/g | 110.6 | 130.6 | 120.6 |
请根据上表数据计算:(结果保留一位小数)
(1)石灰石样品中碳酸钙的质量分数;
(2)第 3 次反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
困难
(0.15)
解题方法
【推荐3】鸡蛋壳的主要成分是碳酸钙(其它成分不溶于水也不与酸反应)。化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做如下实验:

反应①结束后,所加盐酸刚好反应了一半,反应②恰好完全反应。请回答下列问题(可以选下列任意两个问题回答,并写出计算过程):
(1)反应①产生的CO2的质量为___________________ ;
(2)该鸡蛋壳中碳酸钙的质量分数为________________ ;
(3)所加氢氧化钙的质量为__________________ ;
(4)溶液b中溶质的质量分数为_________________ ;
计算过程:

反应①结束后,所加盐酸刚好反应了一半,反应②恰好完全反应。请回答下列问题(可以选下列任意两个问题回答,并写出计算过程):
(1)反应①产生的CO2的质量为
(2)该鸡蛋壳中碳酸钙的质量分数为
(3)所加氢氧化钙的质量为
(4)溶液b中溶质的质量分数为
计算过程:
您最近一年使用:0次
计算题
|
困难
(0.15)
真题
名校
【推荐1】一些骗子常用黄铜冒充黄金骗取钱财,某同学通过查阅资料得知黄铜是锌和铜的合金,他取一定量的某黄铜样品放入烧杯中,再向其中分4次加入等质量的同一稀硫酸,每次均充分反应。实验过程中有关物质的用量及质量测定记录如下表:
分析表中数据,完成下列问题:
(1)所取黄铜样品的质量为___________ g;
(2)第4次实验结束后溶液的pH __________7(填“>”、“=”或“<”);
(3)所用稀硫酸中溶质的质量分数为?(要求有解答过程)
| 实验次数 | 1 | 2 | 3 | 4 |
| 稀硫酸的用量/g | 20 | 20 | 20 | 20 |
| 剩余固体的质量 | 10 | 8.7 | 7.4 | 7.2 |
分析表中数据,完成下列问题:
(1)所取黄铜样品的质量为___________ g;
(2)第4次实验结束后溶液的pH __________7(填“>”、“=”或“<”);
(3)所用稀硫酸中溶质的质量分数为?(要求有解答过程)
您最近一年使用:0次
计算题
|
困难
(0.15)
解题方法
【推荐2】鸡蛋壳的主要成分是碳酸钙(其它成分不溶于水也不与酸反应)。化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做如下实验:

反应①结束后,所加盐酸刚好反应了一半,反应②恰好完全反应。请回答下列问题(可以选下列任意两个问题回答,并写出计算过程):
(1)反应①产生的CO2的质量为___________________ ;
(2)该鸡蛋壳中碳酸钙的质量分数为________________ ;
(3)所加氢氧化钙的质量为__________________ ;
(4)溶液b中溶质的质量分数为_________________ ;
计算过程:

反应①结束后,所加盐酸刚好反应了一半,反应②恰好完全反应。请回答下列问题(可以选下列任意两个问题回答,并写出计算过程):
(1)反应①产生的CO2的质量为
(2)该鸡蛋壳中碳酸钙的质量分数为
(3)所加氢氧化钙的质量为
(4)溶液b中溶质的质量分数为
计算过程:
您最近一年使用:0次
计算题
|
困难
(0.15)
真题
解题方法
【推荐1】菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究。取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如下表:
说明:菱镁矿中的杂质不溶于水,不与酸发生反应。.
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为 。
(2)计算该菱镁矿中镁元素的质量分数。(写出计算过程)

(3)该实验研究中所用H2SO4溶液的溶质的质量分数是 。
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了l.71%的Ba(OH)2溶液。请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图。(在答题卡的坐标中作图,并标出曲线折点的坐标)
| 加入H2S04溶液的质量/g | 50 | 100 | 150 | 200 |
| NaOH溶液增加的质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为 。
(2)计算该菱镁矿中镁元素的质量分数。(写出计算过程)

(3)该实验研究中所用H2SO4溶液的溶质的质量分数是 。
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了l.71%的Ba(OH)2溶液。请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图。(在答题卡的坐标中作图,并标出曲线折点的坐标)
您最近一年使用:0次
【推荐2】某同学在实验室用石灰石(杂质不含钙元素,不溶于水与酸反应)和稀盐酸制取二氧化碳气体。回答下列问题:

(1)上述实验过程中发生反应的化学方程式为___________ ;
(2)产生二氧化碳的质量为___________ g;
(3)根据生成二氧化碳的质量列出求解参加反应的碳酸钙质量(x)的比例式___________ ;
(4)此石灰石样品中碳酸钙的含量为___________ ;
(5)向反应后的滤液中加入332.8g水,计算最终所得溶液溶质质量分数,并填写在B图的标签上(标签样式如图);

(6)若配制100g上述稀盐酸,需质量分数36.5%的浓盐酸与水的质量比为___________ ;
(7)某工厂要用该石灰石制取生石灰,若要制得含杂质5%的生石灰112t,假设在煅烧的过程中有5%的原料损失,则需要上述石灰石的质量为___________ 。

(1)上述实验过程中发生反应的化学方程式为
(2)产生二氧化碳的质量为
(3)根据生成二氧化碳的质量列出求解参加反应的碳酸钙质量(x)的比例式
(4)此石灰石样品中碳酸钙的含量为
(5)向反应后的滤液中加入332.8g水,计算最终所得溶液溶质质量分数,并填写在B图的标签上(标签样式如图);

(6)若配制100g上述稀盐酸,需质量分数36.5%的浓盐酸与水的质量比为
(7)某工厂要用该石灰石制取生石灰,若要制得含杂质5%的生石灰112t,假设在煅烧的过程中有5%的原料损失,则需要上述石灰石的质量为
您最近一年使用:0次
计算题
|
困难
(0.15)
名校
解题方法
【推荐3】在化学实验室,小建同学发现用石灰石和稀盐酸制取二氧化碳的锥形瓶中有残留的白色固体,成分为未反应的碳酸钙、杂质(不溶于水也不参与反应)和氯化钙的混合物。小设同学想测定石灰石中碳酸钙的含量并配制一种溶液,实验及数据如下(实验中所得的溶液都为不饱和溶液):

(1)请写出发生反应的化学方程式;
(2)利用已知条件列出与5g碳酸钙反应的物质质量(x)的比例式;
(3)石灰石中碳酸钙的含量是多少?
(4)实验所用稀盐酸中溶质的质量分数是多少?
(5)若将滤液A蒸发16.7g水后,所得溶液的溶质质量分数是多少?
(6)配制上述实验所用稀盐酸,需要36.5%的浓盐酸与水的质量比是多少?

(1)请写出发生反应的化学方程式;
(2)利用已知条件列出与5g碳酸钙反应的物质质量(x)的比例式;
(3)石灰石中碳酸钙的含量是多少?
(4)实验所用稀盐酸中溶质的质量分数是多少?
(5)若将滤液A蒸发16.7g水后,所得溶液的溶质质量分数是多少?
(6)配制上述实验所用稀盐酸,需要36.5%的浓盐酸与水的质量比是多少?
您最近一年使用:0次
计算题
|
困难
(0.15)
真题
【推荐1】某钢铁厂实验室为测定赤铁矿中Fe2O3的含量,将矿石粉碎(其中杂质既不溶于水也不与酸反应),进行如下实验:

请回答下列问题:
(1)上述实验过程中发生反应的化学方程式为______________________________;
(2)样品中Fe2O3的质量分数是_______;
(3)根据已知条件列出求解200g稀硫酸中溶质质量(x)的比例式___________________;
(4)若向最终滤液中加入16g水,所得不饱和溶液中溶质的质量分数为_________;
(5)该钢铁厂每天用上述赤铁矿石1900t来生产生铁。则理论上日产含杂质5%的生铁的质量为_________。

请回答下列问题:
(1)上述实验过程中发生反应的化学方程式为______________________________;
(2)样品中Fe2O3的质量分数是_______;
(3)根据已知条件列出求解200g稀硫酸中溶质质量(x)的比例式___________________;
(4)若向最终滤液中加入16g水,所得不饱和溶液中溶质的质量分数为_________;
(5)该钢铁厂每天用上述赤铁矿石1900t来生产生铁。则理论上日产含杂质5%的生铁的质量为_________。
您最近一年使用:0次
计算题
|
困难
(0.15)
解题方法
【推荐2】为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),称取40g石灰石样品等分为4份(分别编号为①②③④),每份样品分别与一定量的稀盐酸反应,所得数据如下表所示:
然后,为了探究石灰石与稀盐酸反应后所得废液中的溶质成分,将编号③所得废液过滤,取滤液质量的 于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示。分析题中有关信息和图象,回答下列问题:
于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示。分析题中有关信息和图象,回答下列问题:

(1)石灰石样品的纯度为_____;
(2)图象中5﹣25阶段发生的反应方程式是_____;
(3)编号③所用稀盐酸的质量m为_____g (要写计算过程)。
| 样品编号 | ① | ② | ③ | ④ |
| 稀盐酸的质量 | 20g | 40g | m(80<m<130)g | 130g |
| 剩余固体的质量 | 8g | 6g | 2g | 2g |
 于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示。分析题中有关信息和图象,回答下列问题:
于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示。分析题中有关信息和图象,回答下列问题:
(1)石灰石样品的纯度为_____;
(2)图象中5﹣25阶段发生的反应方程式是_____;
(3)编号③所用稀盐酸的质量m为_____g (要写计算过程)。
您最近一年使用:0次
计算题
|
困难
(0.15)
名校
解题方法
【推荐3】下图烧杯中装有100g稀盐酸和氯化镁的混合溶液,向该溶液中加入10%的氢氧化钠溶液至恰好完全反应时,生成沉淀2.9g。请回答:

(1)写出实验中产生沉淀的化学方程式_______________。
(2)列出求解原混合溶液中含有氯化镁质量(x)的比例式_______________。
(3)第一次实验后所得溶液中溶质的化学式为_______________。
(4)该混合溶液中氯化氢和氯化镁的质量比为_______________。
(5)向过滤后所得溶液中加入82. 9g水后,所得溶液中溶质质量分数为_______________。

(1)写出实验中产生沉淀的化学方程式_______________。
(2)列出求解原混合溶液中含有氯化镁质量(x)的比例式_______________。
(3)第一次实验后所得溶液中溶质的化学式为_______________。
(4)该混合溶液中氯化氢和氯化镁的质量比为_______________。
(5)向过滤后所得溶液中加入82. 9g水后,所得溶液中溶质质量分数为_______________。
您最近一年使用:0次



