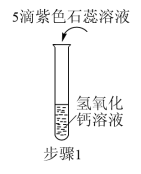
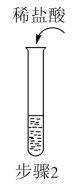
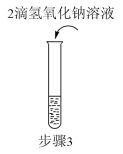
归纳总结是学习知识的重要方法。小军同学用图1总结了NaOH的四条化学性质。
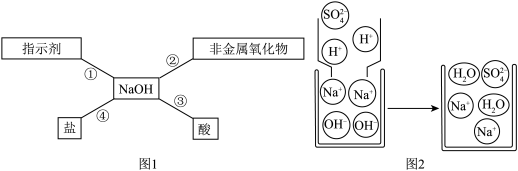
(1)验证反应①:将紫色石蕊溶液滴入NaOH溶液中,溶液会变成_________ 色。
(2)图2利用微观示意图来说明反应③的发生,请写出该反应的化学方程式:_______ ;从该图还可以看出,反应后的溶液pH_________ 7(填“>”、“=”或“<”)。
(3)如果反应④能够发生,你选择的物质是________ (填序号)。
A HCl B Na2CO3 C CuSO4
(4)另外,NaOH溶液还能与某些金属(如Al)发生反应。请配平该反应的化学方程式:_____ NaOH + _____ H2O + _____ Al= _____ NaAlO2 + _____ H2↑。

(1)验证反应①:将紫色石蕊溶液滴入NaOH溶液中,溶液会变成
(2)图2利用微观示意图来说明反应③的发生,请写出该反应的化学方程式:
(3)如果反应④能够发生,你选择的物质是
A HCl B Na2CO3 C CuSO4
(4)另外,NaOH溶液还能与某些金属(如Al)发生反应。请配平该反应的化学方程式:
更新时间:2020-04-23 10:46:36
|
相似题推荐
【推荐1】鉴别两瓶无色透明的液体。已知一瓶是稀盐酸,一瓶是氢氧化钙溶液(采用两种不同类型的化学方法)。
| 实验步骤 | 现象和结论 | |
| 方法1 | 分别取样: | |
| 方法2 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】为探究酸的性质,同学们设计了如下实验,请你参与。

(1)检验物质。按图1实验,可确定X是盐酸,则Y可以是___________ (选填“酚酞溶液”或“紫色石蕊溶液”)。盐酸与AgNO3溶液反应的实验现象是___________ 。
(2)确定溶质成分。由图2实验,A中固体全部溶解,B中有白色沉淀产生,得出结论:A中溶质只有硫酸铁。有同学认为该结论不合理。接着向试管B中滴加氢氧化钠溶液,且产生沉淀的最随氢氧化钠溶液量的关系如图3所示。则A中溶质有___________ 。实验中,A中发生反应的化学方程式为___________ c点对应溶液中含有溶质可能的组成有___________ 种。
(3)由以上实验总结酸的化学性质有___________ ;
①能使酸碱指示剂变色②能与活泼金属反应③能与某些金属氧化物反应④能与碱反应⑤能与某些盐反应

(1)检验物质。按图1实验,可确定X是盐酸,则Y可以是
(2)确定溶质成分。由图2实验,A中固体全部溶解,B中有白色沉淀产生,得出结论:A中溶质只有硫酸铁。有同学认为该结论不合理。接着向试管B中滴加氢氧化钠溶液,且产生沉淀的最随氢氧化钠溶液量的关系如图3所示。则A中溶质有
(3)由以上实验总结酸的化学性质有
①能使酸碱指示剂变色②能与活泼金属反应③能与某些金属氧化物反应④能与碱反应⑤能与某些盐反应
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
【推荐3】酸菜,古称菹(zū),《周礼》中就有其大名。据东汉许慎《说文解字》解释:“菹菜者,酸菜也”。由此可见,中国酸菜的历史颇为悠久。酸菜可分为东北酸菜、四川酸菜等,不同地区的酸菜原料不同,口味风格也不同。北方酸菜多以白菜为原料,称作酸白菜。酸白菜是大白菜在一定条件下由乳酸菌发酵而成的, 发酵时产生大量的有机酸而具有酸味。实验证明,发酵时,蔬菜中含有的硝酸盐会被还原成亚硝酸盐,而亚硝酸盐又与癌症细胞诱导物有关, 因此, 发酵蔬菜的安全性引起了很多人的关注。酸白菜腌制中亚硝酸盐的消长规律是怎样的呢?本研究通过实验观察酸白菜腌制中亚硝酸盐的动态变化, 指导人们食用时避开“亚硝峰” , 对保障健康具有重要意义。
实验材料:大白菜和食盐。大白菜选用地产优质大白菜。食盐选用市售加碘食盐,其中NaCl%≥98.5%。
腌制方法:传统腌制方法,按3%、5%、7%、9%的预设食盐浓度添加食盐。腌制温度:室温,温度范围在10~25oC之间。
主要方法:实验过程中定期从不同的容器中取样进行产酸量和亚硝酸盐含量的测定。
(1)用酸度计测定用不同浓度食盐腌制过程中产酸量(用%表示)的变化。实验结果如图1所示:
(2)测定用不同浓度食盐腌制过程中亚硝酸盐含量的变化。实验结果如图2、图3所示。

结果分析:腌菜中亚硝酸盐的形成主要与细菌的还原作用有关, 具有硝酸还原酶的细菌是使蔬菜产生大量亚硝酸盐的一个决定性因素。腌菜的发酵过程主要是有益微生物—乳酸菌进行乳酸发酵的结果,从乳酸菌的生化特性看,几乎所有乳酸菌(个别种类如植物乳杆菌在pH6.0以上有些菌株有还原硝酸盐的能力)都不能使硝酸盐还原成亚硝酸盐, 因为它们不具备细胞色素氧化酶系统,乳酸菌大多也不具备氨基酸脱羧酶, 因而也不产生氨, 所以, 纯培养条件下是不会产生亚硝酸盐和亚硝胺的,因此, 我国传统的调味副食品—腌菜, 极具生存与发展的活力。传统方法制作酸白菜, 是由白菜自然带入的乳酸菌经发酵而成的,白菜中既附有乳酸菌,也有一些有害菌, 如大肠杆菌、金黄色葡萄球菌等, 它们能使硝酸盐还原成亚硝酸盐, 腌制初期, 乳酸菌迅速繁殖, 有害菌的生长也相应增强, 随着乳酸发酵的旺盛进行, 酸度加大。有害菌的生长就逐渐受到抑制, 硝酸还原能力减弱,已生成的亚硝酸盐则继续被还原或被分解、破坏, 使亚硝酸盐的含量逐渐下降。“亚硝峰”消失的原因:(1)是酸性条件下的化学降解;(2)是乳酸菌本身对亚硝酸盐的还原作用, 低pH是促使亚硝酸盐降解的主要原因。
回答下列问题:
(1)检测酸白菜腌渍液酸碱性可采取的方法是__________ 。
(2)实验所用的食盐中含钠元素质量分数是_________ (写计算式)。
(3)从实验结果分析,食盐溶液的浓度与白菜发酵过程中产酸量的关系是__________ 。
(4)根据实验结果,你给腌制或食用酸白菜提出的合理化建议是__________ ,理由是___________ 。
实验材料:大白菜和食盐。大白菜选用地产优质大白菜。食盐选用市售加碘食盐,其中NaCl%≥98.5%。
腌制方法:传统腌制方法,按3%、5%、7%、9%的预设食盐浓度添加食盐。腌制温度:室温,温度范围在10~25oC之间。
主要方法:实验过程中定期从不同的容器中取样进行产酸量和亚硝酸盐含量的测定。
(1)用酸度计测定用不同浓度食盐腌制过程中产酸量(用%表示)的变化。实验结果如图1所示:
(2)测定用不同浓度食盐腌制过程中亚硝酸盐含量的变化。实验结果如图2、图3所示。

结果分析:腌菜中亚硝酸盐的形成主要与细菌的还原作用有关, 具有硝酸还原酶的细菌是使蔬菜产生大量亚硝酸盐的一个决定性因素。腌菜的发酵过程主要是有益微生物—乳酸菌进行乳酸发酵的结果,从乳酸菌的生化特性看,几乎所有乳酸菌(个别种类如植物乳杆菌在pH6.0以上有些菌株有还原硝酸盐的能力)都不能使硝酸盐还原成亚硝酸盐, 因为它们不具备细胞色素氧化酶系统,乳酸菌大多也不具备氨基酸脱羧酶, 因而也不产生氨, 所以, 纯培养条件下是不会产生亚硝酸盐和亚硝胺的,因此, 我国传统的调味副食品—腌菜, 极具生存与发展的活力。传统方法制作酸白菜, 是由白菜自然带入的乳酸菌经发酵而成的,白菜中既附有乳酸菌,也有一些有害菌, 如大肠杆菌、金黄色葡萄球菌等, 它们能使硝酸盐还原成亚硝酸盐, 腌制初期, 乳酸菌迅速繁殖, 有害菌的生长也相应增强, 随着乳酸发酵的旺盛进行, 酸度加大。有害菌的生长就逐渐受到抑制, 硝酸还原能力减弱,已生成的亚硝酸盐则继续被还原或被分解、破坏, 使亚硝酸盐的含量逐渐下降。“亚硝峰”消失的原因:(1)是酸性条件下的化学降解;(2)是乳酸菌本身对亚硝酸盐的还原作用, 低pH是促使亚硝酸盐降解的主要原因。
回答下列问题:
(1)检测酸白菜腌渍液酸碱性可采取的方法是
(2)实验所用的食盐中含钠元素质量分数是
(3)从实验结果分析,食盐溶液的浓度与白菜发酵过程中产酸量的关系是
(4)根据实验结果,你给腌制或食用酸白菜提出的合理化建议是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐1】“宏观—微观—符号”三重表征是化学独特的表示物质及其变化的方式。请结合图示回答下列问题:
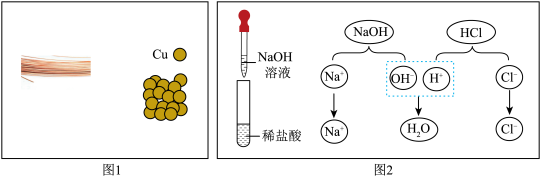
(1)图1 中,“Cu”表示多种信息,如表示铜元素、铜单质,还能表示________ 。
(2)从微粒的角度说明图2反应的实质是_______________ .
(3)图3 为物质甲发生分解反应的微观示意图。

①物质甲中氧元素的化合价为_________ ;
②写出反应的化学方程式_______________________________ 。

(1)图1 中,“Cu”表示多种信息,如表示铜元素、铜单质,还能表示
(2)从微粒的角度说明图2反应的实质是
(3)图3 为物质甲发生分解反应的微观示意图。

①物质甲中氧元素的化合价为
②写出反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】归纳总结是学习化学的重要方法,小明同学用思维导图的形式总结了NaOH的四条化学性质如图甲(即NaOH与四类物质能够发生化学反应)。请回答:

(1)反应①中若把酚酞溶液滴加到氢氧化钠溶液中,观察到的现象是_______ 。
(2)写出一个符合反应②的化学方程式_______ ;小红同学将某稀酸溶液逐滴滴入一定量的稀氢氧化钠溶液中,用温度传感器对反应过程中溶液的温度进行实时测定,得到的曲线如图乙,根据图像可以得出该反应是_______ (填“吸热”或“放热”)反应。
(3)反应③可以选用的盐是

(1)反应①中若把酚酞溶液滴加到氢氧化钠溶液中,观察到的现象是
(2)写出一个符合反应②的化学方程式
(3)反应③可以选用的盐是
| A.NaNO3 | B.CuSO4 | C.NH4NO3 | D.KNO3 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】构建知识网络,可以帮助我们理解知识间的内在联系,如图是氢氧化钠与不同类别物质之间反应的知识网络。

(1)用氢氧化钠溶液吸收SO2的化学方程式___________ 。
(2)氢氧化钠能与酸发生中和反应,中和反应的实质是___________ 。
(3)图中M应为盐类物质,写出其中一个蓝色沉淀生成的反应的化学方程式___________ 。
(4)现有一瓶长期露置于空气中的氢氧化钠溶液。
①小丽同学用实验方法证明该瓶氧氧化钠溶液已变质,可选择下列试剂中的___________ (填字母序号)。
A.酚酞溶液 B.稀盐酸 C.石灰水 D.食盐水 E.氯化钙溶液
②小明要除去氢氧化钠溶液中的Na2CO3,可选用上述试剂___________ 。(填字母序号)

(1)用氢氧化钠溶液吸收SO2的化学方程式
(2)氢氧化钠能与酸发生中和反应,中和反应的实质是
(3)图中M应为盐类物质,写出其中一个蓝色沉淀生成的反应的化学方程式
(4)现有一瓶长期露置于空气中的氢氧化钠溶液。
①小丽同学用实验方法证明该瓶氧氧化钠溶液已变质,可选择下列试剂中的
A.酚酞溶液 B.稀盐酸 C.石灰水 D.食盐水 E.氯化钙溶液
②小明要除去氢氧化钠溶液中的Na2CO3,可选用上述试剂
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】实验小组用pH传感器探究稀盐酸和氢氧化钠溶液的反应。实验操作和测定结果如图所示:

(1)盐酸和氢氧化钠反应的化学方程式为_______ 。
(2)该实验中,乙溶液是_______ 。
(3)能说明盐酸与氢氧化钠发生化学反应的依据是_______ 。

(1)盐酸和氢氧化钠反应的化学方程式为
(2)该实验中,乙溶液是
(3)能说明盐酸与氢氧化钠发生化学反应的依据是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
名校
【推荐2】酸、碱、盐在生产、生活中有广泛的应用。
(1)氢氧化钠溶液与稀硫酸反应时,溶液pH值变化如图所示。
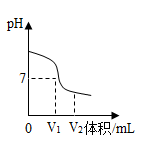
①根据图示判断该实验是将______ 滴入到______ 中。
②滴入溶液体积为V2mL时,溶液中溶质为______ (填化学式)。
(2)测定某酸溶液pH时,如果放pH试纸的玻璃片上的水没有擦干就进行测定,会使测得的pH______ (填“偏大”或“偏小”)
(3)用来改良酸性土壤的碱是______ 。
(1)氢氧化钠溶液与稀硫酸反应时,溶液pH值变化如图所示。

①根据图示判断该实验是将
②滴入溶液体积为V2mL时,溶液中溶质为
(2)测定某酸溶液pH时,如果放pH试纸的玻璃片上的水没有擦干就进行测定,会使测得的pH
(3)用来改良酸性土壤的碱是
您最近一年使用:0次