(1)自然界中吸收大气中CO2的最重要环节是_____ .
(2)科学家研究得到:海洋是吸收大量CO2的地方.如果CO2排放量继续增加,海洋将被“酸化”.请写出海洋酸化原因的化学方程式________ .
(3)科学家目前正在研究将空气中过量的CO2和H2在催化剂和适量条件下转化成液态甲醇和水,反应的化学方程式:CO2+3H2 甲醇+H2O.则甲醇的化学式是
甲醇+H2O.则甲醇的化学式是______ .
(4)已知20℃时,KCl的溶解度为34克,50℃时的溶解度为42.6克.通过以下实验操作得到溶液①至⑤:
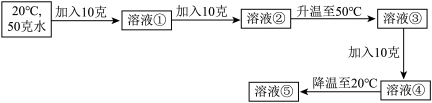
Ⅰ、上述实验所得溶液中,属于饱和溶液的是____ ;
Ⅱ、溶液④的质量为____ 克;
Ⅲ、溶液⑤中,溶质的质量分数为_____ .
(2)科学家研究得到:海洋是吸收大量CO2的地方.如果CO2排放量继续增加,海洋将被“酸化”.请写出海洋酸化原因的化学方程式
(3)科学家目前正在研究将空气中过量的CO2和H2在催化剂和适量条件下转化成液态甲醇和水,反应的化学方程式:CO2+3H2
 甲醇+H2O.则甲醇的化学式是
甲醇+H2O.则甲醇的化学式是(4)已知20℃时,KCl的溶解度为34克,50℃时的溶解度为42.6克.通过以下实验操作得到溶液①至⑤:

Ⅰ、上述实验所得溶液中,属于饱和溶液的是
Ⅱ、溶液④的质量为
Ⅲ、溶液⑤中,溶质的质量分数为
更新时间:2020-04-24 14:13:27
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】请写出下列反应的化学方程式:
(1)反应后生成黑色固体的化合反应_______
(2)硫在氧气中燃烧_______
(3)氧化汞加热分解_______
(4)水在通电条件分解:________
(5)硫酸铜溶液和氢氧化钠溶液反应生成氢氧化铜和硫酸钠______
(1)反应后生成黑色固体的化合反应
(2)硫在氧气中燃烧
(3)氧化汞加热分解
(4)水在通电条件分解:
(5)硫酸铜溶液和氢氧化钠溶液反应生成氢氧化铜和硫酸钠
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】请按要求填空:
(1)下面各项都有数字2,写出它们所代表意义:
①2Al____________________________ ;
②2Cl-___________________________ ;
③2C60___________________________ ;
④Fe2+____________________________ ;
⑤
___________________________ 。
(2)某化学反应的微粒示意图是:

该反应的化学方程式为_____________________________________ ,
所属基本反应类型为______________________ 。
(1)下面各项都有数字2,写出它们所代表意义:
①2Al
②2Cl-
③2C60
④Fe2+
⑤

(2)某化学反应的微粒示意图是:

该反应的化学方程式为
所属基本反应类型为
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】阅读下面科技短文,回答问题。
随着人类社会的发展,化石燃料的消耗量急剧增加,释放的CO2越来越多。从而导致温室效应增强,全球气候变暖。科学家一直致力于将CO2分离回收、循环利用和再生转化成资源,化学吸收法是利用吸收剂与CO2发生化学反应来吸收分离CO2的方法,常见的吸收剂有氢氧化钠溶液、氢氧化钙溶液、碳酸钾溶液等,同时加压水洗法也可用于捕获收集CO2。CO2和H2在催化剂的作用下会发生生成甲醇、一氧化碳和甲烷等的一系列反应,实现再生转化。我国科学家在催化剂研究方面取得重大突破,分别合成出了镓酸锌(ZnGa2O4)介孔光催化材料和单晶纳米带,并将其用于CO2的光还原,成功实现了将CO2转化为碳氢化合物燃料。
(1)空气中CO2的主要来源是___________ ;
(2)镓酸锌中镓元素的化合价为___________ ;
(3)用氢氧化钠溶液吸收二氧化碳的化学方程式为___________ ;
(4)CO2和H2在催化剂的作用下生成甲醇的原理为 ,则的化学式为X
,则的化学式为X___________ ;
(5)下列说法正确的是___________ 。
A 化石燃料主要包括煤、石油和天然气,属于可再生能源
B 加压水洗法可捕获收集CO2,是因为压强增大时CO2在水中的溶解度减小
C 对CO2气体加压降温,可获得干冰,此过程中二氧化碳分子之间的间隔会变小
随着人类社会的发展,化石燃料的消耗量急剧增加,释放的CO2越来越多。从而导致温室效应增强,全球气候变暖。科学家一直致力于将CO2分离回收、循环利用和再生转化成资源,化学吸收法是利用吸收剂与CO2发生化学反应来吸收分离CO2的方法,常见的吸收剂有氢氧化钠溶液、氢氧化钙溶液、碳酸钾溶液等,同时加压水洗法也可用于捕获收集CO2。CO2和H2在催化剂的作用下会发生生成甲醇、一氧化碳和甲烷等的一系列反应,实现再生转化。我国科学家在催化剂研究方面取得重大突破,分别合成出了镓酸锌(ZnGa2O4)介孔光催化材料和单晶纳米带,并将其用于CO2的光还原,成功实现了将CO2转化为碳氢化合物燃料。
(1)空气中CO2的主要来源是
(2)镓酸锌中镓元素的化合价为
(3)用氢氧化钠溶液吸收二氧化碳的化学方程式为
(4)CO2和H2在催化剂的作用下生成甲醇的原理为
 ,则的化学式为X
,则的化学式为X(5)下列说法正确的是
A 化石燃料主要包括煤、石油和天然气,属于可再生能源
B 加压水洗法可捕获收集CO2,是因为压强增大时CO2在水中的溶解度减小
C 对CO2气体加压降温,可获得干冰,此过程中二氧化碳分子之间的间隔会变小
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】二氧化碳的捕集和资源化利用是碳中和领域研究热点。
碳捕集 捕捉烟气中 ,将其再释出可实现资源化利用,相关物质转化如下:
,将其再释出可实现资源化利用,相关物质转化如下:____________________ 。
(2)上述流程中可循环使用的物质有__________ 、__________ (填化学式)。
碳的资源化利用 中国科学家已实现由 到淀粉的全人工合成,主要过程如下:
到淀粉的全人工合成,主要过程如下:
 (阶段I)->甲醇->(阶段II)甲醛→…→葡萄糖>·->淀粉
(阶段I)->甲醇->(阶段II)甲醛→…→葡萄糖>·->淀粉
(3)绿色植物实现到葡萄糖的转化过程称为__________ 。
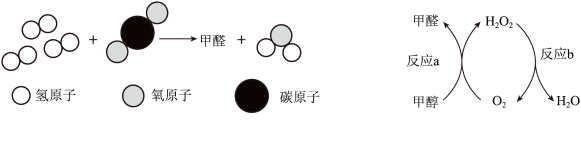
(4)阶段I反应的微观过程如图所示,写出甲醇的化学式:____________________ 。
碳捕集 捕捉烟气中
 ,将其再释出可实现资源化利用,相关物质转化如下:
,将其再释出可实现资源化利用,相关物质转化如下:
(2)上述流程中可循环使用的物质有
碳的资源化利用 中国科学家已实现由
 到淀粉的全人工合成,主要过程如下:
到淀粉的全人工合成,主要过程如下: (阶段I)->甲醇->(阶段II)甲醛→…→葡萄糖>·->淀粉
(阶段I)->甲醇->(阶段II)甲醛→…→葡萄糖>·->淀粉(3)绿色植物实现到葡萄糖的转化过程称为
(4)阶段I反应的微观过程如图所示,写出甲醇的化学式:
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐3】完成下列化学反应的符号表达式,并回答问题。
(1)镁条在空气中燃烧:________________ ;燃烧的镁条应用________ 夹持置于石棉网上。
(2)碳酸氢铵受热分解:________ ;硫酸氢铵通常保存在________ 的地方。
(3)实验室常用来检验二氧化碳的反应:________________ ;现象是________ 。
(4)绿色植物在光照条件下,在叶绿体中将水和二氧化碳转化成葡萄糖(C6H12O6)和氧气:________ ,该反应________ 能量(填“吸收”或“释放”)。
(1)镁条在空气中燃烧:
(2)碳酸氢铵受热分解:
(3)实验室常用来检验二氧化碳的反应:
(4)绿色植物在光照条件下,在叶绿体中将水和二氧化碳转化成葡萄糖(C6H12O6)和氧气:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答下列问题:
(2)t2℃时,将40g甲物质放入50g水中,充分溶解后,所得溶液的质量是______ g。
(3)将t2℃时三种物质的饱和溶液分别降温至t1℃时,所得溶液的溶质质量分数由大到小的顺序是______ 。
(4)某温度下,将一定质量的KNO3溶液进行恒温蒸发结晶,实验过程如图所示,则蒸发前原溶液是
______ (填“饱和”或“不饱和”)溶液,n的数值是______ 。

| A.加乙物质 | B.恒温蒸发部分溶剂 | C.升高温度 | D.降低温度 |
(2)t2℃时,将40g甲物质放入50g水中,充分溶解后,所得溶液的质量是
(3)将t2℃时三种物质的饱和溶液分别降温至t1℃时,所得溶液的溶质质量分数由大到小的顺序是
(4)某温度下,将一定质量的KNO3溶液进行恒温蒸发结晶,实验过程如图所示,则蒸发前原溶液是

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】甲、乙、丙三种物质的溶解度曲线如图。回答下列问题:

(1)在______ ℃时,乙和丙的溶解度相等。
(2)t3℃,将35g甲加入到50g水中,所得溶液中溶质与溶剂的质量比为______ 。
(3)t1℃,将乙溶液的状态由M点变为N点,方法是______ 。
(4)t3℃时,甲、乙、丙三种物质的饱和溶液同时降温至t2℃时,所得溶液中溶质质量分数由大到小的顺序为______ 。

(1)在
(2)t3℃,将35g甲加入到50g水中,所得溶液中溶质与溶剂的质量比为
(3)t1℃,将乙溶液的状态由M点变为N点,方法是
(4)t3℃时,甲、乙、丙三种物质的饱和溶液同时降温至t2℃时,所得溶液中溶质质量分数由大到小的顺序为
您最近一年使用:0次




