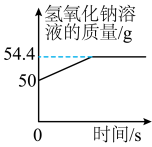
工业盐酸中通常溶有少量的FeCl3而呈黄色,小红进行了如下实验:取一定质量该工业盐酸,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示。请回答下列问题:
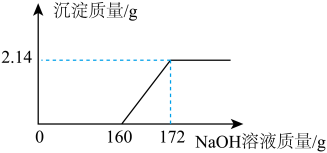
(1)FeCl3与NaOH恰好完全反应时,生成沉淀的质量是 g。
(2)所用NaOH溶液的溶质质量分数是多少?

(1)FeCl3与NaOH恰好完全反应时,生成沉淀的质量是 g。
(2)所用NaOH溶液的溶质质量分数是多少?
更新时间:2020-04-29 17:40:42
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】为测定一瓶由Na2CO3 、NaOH组成的固体混合物中NaOH的质量分数,小明采用沉淀法进行如下操作:①取20克样品于烧杯中,加足量水配成溶液;②在样品溶液中加入过量的BaCl2溶液;③待反应完全后,过滤、洗涤、干燥、称量。有关数据记录如下表:
请回答下列问题:
(1)反应共生成沉淀_____g,原样品中NaOH的质量分数是多少?
(2)在反应前后的溶液中,下列元素质量保持不变的是_____。
A 钠元素 B 碳元素 C 钡元素 D 氧元素
(3)实验操作步骤③中,确定沉淀洗涤干净的方法:取最后一次洗涤液,滴加_____试剂,观察到_____现象,则已洗涤干净。
| 反应前 | 反应后 | |
| 烧杯和样品 溶液总质量/g | 加入的氯化钡 溶液质量/g | 过滤后烧杯和溶液总质量/g (滤液的损失忽略不计) |
| 95 | 65 | 140.3 |
请回答下列问题:
(1)反应共生成沉淀_____g,原样品中NaOH的质量分数是多少?
(2)在反应前后的溶液中,下列元素质量保持不变的是_____。
A 钠元素 B 碳元素 C 钡元素 D 氧元素
(3)实验操作步骤③中,确定沉淀洗涤干净的方法:取最后一次洗涤液,滴加_____试剂,观察到_____现象,则已洗涤干净。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献.工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质.现称取只含氯化钠杂质的纯碱样品l1g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g.
试求:
(1)该纯碱样品的纯度(计算结果精确到0.1%)
(2)所得溶液中溶质的质量分数.
试求:
(1)该纯碱样品的纯度(计算结果精确到0.1%)
(2)所得溶液中溶质的质量分数.
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】将木炭和氧化铜的粉末均匀混合,放入试管中高温加热至质量不再减少,冷却后称量粉末为10.6g。把该粉末全部倒入烧杯中,加入足量的溶质质量分数为9.8%的稀硫酸充分搅拌,得到蓝色溶液和红色不溶物,将不溶物进行过滤、干燥、称量其质量(如图所示)。请计算
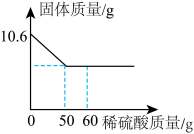
(1)反应生成铜的质量为多少克?
(2)恰好完全反应时溶液中溶质质量分数是多少?(结果保留至0.1%)

(1)反应生成铜的质量为多少克?
(2)恰好完全反应时溶液中溶质质量分数是多少?(结果保留至0.1%)
您最近一年使用:0次
【推荐1】现有H2SO4与CuSO4的混合溶液,为了分析混合溶液中H2SO4与CuSO4的质量分数,设计了如图实验方案:
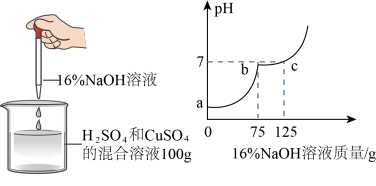
(1)根据图坐标,推测CuSO4溶液呈______ (填“酸”、“碱”、“中”)性;C点溶液中的溶质为______ (写化学式)。
(2)请计算该混合溶液中的CuSO4的溶质质量分数。
(3)若在100g混合溶液中不断加入上述氢氧化钠溶液,请你在图中画出加入氢氧化钠溶液的质量与产生沉淀的质量的关系图。

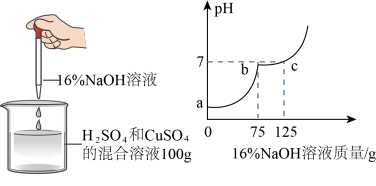
(1)根据图坐标,推测CuSO4溶液呈
(2)请计算该混合溶液中的CuSO4的溶质质量分数。
(3)若在100g混合溶液中不断加入上述氢氧化钠溶液,请你在图中画出加入氢氧化钠溶液的质量与产生沉淀的质量的关系图。

您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】将7.2g含有氧化铜和铜的混合物粉末置于烧杯中,向其中加入70.9g稀硫酸,充分反应后,再向烧杯中加入溶质质量分数为20%的氢氧化钠溶液,在加入氢氧化钠溶液的过程中,烧杯内不溶性固体物质的质量与加入氢氧化钠溶液的质量关系如图所示。试计算:(反应用到的化学方程式: ,
,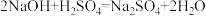 )。
)。
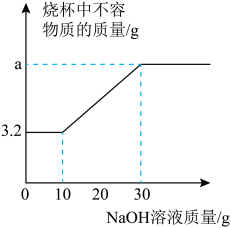
(1)a的质量为______g;
(2)求氢氧化钠溶液恰好完全反应后所得溶液的溶质质量分数(写出计算过程)。
 ,
,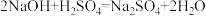 )。
)。
(1)a的质量为______g;
(2)求氢氧化钠溶液恰好完全反应后所得溶液的溶质质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】为确定某变质的烧碱样品的变质情况,某化学小组进行了如图1实验:
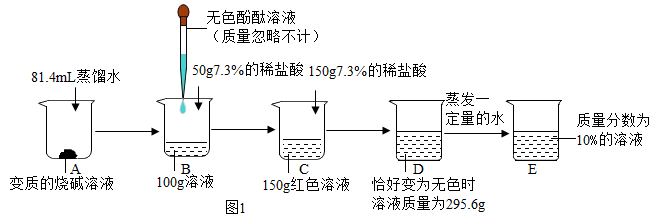
(1)B中加入稀盐酸后发生反应的化学方程式为_____;
(2)根据已知条件列出求解样品中碳酸钠的质量(x)的比例式为_____;
(3)由D﹣E蒸发水的质量为_____g;
(4)样品中未变质的烧碱占变质前原烧碱的质量分数为_____;
(5)提纯上述变质的烧碱样品需要①_____(填一种固体)的质量为②_____;
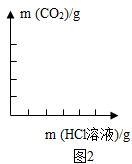
(6)请绘制加入稀盐酸与生成气体质量关系的曲线图____。

(1)B中加入稀盐酸后发生反应的化学方程式为_____;
(2)根据已知条件列出求解样品中碳酸钠的质量(x)的比例式为_____;
(3)由D﹣E蒸发水的质量为_____g;
(4)样品中未变质的烧碱占变质前原烧碱的质量分数为_____;
(5)提纯上述变质的烧碱样品需要①_____(填一种固体)的质量为②_____;

(6)请绘制加入稀盐酸与生成气体质量关系的曲线图____。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某锥形瓶盛有盐酸和氯化镁的混合溶液100g,向其中逐滴滴加溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量变化关系如图所示。请计算:_______ g。
(2)写出AB段反应的化学方程式:________ 。
(3)混合溶液中稀盐酸的质量分数为________ 。
(4)反应后生成白色沉淀的质量为________ 。
(5)设参加反应的氯化镁的质量为x,列出求解氯化镁质量的比例式:________ 。
(6)向反应至B点时锥形瓶内所得溶液中再加入4.1g水后,请计算所得溶液溶质质量分数为________ 。
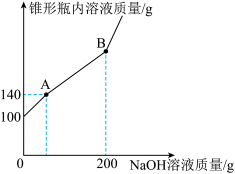
(2)写出AB段反应的化学方程式:
(3)混合溶液中稀盐酸的质量分数为
(4)反应后生成白色沉淀的质量为
(5)设参加反应的氯化镁的质量为x,列出求解氯化镁质量的比例式:
(6)向反应至B点时锥形瓶内所得溶液中再加入4.1g水后,请计算所得溶液溶质质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某校化学兴趣小组同学,将一定量的稀硫酸滴入12.5g氢氧化钾和碳酸钾的固体混合物中,产生气体质量与滴入稀硫酸的质量关系如图所示。请回答:
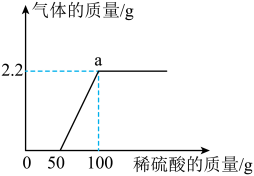
(1)发生中和反应的化学方程式:_______ 。
(2)a点时溶液中的溶质为_______ ,其质量分数为_______ (计算结果精确至0.1%)。

(1)发生中和反应的化学方程式:
(2)a点时溶液中的溶质为
您最近一年使用:0次