超市出现了一种名为“污渍爆炸盐”的洗新产品,能在瞬间去除洗衣粉难以洗掉的多种顽固污渍。某校化学兴趣小组的同学在老师的指导下对该产品开展了以下探究活动。
【阅读标签】本产品不含磷,环保。
【查阅资料】①“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4,俗称固体双氧水),它是一种白色结晶颗粒,易溶于水,且能与水反应,生成碳酸盐和其他化合物。
②氢氧化镁是不溶于水的白色固体。
【提出问题】“污渍爆炸盐”水溶液的成分是什么呢?
【作出猜想】猜想一:Na2CO3 和_____________ ;
猜 想 二 :Na2CO3 和 NaOH;
猜想三:Na2CO3、______________ 和____________ 。
【实验探究】
【得出结论】猜想_______________________ 正确。
请写出过碳酸钠与水反应的化学方程式:________________________ 。
【阅读标签】本产品不含磷,环保。
【查阅资料】①“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4,俗称固体双氧水),它是一种白色结晶颗粒,易溶于水,且能与水反应,生成碳酸盐和其他化合物。
②氢氧化镁是不溶于水的白色固体。
【提出问题】“污渍爆炸盐”水溶液的成分是什么呢?
【作出猜想】猜想一:Na2CO3 和
猜 想 二 :Na2CO3 和 NaOH;
猜想三:Na2CO3、
【实验探究】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取少量“污渍爆炸盐”于烧杯中,加入足量蒸馏水充分搅拌。 | 固体完全溶解形成无色溶液 | / |
| ② | 取适量①的溶液于试管中,先向其中加入少量二氧化锰粉末,再将带火星的木条置于试管口 | 有大量气泡产生,木条复燃 | 含有 |
| ③ | 取适量①的溶液于试管中,向其中加入足量 | 有白色沉淀产生 | 含有碳酸钠 |
| ④ | 取适量③的上层清液于试中,向其中滴加少量氯化镁溶液,振荡 | 清液中 | 不含氢氧化钠 |
【得出结论】猜想
请写出过碳酸钠与水反应的化学方程式:
更新时间:2020-05-01 22:51:23
|
相似题推荐
【推荐1】欧阳同学用“双氧水”(过氧化氢溶液)油洗伤口时,不小心将过氧化氢溶液滴到水泥地板上,发现有大量气泡产生。
【查阅资料】
①水泥块中含有的氯化铁,二氧化锰,碘化钾都可以作过氧化氢分解的催化剂。
②气压传感器能描绘出密闭容器中压强随时间的变化曲线(如图1)。曲线斜率越大,说明过氧化氢分解速度越快,则该条件对过氧化氢分解速率影响越大。
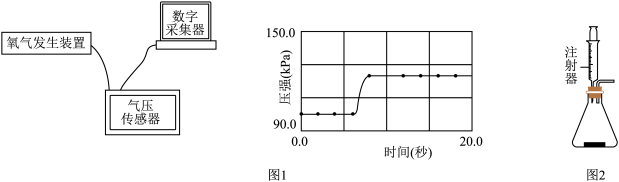
实验一:探究氯化铁能否做过氧化氢分解的催化剂。
(1)在进行实验前,要注意检查装置的气密性。检查图2装置气密性的方法是玻璃管右侧加橡皮管,用止水夹夹住橡皮管,再拉注射器,一段时间后,注射器
______ (填“能”、“不能”)回到原来的位置,则表明气密性良好。
(2)小芳认为:仅凭上述两个实验不能证明氯化铁为过氧化氢分解的催化剂,她觉得还需要证明它在化学反应前后
______ 不变。
(3)经实验证明,氯化铁能做过氧化氢分解的催化剂,写出此反应的文字表达式
______ 。
实验二:探究过氧化氢分解速率的影响因素。
将体积相同、浓度不同的过氧化氢溶液和不同质量的二氧化锰、氯化铁、碘化钾分别放在如图2的密闭容器中,并用气压传感器采集数据:
(4)由实验1和2对比得出结论是
______ 。
(5)小明认为:不采用气压传感器,还可用100mL量筒、水槽、秒表等,通过测量
______ ,判断过氧化氢的分解速率。
(6)分析上表,过氧化氢分解速率的影响因素,除了温度,还有
______ 。(填一种即可)
【查阅资料】
①水泥块中含有的氯化铁,二氧化锰,碘化钾都可以作过氧化氢分解的催化剂。
②气压传感器能描绘出密闭容器中压强随时间的变化曲线(如图1)。曲线斜率越大,说明过氧化氢分解速度越快,则该条件对过氧化氢分解速率影响越大。

实验一:探究氯化铁能否做过氧化氢分解的催化剂。
(1)在进行实验前,要注意检查装置的气密性。检查图2装置气密性的方法是玻璃管右侧加橡皮管,用止水夹夹住橡皮管,再拉注射器,一段时间后,注射器
| 实验步骤 | 实验现象 | 实验结论 |
| ①向装有过氧化氢溶液的试管中, 伸入带火星的木条 | 木条不复燃 | 常温时过氧化氢溶液不 分解 |
| ②向装有过氧化氢溶液的试管中加入 氯化铁,再伸入带火星的木条 | 氯化铁能加快过氧化氢 的分解速率 |
(2)小芳认为:仅凭上述两个实验不能证明氯化铁为过氧化氢分解的催化剂,她觉得还需要证明它在化学反应前后
(3)经实验证明,氯化铁能做过氧化氢分解的催化剂,写出此反应的文字表达式
实验二:探究过氧化氢分解速率的影响因素。
将体积相同、浓度不同的过氧化氢溶液和不同质量的二氧化锰、氯化铁、碘化钾分别放在如图2的密闭容器中,并用气压传感器采集数据:
| 实验序号 | 催化剂种类 | 催化剂质量/g | 温度/℃ | 过氧化氢浓度 | 曲线斜率 |
| 1 | 二氧化锰 | 0.1 | 10 | 2% | 0.383 |
| 2 | 0.1 | 20 | 2% | 2.145 | |
| 3 | 0.3 | 20 | 5% | 6.637 | |
| 4 | 氯化铁 | 0.3 | 20 | 5% | 0.099 |
| 5 | 碘化钾 | 0.3 | 20 | 5% | 0.163 |
(4)由实验1和2对比得出结论是
(5)小明认为:不采用气压传感器,还可用100mL量筒、水槽、秒表等,通过测量
(6)分析上表,过氧化氢分解速率的影响因素,除了温度,还有
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某小组以“探究过氧化氢分解速率的影响因素”为主题开展项目式学习。
【任务1】小组同学探究二氧化锰能否改变反应速率,实验设计方案如图1所示。
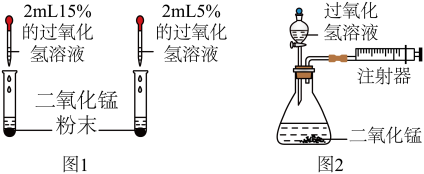
(1)写出向过氧化氢溶液中加入二氧化锰发生反应的化学方程式:_______ 。
(2)该设计方案不能达到实验目的,原因是_______ 。
【任务2】定量研究过氧化氢溶液浓度大小对其分解速率的影响。
小组同学分别取20mL浓度为5%、15%的过氧化氢溶液,按照图2所示装置开展实验,具体实验数据如下。
(3)x=_______ ;实验测量的数据是_______ 。
(4)若测量数据a>b,则得出的结论是_______ 。
【任务3】探究二氧化锰的用量对过氧化氢分解速率的影响。
(5)小组同学探究所用的实验装置及实验数据如图3所示,请分析实验数据可获得的结论是___ 。
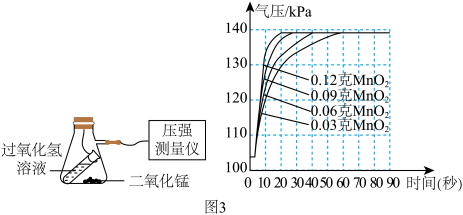
【任务4】继续探究影响过氧化氢分解速率的其他因素。
(6)请大胆猜想其他可能的影响因素:_______ 。
(7)试设计实验方案验证:_______ 。
【任务1】小组同学探究二氧化锰能否改变反应速率,实验设计方案如图1所示。

(1)写出向过氧化氢溶液中加入二氧化锰发生反应的化学方程式:
(2)该设计方案不能达到实验目的,原因是
【任务2】定量研究过氧化氢溶液浓度大小对其分解速率的影响。
小组同学分别取20mL浓度为5%、15%的过氧化氢溶液,按照图2所示装置开展实验,具体实验数据如下。
| 实验次数 | 过氧化氢溶液浓度 | 过氧化氢溶液用量/mL | 二氧化锰用量/g | 反应温度/℃ | 收集气体体积/mL | 测量数据 |
| 1 | 5% | 20 | 1 | 50 | 3 | a |
| 2 | 15% | 20 | x | 50 | 3 | b |
(3)x=
(4)若测量数据a>b,则得出的结论是
【任务3】探究二氧化锰的用量对过氧化氢分解速率的影响。
(5)小组同学探究所用的实验装置及实验数据如图3所示,请分析实验数据可获得的结论是

【任务4】继续探究影响过氧化氢分解速率的其他因素。
(6)请大胆猜想其他可能的影响因素:
(7)试设计实验方案验证:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】兴趣小组同学在老师的带领下,探究影响过氧化氢分解速率的因素。

【提出问题】影响过氧化氢分解的因素有哪些?
【做出假设】假设1:催化剂的种类
假设2:过氧化氢溶液的浓度
假设3:温度
【实验探究】学生利用如图所示装置,以收集50 mL的气体为标准,比较反应的快慢,实验方案如下表所示:
(1)写出实验3发生反应的文字表达式______ 。
(2)对比实验1和2,得出的结论是______ 。
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强的实验依据是______ 。
(4)实验中,使用注射器的优点是______ 。
【拓展延伸】在实验3探究中,学生将注射器换成了压强传感器,测出了实验过程中装置中压强与时间的关系图(如图)。实验过程中,学生触摸谁形瓶外壁,有发烫的感觉。至反应结束后,发生装置的温度慢慢趋于常温。
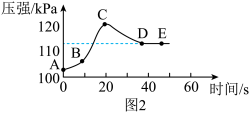
(5)实验中,过氧化氢反应结束是在______ (填字母)点。
(6)根据图所示,我们分析发现:反应速率在不断发生改变。反应过程中从开始到结束影响反应速率的因素有______ (填2种)。
(7)图中,CD段压强降低的主要原因是______ 。

【提出问题】影响过氧化氢分解的因素有哪些?
【做出假设】假设1:催化剂的种类
假设2:过氧化氢溶液的浓度
假设3:温度
【实验探究】学生利用如图所示装置,以收集50 mL的气体为标准,比较反应的快慢,实验方案如下表所示:
序号 | 温度/℃ | 过氧化氢溶液 浓度 | 过氧化氢溶液 体积/mL | l g催化剂 | 时间/s |
1 | 20 | 5% | 40 | 二氧化锰 | 37 |
2 | 20 | 10% | 40 | 二氧化锰 | 14 |
3 | 20 | 5% | 40 | 氧化铜 | b |
4 | 80 | 5% | 40 | 二氧化锰 | 29 |
(2)对比实验1和2,得出的结论是
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强的实验依据是
(4)实验中,使用注射器的优点是
【拓展延伸】在实验3探究中,学生将注射器换成了压强传感器,测出了实验过程中装置中压强与时间的关系图(如图)。实验过程中,学生触摸谁形瓶外壁,有发烫的感觉。至反应结束后,发生装置的温度慢慢趋于常温。

(5)实验中,过氧化氢反应结束是在
(6)根据图所示,我们分析发现:反应速率在不断发生改变。反应过程中从开始到结束影响反应速率的因素有
(7)图中,CD段压强降低的主要原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】同学们为提升化学实验操作技能,在实验室练习如图实验:

(1)实验A中观察到的现象是_______ 。
(2)实验B中的化学方程式________ 。
实验完毕后,小明误将A试管中的物质倒入B试管中,充分振荡后,观察到混合溶液为无色,小明对该无色溶液的成分产生兴趣并开展探究:
【提出问题】混合后无色溶液的溶质除酚酞外还有什么?
【查阅资料】 溶液、
溶液、 溶液显中性
溶液显中性
【猜想与假设】猜想一: ;猜想二:
;猜想二: ;猜想三:
;猜想三: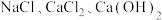 ,经分析猜想三错误,其理由是
,经分析猜想三错误,其理由是________ 。
【设计并进行实验】为了验证其余猜想,小明进行如下实验:
【反思与拓展】
I.有同学提议将上表操作中的氧化铁换成另一种药品或用品:________ (除金属氧化物外),也可得出猜想二正确的实验结论。
Ⅱ.小明误倒后,如果观察到试管底部有白色沉淀,上层清液为红色,则上层清液中一定有的阴离子是______ (填离子符号)。

(1)实验A中观察到的现象是
(2)实验B中的化学方程式
实验完毕后,小明误将A试管中的物质倒入B试管中,充分振荡后,观察到混合溶液为无色,小明对该无色溶液的成分产生兴趣并开展探究:
【提出问题】混合后无色溶液的溶质除酚酞外还有什么?
【查阅资料】
 溶液、
溶液、 溶液显中性
溶液显中性【猜想与假设】猜想一:
 ;猜想二:
;猜想二: ;猜想三:
;猜想三: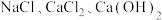 ,经分析猜想三错误,其理由是
,经分析猜想三错误,其理由是【设计并进行实验】为了验证其余猜想,小明进行如下实验:
| 实验操作 | 实验现象 | 解释与结论 |
| 取少量混合后的无色溶液于试管中,加入氧化铁 | 解释: |
I.有同学提议将上表操作中的氧化铁换成另一种药品或用品:
Ⅱ.小明误倒后,如果观察到试管底部有白色沉淀,上层清液为红色,则上层清液中一定有的阴离子是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】日常生活中,人们常利用泡打粉来制作馒头,糕点等食品,主要是利用制作过程中产生的二氧化碳气体,使馒头变得松软可口。某小组同学对利用泡打粉发面的原理进行了如下探究。
【查阅资料】泡打粉是一种复配膨松剂,主要成分是固体碳酸氢钠和酒石酸氢钾(化学式为:KC4H5O6),又称为发泡粉,可作为快速发面剂用于制作面食。
【知识应用】
(1)碳酸氢钠的俗称是_____ 。
【提出问题】泡打粉为什么会产生二氧化碳?
【作出猜想】
猜想一:碳酸氢钠受热分解产生二氧化碳气体。
猜想二:酒石酸氢钾受热分解,产生二氧化碳气体。
猜想三:碳酸氢钠和酒石酸氢钾在溶液中发生反应,产生二氧化碳气体。
【进行实验】
(2)小组同学设计并进行了如图所示的实验。
实验二:在装置1的a试管中放入少量酒石酸氢钾固体,加热,观察到a试管内壁有无色液滴,b试管中_____ 的现象,证明猜想二不成立;
实验三:在装置2的c试管中放入少量碳酸氢钠和酒石酸氢钾的固体混合物,滴加_____ ;观察到试管c中_____ ,d试管中澄清石灰水变浑浊,证明猜想三成立。
【反思交流】
(3)碳酸氢钠受热易分解产生碳酸钠和两种常见氧化物,化学方程式为_____ 。
(4)小组同学又用碳酸钠代替碳酸氢钠,在装置2中做了与实验三相同的实验,结果观察到相同的实验现象。由此,同学们得出泡打粉能发面(能产生二氧化碳)的化学原理是_____ 。
【拓展应用】
(5)在保存泡打粉时,应注意_____ 。
【查阅资料】泡打粉是一种复配膨松剂,主要成分是固体碳酸氢钠和酒石酸氢钾(化学式为:KC4H5O6),又称为发泡粉,可作为快速发面剂用于制作面食。
【知识应用】
(1)碳酸氢钠的俗称是
【提出问题】泡打粉为什么会产生二氧化碳?
【作出猜想】
猜想一:碳酸氢钠受热分解产生二氧化碳气体。
猜想二:酒石酸氢钾受热分解,产生二氧化碳气体。
猜想三:碳酸氢钠和酒石酸氢钾在溶液中发生反应,产生二氧化碳气体。
【进行实验】
(2)小组同学设计并进行了如图所示的实验。
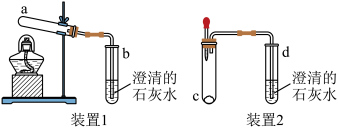
实验二:在装置1的a试管中放入少量酒石酸氢钾固体,加热,观察到a试管内壁有无色液滴,b试管中
实验三:在装置2的c试管中放入少量碳酸氢钠和酒石酸氢钾的固体混合物,滴加
【反思交流】
(3)碳酸氢钠受热易分解产生碳酸钠和两种常见氧化物,化学方程式为
(4)小组同学又用碳酸钠代替碳酸氢钠,在装置2中做了与实验三相同的实验,结果观察到相同的实验现象。由此,同学们得出泡打粉能发面(能产生二氧化碳)的化学原理是
【拓展应用】
(5)在保存泡打粉时,应注意
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小某兴趣小组用图1所示装置试验石灰水的导电性、观察到灯泡发光;有同学发现通电一段时间后,两个石墨电极附近有气泡产生,且与正极相连的石墨附近产生大量白色浑浊。兴趣小组对此展开探究。
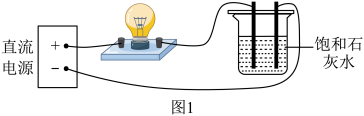
(1)灯泡发光,说明石灰水能导电。氢氧化钙在水中解离出的阳离子是______ (写微粒符号)。
(2)与负极相连的石墨附近产生的气体是______ 。
(3)白色浑浊产生的原因。
猜想一:溶液温度升高导致氢氧化钙析出。
猜想二:水减少导致氢氧化钙析出。
猜想三:与正极相莲的石墨附近产生的气体与______ 反应,生成的气体和石灰水反应生成碳酸钙。最后一个反应的化学方程式为______ 。
(4)另取三份相同的饱和石灰水,测定其温度和质量,进行以下实验探究。
【实验1】一份重复导电性实验。测定溶液产生大量白色浑浊时的温度和质量。
【实验2】一份加热升高且同温度,未观察到明显的白色浑浊。
【实验3】一份恒温蒸发相同质量的水,观察到产生少量白色浑浊。
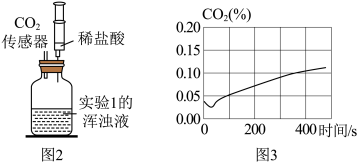
【实验4】实验装置如图2所示;检查装置气密性,加入实验1中的浑浊液,开启传感器,然后注入足量的稀盐酸。广口瓶中二氧化碳的含量随时间变化的曲线如图3所示。
(5)分析与结论:
①白色浑浊物中含有氢氧化钙。氢氧化钙析出的主要原因是______ 。
②图3曲线中,二氧化碳含量在开始阶段降低的原因是______ ;根据图中曲线,说明白色浑浊物中______ 。
(6)实验拓展:若通电相同时间,减少白色浑浊物产生的措施有:______ (写一条)。

(1)灯泡发光,说明石灰水能导电。氢氧化钙在水中解离出的阳离子是
(2)与负极相连的石墨附近产生的气体是
(3)白色浑浊产生的原因。
猜想一:溶液温度升高导致氢氧化钙析出。
猜想二:水减少导致氢氧化钙析出。
猜想三:与正极相莲的石墨附近产生的气体与
(4)另取三份相同的饱和石灰水,测定其温度和质量,进行以下实验探究。
【实验1】一份重复导电性实验。测定溶液产生大量白色浑浊时的温度和质量。
【实验2】一份加热升高且同温度,未观察到明显的白色浑浊。
【实验3】一份恒温蒸发相同质量的水,观察到产生少量白色浑浊。
【实验4】实验装置如图2所示;检查装置气密性,加入实验1中的浑浊液,开启传感器,然后注入足量的稀盐酸。广口瓶中二氧化碳的含量随时间变化的曲线如图3所示。

(5)分析与结论:
①白色浑浊物中含有氢氧化钙。氢氧化钙析出的主要原因是
②图3曲线中,二氧化碳含量在开始阶段降低的原因是
(6)实验拓展:若通电相同时间,减少白色浑浊物产生的措施有:
您最近一年使用:0次



