【查阅资料】
①水泥块中含有的氯化铁,二氧化锰,碘化钾都可以作过氧化氢分解的催化剂。
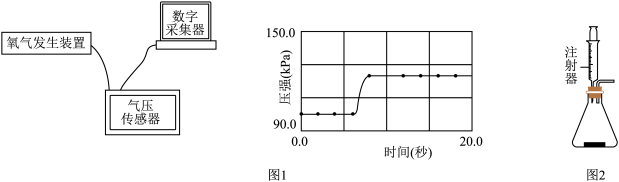
②气压传感器能描绘出密闭容器中压强随时间的变化曲线(如图1)。曲线斜率越大,说明过氧化氢分解速度越快,则该条件对过氧化氢分解速率影响越大。
实验一:探究氯化铁能否做过氧化氢分解的催化剂。
(1)在进行实验前,要注意检查装置的气密性。检查图2装置气密性的方法是玻璃管右侧加橡皮管,用止水夹夹住橡皮管,再拉注射器,一段时间后,注射器
| 实验步骤 | 实验现象 | 实验结论 |
| ①向装有过氧化氢溶液的试管中, 伸入带火星的木条 | 木条不复燃 | 常温时过氧化氢溶液不 分解 |
| ②向装有过氧化氢溶液的试管中加入 氯化铁,再伸入带火星的木条 | 氯化铁能加快过氧化氢 的分解速率 |
(2)小芳认为:仅凭上述两个实验不能证明氯化铁为过氧化氢分解的催化剂,她觉得还需要证明它在化学反应前后
(3)经实验证明,氯化铁能做过氧化氢分解的催化剂,写出此反应的文字表达式
实验二:探究过氧化氢分解速率的影响因素。
将体积相同、浓度不同的过氧化氢溶液和不同质量的二氧化锰、氯化铁、碘化钾分别放在如图2的密闭容器中,并用气压传感器采集数据:
| 实验序号 | 催化剂种类 | 催化剂质量/g | 温度/℃ | 过氧化氢浓度 | 曲线斜率 |
| 1 | 二氧化锰 | 0.1 | 10 | 2% | 0.383 |
| 2 | 0.1 | 20 | 2% | 2.145 | |
| 3 | 0.3 | 20 | 5% | 6.637 | |
| 4 | 氯化铁 | 0.3 | 20 | 5% | 0.099 |
| 5 | 碘化钾 | 0.3 | 20 | 5% | 0.163 |
(4)由实验1和2对比得出结论是
(5)小明认为:不采用气压传感器,还可用100mL量筒、水槽、秒表等,通过测量
(6)分析上表,过氧化氢分解速率的影响因素,除了温度,还有
相似题推荐
小芳发现,氯酸钾与氧化铜或氧化铁混合加热,也能较快产生氧气,于是进行了如下探究:
【提出猜想】除MnO2外,CuO和Fe2O3也可以作KClO3分解的催化剂。
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(℃) |
① | KClO3 | 580 |
② | KClO3、MnO2(质量比1:1) | 350 |
③ | KClO3、CuO(质量比l:1) | 370 |
④ | KClO3、Fe2O3(质量比1:1) | 390 |
【得出结论】(1)由实验
(2)实验所用的三种金属氧化物,催化效果最好的是
【反思】(3)若要证明CuO和Fe2O3是该反应的催化剂,还要验证它们在化学反应前后的质量和
(4)同种催化剂,颗粒大小可能影响催化效果,请你设计实验方案进行验证:
(5)同种催化剂,还有哪些因素可能影响催化效果,请你设计实验探究(探究一种因素即可)。
【影响因素】
【实验设计】


(1)一次性医用三层口罩是由专业两层纤维无纺布和中间一层熔喷布,经超声波焊接而成,能像滤纸一样起到
(2)84消毒液的成分为次氯酸钠(NaClO)、表面活性剂和水等,次氯酸钠中氯元素的化合价为
(3)某兴趣小组对84消毒液和过氧化氢消毒剂进行如下探究活动。
【实验1】取少量84消毒液于试管中,滴加过氧化氢消毒剂,发现有大量气泡产生;然后
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】
猜想一:作反应物,NaClO与过氧化氢消毒剂发生化学反应;
猜想二:作催化剂,与分解过氧化氢溶液制氧气时二氧化锰类似。
【实验2】①按图2所示组装实验装置,并
②向锥形瓶中加入30mL 84消毒液,注射器中吸入25mL过氧化氢溶液。
③将注射器中的过氧化氢溶液平均分5次推入锥形瓶中;每次推入过氧化氢溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响)见表。
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 收集气体的总体积/mL | 140 | 280 | 365 | 370 | 375 |
【拓展反思】生活中常用的消毒剂除84消毒液、过氧化氢消毒剂外,还有医用酒精、过氧乙酸等,在使用各种消毒剂时,要考虑它们的性质,切记:科学使用,注意安全!生活中下列使用消毒剂的做法正确的是
A不同的消毒剂可随意混合使用
B使用84消毒液的浓度越高越好
C使用医用酒精消毒应远离明火,防止火灾
D 84消毒液、医用酒精等消毒剂均应密封保存
【猜想】I.Fe2O3是反应的催化剂,反应前后
II.Fe2O3参与反应产生O2,反应前后质量和化学性质发生了改变;
III.Fe2O3不是催化剂、也不参与反应,反应前后质量和化学性质不变.
【查阅资料】Fe2O3属于碱性氧化物,能够与稀盐酸反应生成氯化铁;氯化铁溶液显棕黄色.
【实验】用天平称量 0.3gFe2O3,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡放出, | 猜想I成立; 猜想II、III不成立. |
(2)步骤①的目的是
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、
(4)过氧化氢能被Fe2O3催化分解放出O2的化学方程式为
【拓展】
(1)要探究步骤⑤做过催化剂的Fe2O3其它化学性质,还应补做的实验是
(2)该同学为了探究Fe2O3的用量对H2O2分解速率的影响.每次均用30mL 10%的H2O2溶液,使用不同质量的Fe2O3作催化剂,测定每次收集到500mL O2所用的时间.结果如图(其他实验条件相同),由图可知,Fe2O3的用量对H2O2分解速率影响的规律是:
①
②Fe2O3的用量超出一定范围后,其用量再增大,反应速率不再继续加快.
【提出问题】氧化铁能否作过氧化氢分解的催化剂?
【作出假设】氧化铁能作过氧化氢分解的催化剂。
【设计实验】
实验步骤 | 实验现象 |
| ①取5mL5%过氧化氢溶液放入A试管中,并插入带火星木条。 | 带火星木条不复燃 |
| ②取5mL5%过氧化氢溶液放入B试管中,加入ag氧化铁粉末, 并插入带火星的木条。 | |
| ③待A试管中没有现象发生时,重新加入过氧化氢溶液,并把 带火星的木条伸入试管,如此反复多次试验,观察现象。 | 带火星木条复燃 |
| ④将实验③中的剩余物过滤,并将所得滤渣进行洗涤、干燥。 称量。 |
(1)实验步骤②中看到的现象是
(2)实验步骤③证明氧化铁的
(3)实验步骤④中,若所得固体质量为
【实验结论】
(4)通过实验步骤
【实验拓展】
(5)比较氧化铁和二氧化锰在分解过氧化氢制氧气反应中的催化效果。可以通过比较在相同条件下测量收集相同体积的氧气所需的时间。若加入氧化铁所需时间
(6)下列有关催化剂的说法中正确的是______。
| A.催化剂只能加快化学反应的速率 |
| B.同一个化学反应可以有多种催化剂 |
| C.二氧化锰只能作过氧化氢分解的催化剂 |
| D.用作催化剂的物质不可能是其他反应的反应物或生成物 |
【猜想】 氧化铜能做过氧化氢分解的催化剂。
【实验】 用天平称量 0.2g 氧化铜,取 5mL5%的过氧化氢溶液于试管中,进行如下实验。

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 产生大量的气泡,带火星的木条复燃 | 氧化铜的质量仍为 | 溶液中有气泡放出, | 猜想成立 |
(3)过氧化氢被氧化铜催化分解放出氧气的文字表达式为
(4)步骤⑦的目的是
【猜想】土豆丝可作过氧化氢分解的催化剂
【实验】设计并完成下表所示的探究实验:
| 实验操作 | 实验现象 | 结论 | 总结 | |
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星木条 | 有小气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是 | 土豆丝可作过氧化氢分解的催化剂 |
| 实验二 | 取5mL5%的过氧化氢溶液于试管中,加入土豆丝,伸入带火星木条[来 | 迅速产生大量气泡, | 土豆丝能加快过氧化氢的分解的速率 |
(1)请你帮小明同学填写上表中未填完的空格.
(2)在小明的探究实验中,“实验一”和“实验二”起的作用是
【反思】小凡同学认为仅由上述实验还不能完全得出表内的“总结”,他补充设计了两个方面的探究实验。
第一方面探究
向反应后试管内的剩余物中重新加入过氧化氢溶液,有大量气泡产生,且木条复燃;
第二方面探究
实验操作中包含了两次称量,将实验二试管中的物质进行过滤、洗涤、干燥、称量(土豆丝本身的水分减少忽略不计)。
[查阅资料]
①电解纯水速率较慢,加入氢氧化钾、氢氧化钠、碳酸钠、硫酸钠等电解质增强导电性,加快反应速率。
②氢氧化钠、氢氧化钾有较强腐蚀性。
③去离子水是指除去呈离子形式杂质后的纯水,生产成本较高。

往图1水杯中分别加入等量的浓度为12%的碳酸钠、硫酸钠、氢氧化钾和氢氧化钠溶液进行实验,通电相同时间读取并记录数据,重复实验三次,计算氢气产生速率,结果如图3。

(2)由图3判断:影响水电解速率最大的电解质是
[实验2]探究水电解实验中电解质溶液的最佳浓度(以氢氧化钠溶液为例),结果如图4。

[实验3]将下列电极连接电源负极,探究不同电极材料对水电解速率的影响,测定产生氢气的速率(cm3/s)如表。
| 电极材料 | 铁丝 | 铜丝 | 铁镍合金 | 石墨 |
| 第1次 | 0.0164 | 0.0214 | 0.0138 | 0.0031 |
| 第2次 | 0.0159 | 0.0207 | 0.0150 | 0.0027 |
| 第3次 | 0.0161 | 0.0209 | 0.0144 | 0.0034 |
| 平均值 | 0.0160 | 0.0210 | 0.0144 | 0.0030 |
(4)本实验条件下,最佳电极材料是
(5)选择电极材料需考虑的因素:电极应与电解质溶液不反应。若用铁作电极,电解质溶液不能用稀硫酸,原因是
(6)为验证温度也是影响水电解速率的因素,请写出实验方案:
【查阅资料】红磷(由磷元素组成的一种单质)在空气中燃烧生成的五氧化二磷刺激人体呼吸道,因此五氧化二磷也是一种空气污染物。

(1)使用这两个装置,在测定氧气含量前必须检查装置的气密性,检查图Ⅰ装置气密性的方法是
(2)由图1实验可以推知反应后剩余气体的主要性质是:
(3)图1实验开始的实验现象是:
(4)图Ⅱ实验过程中,若未用弹簧夹夹紧橡皮管,注射器活塞将从10ml处先向
(5)对照两个实验装置,图Ⅱ实验装置的优点是(回答一个即可)

(1)检查装置的气密性,先打开a,关闭b,在A中加入水,当往下推注射器时,A中
(2)在A、B中加入澄清的石灰水,在集气瓶内放入一定量的大理石,a、b都打开,用注射器加入一定量的稀盐酸,若发现A、B中石灰水都变浑浊,则证明①大理石和稀盐酸反应一定生成了
a、较少,液面没浸没下端管口
b、较多,液面浸没了下端管口
c、很多,液面浸没了上、下端管口
在上述三种情况下
探究一 催化剂的选择
研究表明,许多金属氧化物对氯酸钾有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解 反应和反应剧烈时的温度如表所示:
温度 | 氧化铁(Fe2O3) | 氧化铝(AI2O3) | 氧化铜(CuO) | 氧化镁(MgO) |
开始反应 | 470℃ | 515℃ | 305℃ | 490℃ |
剧烈反应 | 490℃ | 540℃ | 350℃ | 545℃ |
(1)上述实验中,从温度对反应催化效果来看,最好选用
探究二 氧化铜与二氧化锰的催化效果进行比较
用如图装置进行实验,实验均以生成 25mL 气体为准,可能影响实验的因素均已忽略,相关装置和数据见下表:

实验序号 | KCIO3质量 | 催化剂质量 | 待测数据 |
① | 2.45g | / | a |
② | 2.45g | 0.51gMnO2 | b |
③ | 2.45g | 0.51gCuO | c |
(2)上述实验中的“待测数据”是
(3)若 b
探究三
氧化铜与二氧化锰的对于过氧化氢的催化效果进行比较。
小青同学用如图 1 所示的装置进行了两次实验,在试管中分别加入等质量的氧化铜和二氧化锰,分别将注射器内盛有的双氧水缓慢注入试管中,利用注射器收集氧气,收集到氧气的体积和时间的关系如图 2 所示。

(4)实验中造成 U 形管内红墨水液面左低右高的可能原因是
(5)通过图像 2 除了能得出二氧化锰催化效果比氧化铜好,还能得出的结论是
(6)由氧化铜催化的反应,t1-t2时间段反应速率逐渐变慢,原因是
【推荐2】稻草秸秆中含有大量的纤维素,通过预处理可以制备纤维素,用于造纸行业。过氧化氢溶液是一种理想的无污染漂白剂。某实验小组对影响过氧化氢漂白稻草纤维素效果的因素进行了探究。
查阅资料:漂白过程中,如果过氧化氢的分解不受控制,会导致无效分解,因此漂白前先在体系中加入3%的硅酸钠溶液为稳定剂,防止无效分解。
进行实验:
实验1:将稻草纤维素进行1次漂白
将预处理后的稻草纤维素与过氧化氢溶液混合,加入质量分数为3%的硅酸钠溶液,再加入质量分数为6%的氢氧化钠溶液调节初始pH值为10~11,保持温度70~75℃,反应时间90分钟,过滤,水洗至中性,45℃烘干,测定其白度。
实验序号 | 稻草纤维素与液体固液比 | 过氧化氢溶液质量分数 | 硅酸钠溶液与过氧化氢溶液的体积比 | 白度 |
1-1 | 1:5 | 5% | 0.5:1 | 36.5 |
1-2 | 1:8 | 5% | 0.5:1 | 46.9 |
1-3 | 1:10 | 5% | 0.5:1 | 52.4 |
实验2:将稻草纤维素进行二段漂白
首先进行第一段漂白:将预处理后的纤维素与质量分数为3%的过氧化氢溶液混合,加入质量分数为3%的硅酸钠溶液,再加入质量分数为6%的氢氧化钠溶液调节初始pH值为10~11,保持温度70~75℃,反应时间60分钟。
然后进行第二段漂白:经过第一段漂白后的纤维素与过氧化氢溶液混合,接着重复实验1的步骤。记录第二段漂白实验结果如下:
实验序号 | 稻草纤维素与液体固液比 | 过氧化氢溶液质量分数 | 硅酸钠溶液与过氧化氢溶液的体积比 | 白度 |
2-1 | 1:5 | 5% | 0.5:1 | 56.9 |
2-2 | 1:8 | 5% | 0.5:1 | 63.3 |
2-3 | 1:10 | 5% | 0.5:1 | 74.3 |
2-4 | 1:10 | 5% | 0 | 37.3 |
2-5 | a | 5% | 0.25:1 | 54.6 |
2-6 | 1:10 | 5% | 0.75:1 | 72.5 |
2-7 | 1:10 | 5% | 1:1 | 72.1 |
解释与结论:
(1)过氧化氢不稳定,易分解,发生反应的化学方程式
(2)实验2中,表格内a处应该填入的数据是
(3)依据实验1-1至1-3,可以得出的结论是
(4)根据实验结果可知,过氧化氢漂白稻草纤维素的最佳条件是:质量分数为3%的硅酸钠溶液与过氧化氢体积比为
反思与评价:
(5)依据实验数据,不能得出“稻草纤维素与液体固液比相同时,分别用3%和5%的过氧化氢溶液进行两段漂白时,质量分数为3%的硅酸钠溶液与过氧化氢溶液的体积比越大,漂白效果越好”的结论,其证据是

【实验原理】锥形瓶中发生反应的化学反应式为
【实验步骤】
| 实验步骤 | 实验现象 |
| ①保持弹簧夹关闭,将纱布袋伸入双氧水中 | 木炭不燃烧 |
| ②提起纱布袋,打开弹簧夹,挤压氮气袋 | 目的是 |
| ③关闭弹簧夹,点燃酒精灯 | 木炭不燃烧 |
| ④保持酒精灯燃烧,再将纱布袋伸入双氧水中 | 木炭立即燃烧,澄清石灰水变浑浊 |
| 对比 | 结论 |
| 步骤 | 说明木炭燃烧需要氧气助燃 |
| 步骤 | 说明木炭燃烧需要温度达可燃物着火点 |
小兵发现将布袋中二氧化锰换为氧化铁也能较快地产生氧气,若要证明它能作该反应的催化剂还需补做的实验有
①测量反应前后氧化铁质量是否不变 ②检验氧化铁物理性质是否不变
③检验氧化铁化学性质是否不变 ④观察能否改变反应速率



