回答下列问题。
(1)“侯氏制碱法”制备Na2CO3的流程如下。
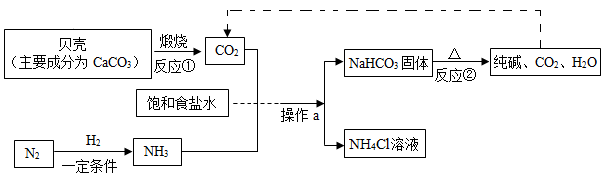
①反应②的化学方程式是___ 。
②操作a的名称是__ ,实验室进行此操作所需的主要玻璃仪器有烧杯、玻璃棒和____ 。
③流程图中能循环利用的物质是_ (填化学式) ,副产品为_ ( 填化学式)。
(2)实验室制备纯碱( Na2CO3 )的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30~35°C,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体。
四种盐在不同温度下的溶解度表( g/100g水)
①反应温度需要控制在30~ 35°C ,原因是__ 。为控制此温度,通常采取的加热方法为___ 。
②保温30分钟,静置后只析出NaHCO3晶体的原因__ 。
(1)“侯氏制碱法”制备Na2CO3的流程如下。

①反应②的化学方程式是
②操作a的名称是
③流程图中能循环利用的物质是
(2)实验室制备纯碱( Na2CO3 )的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30~35°C,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体。
四种盐在不同温度下的溶解度表( g/100g水)
| 温度 溶解度 | 0°C | 10° C | 20° C | 30° C | 40° C | 50° C | 60°C | 100°C |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | 一 | 一 | 一 | 一 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | 一 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
②保温30分钟,静置后只析出NaHCO3晶体的原因
更新时间:2020-05-03 09:44:07
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】小红带着化学兴趣活动小组以粗盐(主要成分是NaC1含少量泥沙、CaCl2、MgCl2)为原料,模拟生产氯气和氢氧化钠,实验操作流程如下:

(1)试剂A与试剂B的组合为______ (填序号);
①KOH ②NaOH ③K2CO3④Na2CO3
(2)操作A的名称是______ ,实验中玻璃棒的作用是______ 。
(3)模拟生产流程中Mg元素必须转化成______ (填化学式)才能完全除去:
(4)已知20℃时,NaC1的溶解度为36.0g。下列说法正确的是______ 。(填字母)
a.可用冷却海水的方法获取大量粗盐
b.加入盐酸是为了使溶液的pH不断增大
c.20℃时,电解200gNaCl饱和溶液中含有72.0gNaCl
d.电解NaC1溶液的化学方程式为

(1)试剂A与试剂B的组合为
①KOH ②NaOH ③K2CO3④Na2CO3
(2)操作A的名称是
(3)模拟生产流程中Mg元素必须转化成
(4)已知20℃时,NaC1的溶解度为36.0g。下列说法正确的是
a.可用冷却海水的方法获取大量粗盐
b.加入盐酸是为了使溶液的pH不断增大
c.20℃时,电解200gNaCl饱和溶液中含有72.0gNaCl
d.电解NaC1溶液的化学方程式为

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】随着手机电脑的广泛使用,现代社会电子垃圾越来越多,为了节约资源,可从废线路板中提炼贵重金属和制备硫酸铜晶体,其中一种工艺流程如图:

【查阅资料】在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子;Cu2(OH)2CO3固体是铜锈的主要成分,不溶于水,具有碱与碳酸盐的性质,能与酸反应。
(1)写出铝与稀硫酸反应的化学方程式___________ 。
(2)提炼出的贵重金属可制作奖牌,其成分是___________ 。
(3)流程中“调节pH”其主要目的是除去滤液中___________ (填离子符号)。如果需要调节pH=5.4,则适宜使用下列试剂为___________ (填序号,下同)。
A.CuO B.NaOH溶液 C.KOH溶液 D.Cu2(OH)2CO3
(4)得到的CuSO4晶体可能会含有硫酸,以下最适宜的洗涤液为___________。

【查阅资料】在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子;Cu2(OH)2CO3固体是铜锈的主要成分,不溶于水,具有碱与碳酸盐的性质,能与酸反应。
(1)写出铝与稀硫酸反应的化学方程式
(2)提炼出的贵重金属可制作奖牌,其成分是
(3)流程中“调节pH”其主要目的是除去滤液中
A.CuO B.NaOH溶液 C.KOH溶液 D.Cu2(OH)2CO3
(4)得到的CuSO4晶体可能会含有硫酸,以下最适宜的洗涤液为___________。
| A.蒸馏水 | B.饱和CuSO4溶液 |
| C.饱和NaOH溶液 | D.饱和BaCl2溶液 |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】某化学兴趣小组用锌、硫酸、氢氧化钙、硫酸铜和碳酸钠五种物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生化学反应。其中B与C反应产生的气体是光合作用的原料之一,E物质的溶液呈蓝色。
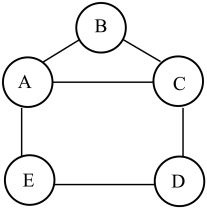
(1)写出D和E的化学式:D_________ ,E_______ 。
(2)B物质的俗称是_________ ,请写出C物质的一种用途_________ 。
(3)D与E的反应所属基本反应类型为__________ 。
(4)按游戏规则,下列能替代A物质的是_____ (填序号)。
①银 ②氢氧化钡 ③氯化钡 ④氧化铜

(1)写出D和E的化学式:D
(2)B物质的俗称是
(3)D与E的反应所属基本反应类型为
(4)按游戏规则,下列能替代A物质的是
①银 ②氢氧化钡 ③氯化钡 ④氧化铜
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】我国化学家侯德榜改进了国外的纯碱生产工艺,生产流程可简要表示如下:

(1)写出纯碱的其中一种用途:___________________ 。
(2)写出步骤③反应的化学方程式:___________________ ;基本反应类型属于________ 反应。
(3)上述工艺流程中_________ 可循环使用,其优点是减缓温室效应和 ___________________ 。
(4)操作I的名称是_____________ ;玻璃棒在该操作中的作用是_________ 。
(5)工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气和氯气,该反应的化学方程式为:_________

(1)写出纯碱的其中一种用途:
(2)写出步骤③反应的化学方程式:
(3)上述工艺流程中
(4)操作I的名称是
(5)工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气和氯气,该反应的化学方程式为:
您最近一年使用:0次
【推荐2】海洋中蕴含着丰富的资源,人们可以从海水中获取很多物质。
(1)海水淡化是解决淡水资源不足的重要方法。下列方法中,可以使海水淡化的是_____ (填字母序号).A.沉降B.过滤C.吸附 D.蒸馏
(2)利用海水制取纯碱和金属镁的流程如图所示,试回答问题:
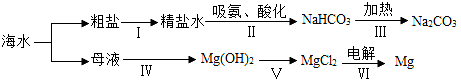
①粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质:A.适量的盐酸B.稍过量的Na2CO3溶液C.稍过量的Ba(OH)2溶液,利用过滤等操作进行除杂,则加入这三种物质的先后顺序为_____ (填字母序号),纯减属于_____ (填“酸”或“碱”或“盐”)。
②反应Ⅳ的基本反应类型是_____ 反应;第Ⅴ步反应的化学方程式为_____ 。
(1)海水淡化是解决淡水资源不足的重要方法。下列方法中,可以使海水淡化的是
(2)利用海水制取纯碱和金属镁的流程如图所示,试回答问题:

①粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质:A.适量的盐酸B.稍过量的Na2CO3溶液C.稍过量的Ba(OH)2溶液,利用过滤等操作进行除杂,则加入这三种物质的先后顺序为
②反应Ⅳ的基本反应类型是
您最近一年使用:0次
【推荐3】我国化学家侯德榜创立的侯氏制碱法为纯碱工业技术的发展做出了杰出的贡献。在制备纯碱的过程中涉及Na2CO3、NaCl、NH4Cl、NaHCO3等物质。请结合表格数据回答下列问题:
(1)表中三种物质中,溶解性属于可溶的物质是__________ 。
(2)在50℃时,向100g水中加入48gNa2CO3充分搅拌所得溶液质量为___________ ;保持烧杯中各物质质量不变,降温至40℃时,所得溶液溶质的质量分数会_________ (填“变小”、“不变”或“变大”)。
(3)请根据表格中数据,在下图中绘制出碳酸钠的溶解度曲线。
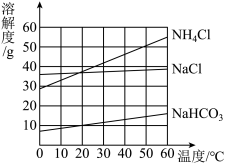
__________
(4)根据溶解度曲线回答下列问题:
①60℃时,向等质量的上述四种 固体物质中分别加水配成饱和溶液,所得溶液质量由大到小的顺序是_____________________________ 。
②侯氏制碱法的关键步骤是:先向饱和食盐水中通入氨气,制成饱和氨盐水,氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,其化学方程式为NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3。请问生成的碳酸氢钠和氯化铵,哪种物质首先析出______________ ,理由是_________________ 。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | Na2CO3 | 7 | 12.2 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
| NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | |
(2)在50℃时,向100g水中加入48gNa2CO3充分搅拌所得溶液质量为
(3)请根据表格中数据,在下图中绘制出碳酸钠的溶解度曲线。

(4)根据溶解度曲线回答下列问题:
①60℃时,向等质量的上述
②侯氏制碱法的关键步骤是:先向饱和食盐水中通入氨气,制成饱和氨盐水,氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,其化学方程式为NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3。请问生成的碳酸氢钠和氯化铵,哪种物质首先析出
您最近一年使用:0次



