化学兴趣小组对某工业废水(含有H2SO4、Na2SO4)中H2SO4的含量进行测定.甲、乙两同学各提出不同的测定方法,请回答有关问题:
(1)甲同学:取50g废水于烧杯中,逐渐滴入溶质质量分数为20%的NaOH溶液,反应过程溶液pH变化如图
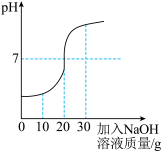
①50g废水中H2SO4的质量是多少?写出计算过程.
②当加入30g NaOH溶液时,烧杯中的溶质为 (填化学式).
(2)乙同学:改用BaCl2溶液代替NaOH溶液测定废水中的H2SO4的含量,结果可能会 (填“偏高”、“偏低”、“不变”),理由是 .
(1)甲同学:取50g废水于烧杯中,逐渐滴入溶质质量分数为20%的NaOH溶液,反应过程溶液pH变化如图

①50g废水中H2SO4的质量是多少?写出计算过程.
②当加入30g NaOH溶液时,烧杯中的溶质为 (填化学式).
(2)乙同学:改用BaCl2溶液代替NaOH溶液测定废水中的H2SO4的含量,结果可能会 (填“偏高”、“偏低”、“不变”),理由是 .
更新时间:2020-05-09 16:09:45
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】盐水选种是我国古代劳动人民发明的一种巧妙的挑选种子的方法。农业生产上常用质量分数为15%—20%的氯化钠溶液来选种。
(1)要配制50kg18%的氯化钠,计算应称取氯化钠的质量_________ 。
(2)选种进行一段时间后,农技员估计溶液和溶质质量分数都有所减少,他取出70g氯化钠溶液,加入过量的AgNO3溶液,得到沉淀28.7g,通过计算确定该氯化钠溶液是否符合选种要求?(计算结果精确到0.1%)
(1)要配制50kg18%的氯化钠,计算应称取氯化钠的质量
(2)选种进行一段时间后,农技员估计溶液和溶质质量分数都有所减少,他取出70g氯化钠溶液,加入过量的AgNO3溶液,得到沉淀28.7g,通过计算确定该氯化钠溶液是否符合选种要求?(计算结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】如图是某胃药标签的部分内容。小明同学测定该药品中NaHCO3含量的过程如下:去10粒该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的PH=7时(已知药品中的其他成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5g。称 得反应后烧杯内物质的总质量为64.3g。

请计算:
(1)胃药中NaHCO3的质量分数。
(2)形成NaCl不饱和溶液中溶质的质量分数。

请计算:
(1)胃药中NaHCO3的质量分数。
(2)形成NaCl不饱和溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
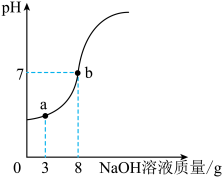
【推荐1】实验室欲测定一瓶标签破损的稀盐酸的溶质质量分数。现取10g稀盐酸样品,将5%的氢氧化钠溶液逐滴加入样品中,边加边搅拌,随着氢氧化钠溶液加入,溶液的pH的变化如图所示。

试回答:
(1)a点溶液中的溶质有______ (填化学式)。
(2)当pH=7时,消耗氢氧化钠溶液中溶质NaOH的质量为_____ 。
(3)计算该盐酸样品中溶质的质量分数(写出计算过程,结果保留一位小数)。

试回答:
(1)a点溶液中的溶质有
(2)当pH=7时,消耗氢氧化钠溶液中溶质NaOH的质量为
(3)计算该盐酸样品中溶质的质量分数(写出计算过程,结果保留一位小数)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】取40g氢氧化钠溶液于烧杯中,将73g溶质质量分数为10%的稀盐酸倒入其中,二者恰好完全反应,求反应后所得溶液的溶质质量分数?(最后结果保留整数部分)
您最近一年使用:0次