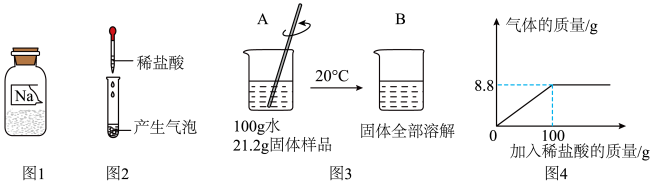
实验室有一瓶标签残损的白色固体粉末,已知其可能是 NaCl、Na2CO3、NaHCO3 三种物质中的一种,小路同学想通过实验的方法来确定其成分组成。其实步骤及现象如图1、2、3所示:(已知:20℃时,碳酸钠的溶解度为 21.8g,碳酸氢钠的溶解度为 9.6g。)
根据上述信息,是回答下列问题
(1)由图2可推知,该白色固体不是 。
(2)由图3可推知,该白色固体是 ,理由为 。
(3)利用烧杯B中的溶液可测定某稀盐酸的溶质质量分数,测得反应过程中某些量的数据关系,如图4所示:请你根据化学方程式,写出具体计算过程(计算结果精确到 0.1%)。

根据上述信息,是回答下列问题
(1)由图2可推知,该白色固体不是 。
(2)由图3可推知,该白色固体是 ,理由为 。
(3)利用烧杯B中的溶液可测定某稀盐酸的溶质质量分数,测得反应过程中某些量的数据关系,如图4所示:请你根据化学方程式,写出具体计算过程(计算结果精确到 0.1%)。
更新时间:2020-05-21 11:00:58
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】小红为了测定如图的钙片中碳酸钙的含量标注是否属实,她取出5片钙片(每片2.5克),研碎后放入烧杯中,把30g稀盐酸分3次加入烧杯中进行反应(假定钙片其它成分不与盐酸反应),每次充分反应后得到的实验数据如表:
(1)碳酸钙中碳元素和氧元素的质量比为_______ 。
(2)5片钙片完全反应可生成二氧化碳的质量为_______ 。
(3)钙片中碳酸钙的含量标注是否属实?(写出计算过程)
| XX钙片 【主要成分】碳酸钙(CaCO3) 【功效成分】每片含碳酸钙≥1.2g 【用法用量】每日2片,嚼食 【适应人群】需要补钙者 | |||
| 实验编号 | 1 | 2 | 3 |
| 稀盐酸的用量 | 10g | 20g | 30g |
| 二氧化碳的质量 | 1.1g | 2.2g | 2.75g |
(1)碳酸钙中碳元素和氧元素的质量比为
(2)5片钙片完全反应可生成二氧化碳的质量为
(3)钙片中碳酸钙的含量标注是否属实?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】用图1所示的装置制取二氧化碳并测定石灰石中碳酸钙的质量,将稀盐酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算:

(1)生成二氧化碳气体的质量为_____;
(2)计算石灰石样品中碳酸钙的质量_____;

(1)生成二氧化碳气体的质量为_____;
(2)计算石灰石样品中碳酸钙的质量_____;
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在20℃时,Ca(OH)2的溶解度是0.17g,问此温度下将1g Ca(OH)2固体放入200g水中,充分溶解后,所得溶液的溶质质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐2】如图是某同学在厨房里看到的食用纯碱(主要成分是Na2CO3)包装袋信息,他带了一包食用纯碱到学校实验室。
(1)为测定室温下Na2CO3的溶解度,在编号为A、B、C、D的四个烧杯中各加入室温下的水100g,并分别加入取自实验室的Na2CO3固体,搅拌至充分溶解,实验数据记录如表:

分析上述数据,烧杯编号为CD中的溶液是饱和溶液,室温下,Na2CO3的溶解度是_____ 。
(2)为确定食用纯碱的纯度,称取自带的食用纯碱5.4g放入烧杯中,再滴加盐酸至刚好完全反应,共用去稀盐酸25g,得溶质质量为28.2g(杂质溶于水且与盐酸不反应),通过计算判断该食用纯碱中碳酸钠的质量分数是否与包装袋信息相符。(计算结果精确到0.1%)

(1)为测定室温下Na2CO3的溶解度,在编号为A、B、C、D的四个烧杯中各加入室温下的水100g,并分别加入取自实验室的Na2CO3固体,搅拌至充分溶解,实验数据记录如表:

分析上述数据,烧杯编号为CD中的溶液是饱和溶液,室温下,Na2CO3的溶解度是
(2)为确定食用纯碱的纯度,称取自带的食用纯碱5.4g放入烧杯中,再滴加盐酸至刚好完全反应,共用去稀盐酸25g,得溶质质量为28.2g(杂质溶于水且与盐酸不反应),通过计算判断该食用纯碱中碳酸钠的质量分数是否与包装袋信息相符。(计算结果精确到0.1%)

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】请回答下列问题。
(1)积极应对气候变化,展现大国担当,中国向世界宣布了 2030 年前实现“碳达峰”、2060 年前实现“碳中和”的国家目标。“碳达峰”是指国家整体二氧化碳气体排放量达到峰值。有研究表明,当前全球每年人为向大气排放二氧化碳 420 亿吨,在这些二氧化碳中含碳元素的质量为多少亿吨?(写出计算过程,计算结果精确至 0.1 亿吨)
(2)20℃时,向 3 个盛有 100 克水的烧杯中,分别加入一定质量的氯化钠,并充分溶解。根据下表实验数据,回答:
①实验所得 3 杯溶液中,属于不饱和溶液的是_______ (填实验编号)。
②求溶液 C 的溶质质量分数_______ 。(写出计算过程,计算结果精确至 0.1%)。
(1)积极应对气候变化,展现大国担当,中国向世界宣布了 2030 年前实现“碳达峰”、2060 年前实现“碳中和”的国家目标。“碳达峰”是指国家整体二氧化碳气体排放量达到峰值。有研究表明,当前全球每年人为向大气排放二氧化碳 420 亿吨,在这些二氧化碳中含碳元素的质量为多少亿吨?(写出计算过程,计算结果精确至 0.1 亿吨)
(2)20℃时,向 3 个盛有 100 克水的烧杯中,分别加入一定质量的氯化钠,并充分溶解。根据下表实验数据,回答:
| 实验编号 | A | B | C |
| 加入氯化钠的质量(克) | 20 | 36 | 50 |
| 溶液质量(克) | 120 | 136 | 136 |
①实验所得 3 杯溶液中,属于不饱和溶液的是
②求溶液 C 的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】用侯氏制碱法制得的纯碱中含有一定量的氯化钠,现称取只含氯化钠杂质的纯碱样品33.0g放入盛有130.0g稀盐酸的烧杯中,恰好完全反应,反应后溶液的质量为149.8g。请计算:
(1)产生二氧化碳的质量为____________;
(2)样品中碳酸钠的质量分数。(写出计算过程,结果保留一位小数)
(1)产生二氧化碳的质量为____________;
(2)样品中碳酸钠的质量分数。(写出计算过程,结果保留一位小数)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】厨房中有一瓶纯碱固体,其中混有少量的氯化钠晶体。现取该固体样品12.6g,加入128.8g稀盐酸恰好完全反应,且无固体剩余,得到溶液的质量为137g。计算:
(1)恰好完全反应时产生的二氧化碳质量为_______ g。
(2)恰好完全反应时所得溶液的溶质质量分数______ 。
(温颦提示:反应化学方程式为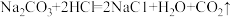 )
)
(1)恰好完全反应时产生的二氧化碳质量为
(2)恰好完全反应时所得溶液的溶质质量分数
(温颦提示:反应化学方程式为
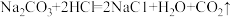 )
)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】实验室现有某铜锌混合物,为了探究其组成,某同学取 200g 9.8%的稀硫酸进行了如下实验:

请根据要求回答问题:
(1)请写出实验中发生反应的化学方程式_______________________;
(2)请写出求解第一步参加反应的固体物质质量( )的比例式______________________;
)的比例式______________________;
(3)滤渣 b 的质量为__________________;
(4)原固体中锌的质量分数为______________;
(5)向最终所得溶液中加入 17.4g 的水,则 C 中溶液的溶质质量分数为______________。

请根据要求回答问题:
(1)请写出实验中发生反应的化学方程式_______________________;
(2)请写出求解第一步参加反应的固体物质质量(
 )的比例式______________________;
)的比例式______________________;(3)滤渣 b 的质量为__________________;
(4)原固体中锌的质量分数为______________;
(5)向最终所得溶液中加入 17.4g 的水,则 C 中溶液的溶质质量分数为______________。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】维C泡腾片是一种常见的补充维生素C的保健品.某品牌维C泡腾片(以下称“本品”)的主要成分如图1所示.已知:本品放入蒸馏水中发生的反应为:H3C6H5O2+3NaHCO3═Na3C6H5O2+3CO2↑+3 (填化学式).为测定该维C泡腾片中碳酸氢钠质量分数,某化学兴趣小组称量相关实验用品质量,将本品一片投入蒸馏水中,待不再产生气体后,称量锥形瓶及瓶内所有物质的总质量.装置如图2所示.相关数据如下表:
请根据以上数据计算本品中碳酸氢钠的质量分数(写出计算过程,结果精确到0.1%).

| 物品 | 反应前 | 反应后 | ||
| 锥形瓶 | 蒸馏水 | 维C泡腾片 | 锥形瓶及瓶内所有物质 | |
| 质量/g | 71.75 | 50.00 | 4.00 | 125.53 |
请根据以上数据计算本品中碳酸氢钠的质量分数(写出计算过程,结果精确到0.1%).

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】为测定某CuSO4溶液中溶质的质量分数,取150gCuSO4溶液,平均分为三份,每一份样品均按如图所示进行实验,实验数据见下表。请计算:
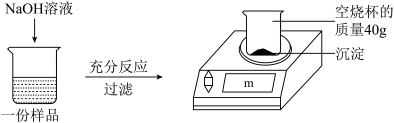
(1)50gCuSO4溶液完全反应时,所得沉淀的质量为___________ g。
(2)CuSO4溶液中溶质的质量分数(写出计算过程)。
(3)要证明反应后NaOH是否过量,可以向反应后所得溶液中加入___________(填字母序号)。
(4)实验3中反应后所得溶液中溶质的成分是___________ (写化学式)。
| 实验1 | 实验2 | 实验3 | |
| 样品质量/g | 50 | 50 | 50 |
| NaOH溶液质量/g | 20 | 40 | 60 |
| m/g | 44.9 | 49.8 | 49.8 |

(1)50gCuSO4溶液完全反应时,所得沉淀的质量为
(2)CuSO4溶液中溶质的质量分数(写出计算过程)。
(3)要证明反应后NaOH是否过量,可以向反应后所得溶液中加入___________(填字母序号)。
| A.氯化钡溶液 | B.稀盐酸 | C.酚酞溶液 |
您最近一年使用:0次





