今年化学实验考查内容是“配制一定溶质质量分数的氯化钠溶液”,如现在需要配制50g溶质质量分数为8%的氯化钠溶液,请回忆实验过程,回答下列问题:
I、配制溶液:
(1)计算:配制50g溶质质量分数为8%的氯化钠溶液需要氯化钠_____ g,水_____ mL。
(2)称量量取:用托盘天平称量所需的氯化钠时,发现天平的指针偏向左盘,应_____ 。
A增加适量氯化钠固体
B减少适量氯化钠固体
C调节平衡螺母
(3)溶解:将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是_____ 。
(4)装瓶并贴上标签。
小明同学所贴标签有不妥之处,如图所示,请在右侧的空白标签上填写正确内容_____ ;

(5)若配制所得的氯化钠溶液中氯化钠的质量分数偏小,可能的原因是_____ 。
A用量筒量取水时俯视读数
B烧杯用蒸馏水润洗后未等晾干就配制溶液
C天平指针偏右就开始称量
D转移已配好的溶液时,有少量溶液溅出
E所用氯化钠晶体未充分干燥
F转移已称好的氯化钠固体时,部分洒落在烧杯外
(6)在实验中,老师观察到了同学们使用量筒的下列操作,其中正确的是_____ 。(填序号)
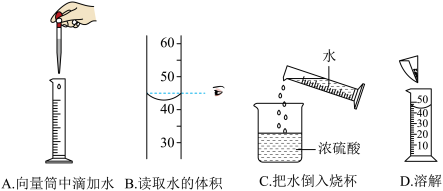
II、已知20℃时氯化钠的溶解度为36g,将该50g溶液转化为20℃的氯化钠饱和溶液,最简单的方法是_____ 。(列式计算说明)
Ⅲ、电解饱和食盐水可以得到多种化工产品,主要过程如下:

①气体A是密度最小的气体,该气体的名称为_____ ,写出一个由酸D转化为气体A的化学方程式_____ 。
②电解后生成的碱B的化学式为_____ ,你猜想的依据是_____ 。
I、配制溶液:
(1)计算:配制50g溶质质量分数为8%的氯化钠溶液需要氯化钠
(2)称量量取:用托盘天平称量所需的氯化钠时,发现天平的指针偏向左盘,应
A增加适量氯化钠固体
B减少适量氯化钠固体
C调节平衡螺母
(3)溶解:将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是
(4)装瓶并贴上标签。
小明同学所贴标签有不妥之处,如图所示,请在右侧的空白标签上填写正确内容

(5)若配制所得的氯化钠溶液中氯化钠的质量分数偏小,可能的原因是
A用量筒量取水时俯视读数
B烧杯用蒸馏水润洗后未等晾干就配制溶液
C天平指针偏右就开始称量
D转移已配好的溶液时,有少量溶液溅出
E所用氯化钠晶体未充分干燥
F转移已称好的氯化钠固体时,部分洒落在烧杯外
(6)在实验中,老师观察到了同学们使用量筒的下列操作,其中正确的是

II、已知20℃时氯化钠的溶解度为36g,将该50g溶液转化为20℃的氯化钠饱和溶液,最简单的方法是
Ⅲ、电解饱和食盐水可以得到多种化工产品,主要过程如下:

①气体A是密度最小的气体,该气体的名称为
②电解后生成的碱B的化学式为
更新时间:2020-05-19 23:22:18
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】实验室欲配制50g5%的NaCl溶液,试回答下列问题.

(1)该实验的操作步骤为__________ 、__________ 、__________ .
(2)请分别说明上图中A,B操作对实验结果的影响,并加以改正.
A操作导致所配制的溶液中溶质的质量分数________ (填“偏大”“偏小”或“不变”),改正:________ ;
B操作导致所配制的溶液中溶质的质量分数________ (填“偏大”“偏小”或“不变”),改正:_________ .
(3)托盘天平称量完毕后,砝码应__________ ,游码应__________ .

(1)该实验的操作步骤为
(2)请分别说明上图中A,B操作对实验结果的影响,并加以改正.
A操作导致所配制的溶液中溶质的质量分数
B操作导致所配制的溶液中溶质的质量分数
(3)托盘天平称量完毕后,砝码应
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】化学仪器是化学实验的条件保障.现有下列仪器:a.试管、b.集气瓶、c.锥形瓶、d.长颈漏斗、e.酒精灯、f.量筒、g.水槽、h.烧杯、i.药匙、j.导管(带胶塞),根据下列实验选取仪器(选填仪器字母)或补充仪器(填仪器名称).
(1)配制质量分数为6%的氯化钠溶液,上述仪器要用到的有_______ ,必须补充的仪器是_______________ .
(2)用高锰酸钾制取、并用排水法收集氧气时,上述仪器要用到的有:_____ ,还需要的仪器是____________ .
(1)配制质量分数为6%的氯化钠溶液,上述仪器要用到的有
(2)用高锰酸钾制取、并用排水法收集氧气时,上述仪器要用到的有:
您最近一年使用:0次
【推荐1】回答下列问题:
(1)根据所给氯化钠和碳酸钠的溶解度及溶解度曲线的信息,回答下列问题:

①t1℃时,NaCl的溶解度是_______ g。该温度时,二者_______ (填“能”或“不能”)形成溶质质量分数相同的饱和溶液。
②t2℃时,将40gNa2CO3固体加入50g水中,充分溶解后所得Na2CO3溶液中溶质与溶剂的质量比为_______ 。
③在不改变溶质质量分数的前提下,要使接近饱和的Na2CO3溶液变为饱和溶液,可采取的措施是_______ 。
(2)小明同学配制100g10%的氯化钠溶液,整个操作过程如图所示。

①图中操作错误的是_______ (填序号)。
②配制溶液的正确操作顺序为_______ (填序号)。
③经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是_______ (填序号)。
A.氯化钠固体不纯 B.用生锈的砝码称量
C.装瓶时有少量溶液洒出 D.溶解时烧杯内壁有水珠
④若要将100g10%的氯化钠溶液稀释成2%的溶液,需要另入水的质量为_______ g。
(3)气体的溶解度也有一定的变化规律。
①打开可乐瓶,溢出大量气体,由此可见,压强越小,CO2的溶解度越_______ 。
②不同温度下,氧气的溶解度随压强的变化如图所示,图中t1对应的温度40℃,则t2对应的温度范围是_______ 。

(1)根据所给氯化钠和碳酸钠的溶解度及溶解度曲线的信息,回答下列问题:

| 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| 氯化钠溶解度/g | 35 | 35.5 | 36 | 36.5 | 37 |
| 碳酸钠溶解度/g | 6 | 10 | 18 | 36.5 | 50 |
②t2℃时,将40gNa2CO3固体加入50g水中,充分溶解后所得Na2CO3溶液中溶质与溶剂的质量比为
③在不改变溶质质量分数的前提下,要使接近饱和的Na2CO3溶液变为饱和溶液,可采取的措施是
(2)小明同学配制100g10%的氯化钠溶液,整个操作过程如图所示。

①图中操作错误的是
②配制溶液的正确操作顺序为
③经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是
A.氯化钠固体不纯 B.用生锈的砝码称量
C.装瓶时有少量溶液洒出 D.溶解时烧杯内壁有水珠
④若要将100g10%的氯化钠溶液稀释成2%的溶液,需要另入水的质量为
(3)气体的溶解度也有一定的变化规律。
①打开可乐瓶,溢出大量气体,由此可见,压强越小,CO2的溶解度越
②不同温度下,氧气的溶解度随压强的变化如图所示,图中t1对应的温度40℃,则t2对应的温度范围是

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下图是配制一定质量分数的NaCl溶液的操作过程。请回答下列问题:

(1)指出图中a、b两种仪器的名称:a________ ,b________ 。
(2)写出图中的一处错误操作________ 。
(3)步骤⑤的操作为溶解,玻璃棒的作用是________ ,其操作要领是 ________ 。
(4)若上面溶解得到的NaCl溶液中还含有少量不溶性物质,则步骤⑤还需增加的操作名称是________ ;配制溶液时,量取水的时候仰视读数,若其他操作都正确,则配制的NaCl溶液的溶质质量分数 ________ (填写“偏大”“偏小”或“无影响”)

(1)指出图中a、b两种仪器的名称:a
(2)写出图中的一处错误操作
(3)步骤⑤的操作为溶解,玻璃棒的作用是
(4)若上面溶解得到的NaCl溶液中还含有少量不溶性物质,则步骤⑤还需增加的操作名称是
您最近一年使用:0次
【推荐3】回答下列问题
(1)图一是锶元素在周期表中的信息,图二是几种粒子的结构示意图。请回答:

图一中锶原子的核外电子数为________ 。图二中表示阳离子的是________ (填序号)。
(2)水是生命的源泉。为确保城市饮用水安全,目前不少自来水用氯气(Cl2)作为消毒剂,氯气通入水中发生反应的示意图如图:

上述四种物质中属于氧化物的是___ (填化学式)。C物质的水溶液能使紫色的石蕊溶液变成____ 色,取C物质的水溶液少许,向其中加入硝酸银溶液,观察到有白色沉淀产生,该过程中发生反应的化学方程式是________ 。
(3)实验室用氯化钠固体配制50克15%的氯化钠溶液,下列操作中可能导致配制氯化钠溶液的溶质质量分数偏小的是 (填字母)。
(1)图一是锶元素在周期表中的信息,图二是几种粒子的结构示意图。请回答:

图一中锶原子的核外电子数为
(2)水是生命的源泉。为确保城市饮用水安全,目前不少自来水用氯气(Cl2)作为消毒剂,氯气通入水中发生反应的示意图如图:

上述四种物质中属于氧化物的是
(3)实验室用氯化钠固体配制50克15%的氯化钠溶液,下列操作中可能导致配制氯化钠溶液的溶质质量分数偏小的是 (填字母)。
| A.称取时,将氯化钠置于托盘天平的右盘 | B.量取水时仰视读数 |
| C.用已有少量水的烧杯溶解氯化钠 | D.转移时,有少量溶液溅出 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】小莉、小晶两位同学用如下两种不同的方法,配制100g溶质质量分数为5%的氯化钠溶液。
(1)小莉用固体氯化钠和水配制溶液。
①小莉用到的玻璃仪器有量筒、胶头滴管、烧杯和________ ;
②小莉实验时应进行的步骤是计算、称量、量取、_________ 、装瓶并贴标签。
(2)小晶用溶质质量分数为20%的氯化钠溶液加水稀释。
①小晶实验时应量取水的体积是________ mL(水的密度可近似看成1g/mL)。
②若小晶量取水时俯视读数,则所配溶液的溶质质量分数_______ (填“>”“<”或“=”)5%。
(1)小莉用固体氯化钠和水配制溶液。
①小莉用到的玻璃仪器有量筒、胶头滴管、烧杯和
②小莉实验时应进行的步骤是计算、称量、量取、
(2)小晶用溶质质量分数为20%的氯化钠溶液加水稀释。
①小晶实验时应量取水的体积是
②若小晶量取水时俯视读数,则所配溶液的溶质质量分数
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是某输液瓶标签上的部分内容。
(1)要把50g这种葡萄糖溶液(密度为1g/mL)稀释为1%的溶液,需要水的质量为___________ g;
(2)若其他操作正确,量取葡萄糖溶液时俯视液面,请分析对稀释后葡萄糖溶液的浓度造成的影响。
(3)葡萄糖进入人体后在酶的催化作用下会转化为二氧化碳和水,则该反应的化学方程式___________ 。
| 葡萄糖注射液 |
| (C6H12O6) |
| 【成分】葡萄糖、水 |
| 【规格】500mL |
| 质量分数5% |
| 【性状】液体,味甜 |
| 【贮藏】密闭保存 |
(2)若其他操作正确,量取葡萄糖溶液时俯视液面,请分析对稀释后葡萄糖溶液的浓度造成的影响。
(3)葡萄糖进入人体后在酶的催化作用下会转化为二氧化碳和水,则该反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】水是宝贵的自然资源,请据图回答问题。
(1)图甲为水的净化装置,经过该装置净化后的池塘水能否直接饮用?___ 。
(2)图乙是电解水的简易装置,由图可知,甲试管中产生的气体是___ 。

(3)为加快水的电解速度,常用较稀的氢氧化钠溶液来代替水。现欲配制200g溶质质量分数为8%的氢氧化钠溶液,过程如下:
①计算:氢氧化钠的质量和所需水的体积。
②称量:用天平称量所需的氢氧化钠,在称量过程中,发现天平指针向右偏,接下来小明该如何操作?____ ,再用量筒量取所需的水。
③溶解:溶解氢氧化钠时要用玻璃棒不断搅拌,加速溶解。
④反思:下列哪项不当操作可能会导致所得溶液溶质质量分数偏小的选项有哪些?____
A 氢氧化钠中有杂质 B 称量时使用了生锈的砝码
C 用量筒量取水时,仰视读数 D 配制完成后移取液体时有部分溅出
(1)图甲为水的净化装置,经过该装置净化后的池塘水能否直接饮用?
(2)图乙是电解水的简易装置,由图可知,甲试管中产生的气体是

(3)为加快水的电解速度,常用较稀的氢氧化钠溶液来代替水。现欲配制200g溶质质量分数为8%的氢氧化钠溶液,过程如下:
①计算:氢氧化钠的质量和所需水的体积。
②称量:用天平称量所需的氢氧化钠,在称量过程中,发现天平指针向右偏,接下来小明该如何操作?
③溶解:溶解氢氧化钠时要用玻璃棒不断搅拌,加速溶解。
④反思:下列哪项不当操作可能会导致所得溶液溶质质量分数偏小的选项有哪些?
A 氢氧化钠中有杂质 B 称量时使用了生锈的砝码
C 用量筒量取水时,仰视读数 D 配制完成后移取液体时有部分溅出
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】食盐是一种重要的化工原料,可以调味,还可用于农业生产选种。
(1)要配制100g溶质质量分数为16.5%的NaCl溶液,需食盐多少_______ 克;
(2)称量食盐时,若天平向左偏,我们应该 ;
(3)如果若用托盘天平称量食盐时,食盐放在右盘,砝码放在左盘(1g以下用游码),所配制溶液中的质量分数_______ (填“偏大”“不变”“偏小”)
(1)要配制100g溶质质量分数为16.5%的NaCl溶液,需食盐多少
(2)称量食盐时,若天平向左偏,我们应该 ;
| A.调节平衡螺母 | B.增加砝码 | C.减少药品 | D.移动游码 |
您最近一年使用:0次
【推荐2】将20克NaOH固体完全溶解在80毫升水中(水的密度为1g/cm3),所配溶液中溶质的质量分数为_______ 。某同学在配制过程中,量取水时仰视读数,其所配氢氧化钠溶液中溶质的质量分数将_______ (填“偏大”或“偏小”),另一位同学称取NaOH时,由于操作不熟练,花了较长时间,那么,他所配氢氧化钠溶液中溶质的质量分数将_______ (填“偏大”或“偏小”)。小明认为他配得的溶液已变质,你认为溶液中还可能有_______ 溶质。
您最近一年使用:0次
【推荐3】水是生命之源,是人类生产生活中不可缺少的物质。我们通过一年的化学学习,进一步加深了对水的认识。请回答下列问题。
(1)生活中常用___________ 的方法降低水的硬度,并能起到消毒杀菌的作用。
(2)在农业生产中,常用溶质质量分数为3%的KNO3溶液作无土栽培的营养液,配制100kg该营养液需要水的质量是___________ kg。
(3)水是常见的溶剂,如图是a、b、c三种固体物质在水中的溶解度曲线,回答下列问题:

①t1℃时,a的溶解度___________ c的溶解度(填“<”“>”“=”)。
②t2℃时,将30g a物质放入50g水中充分溶解,所得溶液中溶质与溶剂质量比是___________ 。
③保持t2℃不变,要使接近饱和的b溶液变为饱和溶液,你采取的方法是___________ 。
(1)生活中常用
(2)在农业生产中,常用溶质质量分数为3%的KNO3溶液作无土栽培的营养液,配制100kg该营养液需要水的质量是
(3)水是常见的溶剂,如图是a、b、c三种固体物质在水中的溶解度曲线,回答下列问题:

①t1℃时,a的溶解度
②t2℃时,将30g a物质放入50g水中充分溶解,所得溶液中溶质与溶剂质量比是
③保持t2℃不变,要使接近饱和的b溶液变为饱和溶液,你采取的方法是
您最近一年使用:0次



