人类的生存和发展离不开能源和资源.
(1)家用燃料的更新过程如下:煤 液化石油气或管道煤气
液化石油气或管道煤气 天然气,下列有关家用燃料更新的理由,正确的是
天然气,下列有关家用燃料更新的理由,正确的是________ (选填字母).
A天然气属于可再生能源
B气体燃料比固体燃料利用率更高
C天然气作为燃料可避免温室效应的发生
D煤仅仅用作燃料烧掉浪费资源
(2)水是生命之源,合理利用和保护水资源是我们义不容辞的责任.
①设法除去硬水中的________ ,可以使硬水软化成软水.
②公共场所可利用“活性炭+超滤膜+紫外线”组合工艺获得直饮水,其中活性炭主要起________ 作用.
(3)海水中有大量可以利用的化学资源,其中所含的氯化镁是金属镁的重要来源之一.从海水中提取金属镁,可按如图流程进行:

①下列有关说法正确的是________ (选填字母).
A步骤I通过一步反应即可实现.
B步骤II、Ⅲ、IV的目的是从海水中提纯氯化镁
C步骤V中化学能转化为电能
D在此流程中涉及的基本反应类型有4种
②在此流程中可以循环利用的物质是________ .
(4)家中蒸馒头常用的纯碱中含有少量氯化钠,某实验小组要测定该纯碱中碳酸钠的质量分数,取12g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡,此时烧杯中没有不溶物,共消耗稀盐酸72.4g,测得反应后溶液的质量为80g.请帮助实验小组完成以下计算(写出计算过程):
①根据质量守恒定律计算生成二氧化碳的质量________
②样品中碳酸钠的质量分数是多少________ ?
(1)家用燃料的更新过程如下:煤
 液化石油气或管道煤气
液化石油气或管道煤气 天然气,下列有关家用燃料更新的理由,正确的是
天然气,下列有关家用燃料更新的理由,正确的是A天然气属于可再生能源
B气体燃料比固体燃料利用率更高
C天然气作为燃料可避免温室效应的发生
D煤仅仅用作燃料烧掉浪费资源
(2)水是生命之源,合理利用和保护水资源是我们义不容辞的责任.
①设法除去硬水中的
②公共场所可利用“活性炭+超滤膜+紫外线”组合工艺获得直饮水,其中活性炭主要起
(3)海水中有大量可以利用的化学资源,其中所含的氯化镁是金属镁的重要来源之一.从海水中提取金属镁,可按如图流程进行:

①下列有关说法正确的是
A步骤I通过一步反应即可实现.
B步骤II、Ⅲ、IV的目的是从海水中提纯氯化镁
C步骤V中化学能转化为电能
D在此流程中涉及的基本反应类型有4种
②在此流程中可以循环利用的物质是
(4)家中蒸馒头常用的纯碱中含有少量氯化钠,某实验小组要测定该纯碱中碳酸钠的质量分数,取12g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡,此时烧杯中没有不溶物,共消耗稀盐酸72.4g,测得反应后溶液的质量为80g.请帮助实验小组完成以下计算(写出计算过程):
①根据质量守恒定律计算生成二氧化碳的质量
②样品中碳酸钠的质量分数是多少
19-20九年级上·上海·课时练习 查看更多[2]
更新时间:2020-05-20 11:47:14
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
【推荐1】(1)生命的孕育和维系需要水,人类的日常生活和工农业生产离不开水。
①下列“水”中,属于纯净物的是____________ (填序号);
a.海水 b.河水 c.蒸馏水 d.井水
②水在通电条件下分解的化学方程式为_________________________ 。
③生活中可用活性炭净水器来净水,是利用了活性炭的____________ 性。活 性炭不能将硬水软化, 生活中可用____________ 的方法降低水的硬度。
(2)化学就在我们身边,它与我们的生产、生活息息相关。现有干冰、熟石灰、钛合金三 种物质。请选择适当的物质填空。
①可用于人工降雨是的_________ ;
②可用于制造人造骨的是______________ ;
③可用于改良酸 性土壤的是_______________ 。
①下列“水”中,属于纯净物的是
a.海水 b.河水 c.蒸馏水 d.井水
②水在通电条件下分解的化学方程式为
③生活中可用活性炭净水器来净水,是利用了活性炭的
(2)化学就在我们身边,它与我们的生产、生活息息相关。现有干冰、熟石灰、钛合金三 种物质。请选择适当的物质填空。
①可用于人工降雨是的
②可用于制造人造骨的是
③可用于改良酸 性土壤的是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】2015年3月22日是第二十三届“世界水日”,3月22-28日是第二十八届“中国水周”。联合国确定2015年“世界水日”的宣传主题是“水与可持续发展”(Water and Sustainable Development)。我国纪念2015年“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”。水资源的保护和合理利用已受到人们的普遍关注。请回答下列有关问题:
(1)保持水的化学性质的最小粒子是________ 。
(2)小恺家屋后刚挖了一口深井,学习化学后,他知道长期饮用硬水会对健康有害。能用_____________ 鉴别井水是否为硬水,生活中可用_____________ 的方法将硬水软化。
(3)请列举出你在生活中爱护水资源的一种做法:__________________________ 。
(1)保持水的化学性质的最小粒子是
(2)小恺家屋后刚挖了一口深井,学习化学后,他知道长期饮用硬水会对健康有害。能用
(3)请列举出你在生活中爱护水资源的一种做法:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
解题方法
【推荐1】A~F 均是初中化学常见的物质,它们之间的转化关系如图所示(反应条件及部分反应物和生成物已略去)。图中“→”表示物质间可以直接转化,“—”表示物质间可以反应。F 为温室气体,A、B、C、D 四种物质含有一种相同元素。
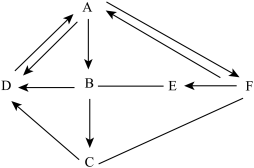
(1)F 的化学式______ 。
(2)D→A 的化学方程式______ 。

(1)F 的化学式
(2)D→A 的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】甲、乙、丙都是金属单质,且甲是世界产量最高的,B、C、E均是硝酸盐,E是蓝色溶液,F既不溶于水也不溶于盐酸,它们之间有如下图所示关系:

(1)根据上述各物质的相互关系,试写出乙、C的名称:乙______________ ,C____________ 。
(2)A溶液与B溶液反应的化学方程式:____________ 。

(1)根据上述各物质的相互关系,试写出乙、C的名称:乙
(2)A溶液与B溶液反应的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】我国提出力争在2030年前实现碳达峰,2060年前实现碳中和,彰显了负责任大国的作为与担当。为达成这一目标,一方面要减少碳排放,另一方面要尽量捕集、利用和封存不可避免的碳排放。
(1)“碳减排”。从能源结构看减排。我国近20年一次能源消费结构对比如图1。

①根据图1,2000-2020年能源消费结构中逐渐升高的是___________ 。利用天然气代替含硫煤做家庭燃料的优点是可以减少___________ 的排放。做饭时,若燃气灶的火焰呈现黄色或橙色,则需将灶具进风口_____ (填“调大”或“调小”)即可恢复正常的淡蓝色火焰。
②人类活动排放CO2的主要途径有_______________ (写一个)等。下列燃料在O2中燃烧时,不会产生CO2的是___________ (填序号)。
A 天然气B 氢气C 肼(N2H4)
③写出日常生活中你能做到的一种“低碳”行为:______________________ 。
(2)“碳捕获”。利用化学方法吸收CO2是实现“碳捕获”的方法之一。海水吸收CO2的产物是___________ 。若用石灰乳(主要成分是氢氧化钙),“捕获”CO2,反应的化学方程式为______________________ 。
(3)“碳利用”。我国科学家使用纳米纤维作催化剂实现了CO2的转化。反应原理如下图所示:

①反应前后未发生改变的微观粒子有___________ (填一种即可)。
②上述反应的化学方程式为______________________ 。
(4)“碳封存”。矿物质碳化封存的反应之一是氧化镁与CO2化合生成碳酸镁,碳酸镁的化学式为___________ 。作为参与者,除本题中的措施外,请写一条有利于实现“碳中和”的措施______________________ 。
(1)“碳减排”。从能源结构看减排。我国近20年一次能源消费结构对比如图1。

①根据图1,2000-2020年能源消费结构中逐渐升高的是
②人类活动排放CO2的主要途径有
A 天然气B 氢气C 肼(N2H4)
③写出日常生活中你能做到的一种“低碳”行为:
(2)“碳捕获”。利用化学方法吸收CO2是实现“碳捕获”的方法之一。海水吸收CO2的产物是
(3)“碳利用”。我国科学家使用纳米纤维作催化剂实现了CO2的转化。反应原理如下图所示:

①反应前后未发生改变的微观粒子有
②上述反应的化学方程式为
(4)“碳封存”。矿物质碳化封存的反应之一是氧化镁与CO2化合生成碳酸镁,碳酸镁的化学式为
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
【推荐2】能源和环境问题日益成为人们关注的焦点。
(1)常见的化石燃料有煤、石油和天然气等。天然气在空气中完全燃烧的化学方程式为:_____________________________________ 。
(2)燃煤会影响环境。下列环境问题与燃煤没有直接关系的是____ (填字母)。
A.酸雨 B.臭氧层破坏 C.温室效应 D.可吸入颗粒物增加
(3)CO2含量不断升高,使全球气候问题日趋严重。如图是CO2参与的一种“碳转化”。
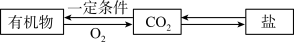
①CO2和H2在催化剂和加热条件下,可以转化为化工原料乙烯(C2H4),请将该反应的化学方程式补充完整:2CO2+6H2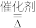 C2H4+4
C2H4+4_____ 。
②将CO2通入Na2CO3溶液中,只生成NaHCO3,该反应的化学方程式为_____________ 。
(1)常见的化石燃料有煤、石油和天然气等。天然气在空气中完全燃烧的化学方程式为:
(2)燃煤会影响环境。下列环境问题与燃煤没有直接关系的是
A.酸雨 B.臭氧层破坏 C.温室效应 D.可吸入颗粒物增加
(3)CO2含量不断升高,使全球气候问题日趋严重。如图是CO2参与的一种“碳转化”。

①CO2和H2在催化剂和加热条件下,可以转化为化工原料乙烯(C2H4),请将该反应的化学方程式补充完整:2CO2+6H2
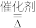 C2H4+4
C2H4+4②将CO2通入Na2CO3溶液中,只生成NaHCO3,该反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
【推荐3】近年来我国北方地区冬季常出现雾霾天气,主要原因之一是燃煤产生的烟气。燃煤产生的烟气中含有二氧化硫,直接排放会污染空气,某科研小组利用海水除去二氧化硫,其工艺流程见图:

请回答下列问题:
(1)二氧化硫对环境造成的污染是形成_____ 。
(2)为了研究脱硫率(脱硫率是已除去的二氧化硫的量占总二氧化硫量的百分比) 与温度、烟气中SO2浓度的关系,他们进行了探究实验。实验结果如下:
由表中实验数据可得出的结论是_____ 。
(3)目前,利用乙烯(C2H4)和烟气混合后在Cu+作用下除去二氧化硫,生成一种固体单质、一种能使澄清石灰水变浑浊的气体和一种液体。
①完成下列化学方程式:C2H4+SO2+2O2═_____ 。
②反应过程中Cu+的作用是_____ 。

请回答下列问题:
(1)二氧化硫对环境造成的污染是形成
(2)为了研究脱硫率(脱硫率是已除去的二氧化硫的量占总二氧化硫量的百分比) 与温度、烟气中SO2浓度的关系,他们进行了探究实验。实验结果如下:
| 实验序号 | 温度/℃ | 烟气中SO2浓度/10﹣2g•L﹣1 | 脱硫率 |
| Ⅰ | 23 | 2.5% | 99.5 |
| Ⅱ | 23 | 3.2% | 97.1 |
| Ⅲ | 40 | 2.5% | 94.3 |
(3)目前,利用乙烯(C2H4)和烟气混合后在Cu+作用下除去二氧化硫,生成一种固体单质、一种能使澄清石灰水变浑浊的气体和一种液体。
①完成下列化学方程式:C2H4+SO2+2O2═
②反应过程中Cu+的作用是
您最近一年使用:0次
【推荐1】海洋是一个聚宝盆。
(1)利用海水提取粗盐的过程如图所示:

一定质量的海水,通过贮水池引入到蒸发池,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量会___________ (填“增大”“不变”或“减小”)。
(2)实验室除去粗盐中难溶性杂质的主要实验步骤有:

Ⅰ、溶解;Ⅱ、过滤;Ⅲ、___________ (填操作名称)。上述三个步骤中,用到的可以直接加热的仪器(玻璃棒除外)是___________ 。常温下,粗盐溶解的步骤如图1所示,从节约能源和提高产率的角度分析,图1中所需水的最佳体积是___________ mL。(提示:水的密度为1g/mL;常温下,100g氯化钠饱和溶液中含有氯化钠25g)
(3)氯化钠溶液在一定条件下能制备84消毒液,其有效氯含量越高消毒效果越好。
实验1:20℃,钛电极间距1cm,电压10V,1L氯化钠溶液,通电1小时。
实验2:1L4%氯化钠溶液,通电1小时。
①设计实验2﹣1、2﹣4、2﹣5的目的是___________ 。
②请根据实验2的数据,写出一条有效氯含量随影响因素的变化规律:___________ 。
③能证明电压对有效氯含量有影响的实验是___________ (填实验编号)。
(4)从海水中提取金属镁,可按如图流程进行:

①下列说法正确的是___________ (填字母)。
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C.步骤Ⅴ中化学能转化为电能
D.步骤Ⅱ、Ⅲ都发生了中和反应
②该流程中采取的一种降低成本且减少污染的措施是___________ 。
(1)利用海水提取粗盐的过程如图所示:

一定质量的海水,通过贮水池引入到蒸发池,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量会
(2)实验室除去粗盐中难溶性杂质的主要实验步骤有:

Ⅰ、溶解;Ⅱ、过滤;Ⅲ、
(3)氯化钠溶液在一定条件下能制备84消毒液,其有效氯含量越高消毒效果越好。
实验1:20℃,钛电极间距1cm,电压10V,1L氯化钠溶液,通电1小时。
| 实验编号 | 1﹣1 | 1﹣2 | 1﹣3 | 1﹣4 | 1﹣5 | 1﹣6 |
| NaCl溶液浓度 | 1% | 2% | 3% | 4% | 5% | 6% |
| 有效氯含量/(g/L) | 3.5 | 3.8 | 3.9 | 4 | 3.9 | 3.7 |
| 实验编号 | 温度/℃ | 电压/V | 钛电极间距/cm | 有效氯含量/(g/L) |
| 2﹣1 | 20 | 20 | 1 | 8.4 |
| 2﹣2 | 30 | 20 | 1 | 8.0 |
| 2﹣3 | 40 | 20 | 1 | 7.8 |
| 2﹣4 | 20 | 20 | 0.5 | 8.2 |
| 2﹣5 | 20 | 20 | 1.5 | 8 |
②请根据实验2的数据,写出一条有效氯含量随影响因素的变化规律:
③能证明电压对有效氯含量有影响的实验是
(4)从海水中提取金属镁,可按如图流程进行:

①下列说法正确的是
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C.步骤Ⅴ中化学能转化为电能
D.步骤Ⅱ、Ⅲ都发生了中和反应
②该流程中采取的一种降低成本且减少污染的措施是
您最近一年使用:0次
【推荐2】某企业将海水综合利用与联合制碱法结合,实现资源利用最大化。
①母液中含有大量MgCl2、少量的CaCl2等。
②NaHCO3受热易分解。
③氨气极易溶于水,二氧化碳能溶于水。
(1)从海水中获得粗盐的方法是______ (填“蒸发结晶”或“降温结晶”),得到的母液是氯化钠的______ (填“饱和”或“不饱和”)溶液。
(2)向饱和食盐水中先通足量的NH3,再缓缓通入CO2的目的是______ 。
(3)制备NaHCO3固体过程中采用水浴加热,温度维持在42℃左右。温度过低,反应速率太慢,不利于晶体析出,温度也不宜过高,原因是______ 、______ 。
(4)向母液中加入石灰乳,生成氢氧化镁的化学方程式为______ ;工业上常常选用石灰乳而不选用澄清石灰水的理由是______ ,实际工业生产中,部分企业选择价格较高的NaOH进行沉镁而不选用石灰乳的理由是______ 。
(5)为了尽可能除尽Ca2+,同时减少Mg2+的损耗,某同学设计了利用Na2CO3做脱钙剂,控制不同反应条件的实验,结果如下:(A表示Na2CO3与CaCl2的质量比)
以去除钙离子为核心,综合考虑多方面因素,你认为最优的方案是______ (填实验序号),理由是______ 。

①母液中含有大量MgCl2、少量的CaCl2等。
②NaHCO3受热易分解。
③氨气极易溶于水,二氧化碳能溶于水。
(1)从海水中获得粗盐的方法是
(2)向饱和食盐水中先通足量的NH3,再缓缓通入CO2的目的是
(3)制备NaHCO3固体过程中采用水浴加热,温度维持在42℃左右。温度过低,反应速率太慢,不利于晶体析出,温度也不宜过高,原因是
(4)向母液中加入石灰乳,生成氢氧化镁的化学方程式为
(5)为了尽可能除尽Ca2+,同时减少Mg2+的损耗,某同学设计了利用Na2CO3做脱钙剂,控制不同反应条件的实验,结果如下:(A表示Na2CO3与CaCl2的质量比)
| 实验序号 | A | 温度/℃ | 反应时间 | 静置时间 | Ca2+去除率 | Mg2+损耗率 |
| 1 | 106.0:111 | 25 | 2min | 30 min/ | 65.8% | 7.4% |
| 2 | 106.0:111 | 30 | 4min | 60 min | 77.6% | 9.4% |
| 3 | 127.2:111 | 25 | 4min | 90min | 82.4% | 14% |
| 4 | 127.2:111 | 30 | 6min | 30min | 90.5% | 12.6% |
| 5 | 148.4:111 | 25 | 6min | 60min | 90.8% | 15.9% |
| 6 | 148.4:111 | 30 | 2min | 90min | 83.4% | 16.4% |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】我国海洋资源丰富,开发前景十分远大。
(1)中国航空工业的发展需要大国工匠精神,也需要化学知识的支持。其中“国防金属”镁是制造火箭的重要材料,目前世界上大约60%的金属镁是利用化学方法从海水(或卤水)中提取的。从海水中提取单质镁的过程如下图所示:

Ⅰ.过程①中所发生的化学反应属于_______ 反应(填“置换”“复分解”“化合”“分解”之一)
Ⅱ.过程②中加入的试剂X的名称为_______ 。
Ⅲ.下列有关海水的说法中,不正确的是_____ (选填字母序号之一)。
A海水淡化是解决淡水缺乏的重要途径之一
B.海水“晒盐”是利用蒸发结晶的方法从海水中得到食盐
C.从海水中提取单质镁步骤①、②的目的是从海水中富集提纯氯化镁
D.步骤③中化学能转化为了电能
(2)某化学兴趣小组取2.9g氢氧化镁和氯化镁的固体混合物放于烧杯中,加适量蒸馏水使之充分溶解,再向烧杯中加入 溶液,反应过程中烧杯中固体的质量与所加入
溶液,反应过程中烧杯中固体的质量与所加入 溶液的质量关系如下图所示,试回答:
溶液的质量关系如下图所示,试回答:

①当加入 溶液即图中B点时,烧杯中溶液里大量存在的阳离子是
溶液即图中B点时,烧杯中溶液里大量存在的阳离子是______ (填写离子符号),烧杯中溶液的pH_____ 7。(填“大于”“小于”“等于”之一)
②固体混合物中 的质量为
的质量为___ g。
③当加入 溶液即图中A点时,求过滤后所得固体的质量
溶液即图中A点时,求过滤后所得固体的质量_____ (列方程式计算,结果精确到0.01g)?
(1)中国航空工业的发展需要大国工匠精神,也需要化学知识的支持。其中“国防金属”镁是制造火箭的重要材料,目前世界上大约60%的金属镁是利用化学方法从海水(或卤水)中提取的。从海水中提取单质镁的过程如下图所示:

Ⅰ.过程①中所发生的化学反应属于
Ⅱ.过程②中加入的试剂X的名称为
Ⅲ.下列有关海水的说法中,不正确的是
A海水淡化是解决淡水缺乏的重要途径之一
B.海水“晒盐”是利用蒸发结晶的方法从海水中得到食盐
C.从海水中提取单质镁步骤①、②的目的是从海水中富集提纯氯化镁
D.步骤③中化学能转化为了电能
(2)某化学兴趣小组取2.9g氢氧化镁和氯化镁的固体混合物放于烧杯中,加适量蒸馏水使之充分溶解,再向烧杯中加入
 溶液,反应过程中烧杯中固体的质量与所加入
溶液,反应过程中烧杯中固体的质量与所加入 溶液的质量关系如下图所示,试回答:
溶液的质量关系如下图所示,试回答:
①当加入
 溶液即图中B点时,烧杯中溶液里大量存在的阳离子是
溶液即图中B点时,烧杯中溶液里大量存在的阳离子是②固体混合物中
 的质量为
的质量为③当加入
 溶液即图中A点时,求过滤后所得固体的质量
溶液即图中A点时,求过滤后所得固体的质量
您最近一年使用:0次




