实验室有一瓶溶质质量分数为8%的氢氧化钠溶液,使用后忘盖瓶塞,某兴趣小组同学欲探究该氢氧化钠溶液样品中溶质的成分及含量,进行如下实验探究。请你分析并计算。
【实验过程】

【实验结论】
该氢氧化钠溶液样品中含有氢氧化钠和碳酸钠。
(1)若滤液b中只含有一种阴离子,请你写出滤液a与试剂X发生反应的化学方程式_______________。
(2)请你结合上述实验数据,计算该氢氧化钠溶液样品中碳酸钠的溶质质量分数。(写出计算过程,结果精确到0.1%)
(3)该氢氧化钠溶液样品中氢氧化钠的溶质质量分数为 。
【实验过程】

【实验结论】
该氢氧化钠溶液样品中含有氢氧化钠和碳酸钠。
(1)若滤液b中只含有一种阴离子,请你写出滤液a与试剂X发生反应的化学方程式_______________。
(2)请你结合上述实验数据,计算该氢氧化钠溶液样品中碳酸钠的溶质质量分数。(写出计算过程,结果精确到0.1%)
(3)该氢氧化钠溶液样品中氢氧化钠的溶质质量分数为 。
更新时间:2020-05-21 11:24:15
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。请计算:
(1)若要清洗1000 kg的这种石油产品,需要______kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理1000 kg这种产品,可以节约多少经费?___。已知工业级的NaOH和Ca(OH)2的最新市场批发价如下表:
(3)将反应后生成的硫酸钙回收,在一定条件下加入高温硫酸盐还原菌,可以将SO42-离子转化生成H2S气体,然后用以硫酸的生产工业。不考虑整个过程中硫元素的损失,若将(2)中产生的硫酸钙全部转化,可生产H2S的质量为______kg。
(1)若要清洗1000 kg的这种石油产品,需要______kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理1000 kg这种产品,可以节约多少经费?___。已知工业级的NaOH和Ca(OH)2的最新市场批发价如下表:
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 1.00 | 6.00 |
(3)将反应后生成的硫酸钙回收,在一定条件下加入高温硫酸盐还原菌,可以将SO42-离子转化生成H2S气体,然后用以硫酸的生产工业。不考虑整个过程中硫元素的损失,若将(2)中产生的硫酸钙全部转化,可生产H2S的质量为______kg。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】我国著名化学家侯德榜先生在改进纯碱的生产技术方面曾做出了杰出的贡献。某化工厂运用“侯氏制碱法”生产的纯碱中含有少量的氯化钠,现称取只含有氯化钠杂质的纯碱样品11.4g,将其全部溶解在68.0g蒸馏水中,再加入50.0g稀盐酸,恰好完全反应并生成4.4gCO2。(Na2CO3 + 2HCl=2NaCl+ H2O + CO2↑)求:
(1)11.4g纯碱样品中碳酸钠的质量;
(2)加入的稀盐酸中溶质的质量分数;
(3)反应后所得溶液中溶质的质量分数。
(1)11.4g纯碱样品中碳酸钠的质量;
(2)加入的稀盐酸中溶质的质量分数;
(3)反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】阳春鱼产丰富,鱼骨可用于补钙和做饲料。某项目化学习小组准备用图甲实验装置测定鱼骨中的碳酸钙含量,进而测定其中钙的含量。其操作如下:
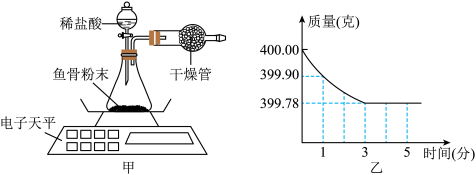
提示:假设鱼骨中只有碳酸钙与盐酸反应产生的气体;生成的二氧化碳气体全部逸出锥形瓶;空气成分对实验的影响忽略不计。
碳酸钙和盐酸反应的化学方程式为: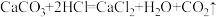 。
。
I.加入药品:在锥形瓶中加入40克鱼骨粉末,往分液漏斗中加足量的稀盐酸;
Ⅱ.记录数据:打开活塞加入稀盐酸,每隔10秒记录天平读数,并将测得的数据绘制成图(图乙)。
Ⅲ.计算:
(1)根据上述数据可知,在分钟时,实验恰好完全反应,放出气体质量为_____________ 克。
(2)根据上述实验数据计算鱼骨样品中碳酸钙的质量。(写出计算过程)
(3)鱼骨样品中Ca元素的质量分数为_______________ 。
(4)查资料得:鱼骨中钙元素的质量分数为14%-25%。而按照上述实验计算出来的结果远小于资料中的14%-25%,请你写出可能的一种原因_______________ 。

提示:假设鱼骨中只有碳酸钙与盐酸反应产生的气体;生成的二氧化碳气体全部逸出锥形瓶;空气成分对实验的影响忽略不计。
碳酸钙和盐酸反应的化学方程式为:
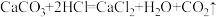 。
。I.加入药品:在锥形瓶中加入40克鱼骨粉末,往分液漏斗中加足量的稀盐酸;
Ⅱ.记录数据:打开活塞加入稀盐酸,每隔10秒记录天平读数,并将测得的数据绘制成图(图乙)。
Ⅲ.计算:
(1)根据上述数据可知,在分钟时,实验恰好完全反应,放出气体质量为
(2)根据上述实验数据计算鱼骨样品中碳酸钙的质量。(写出计算过程)
(3)鱼骨样品中Ca元素的质量分数为
(4)查资料得:鱼骨中钙元素的质量分数为14%-25%。而按照上述实验计算出来的结果远小于资料中的14%-25%,请你写出可能的一种原因
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】取一定量溶质质量分数为25%的氢氧化钠溶液,将其蒸发掉24g水后,得到溶质质量分数为40%的不饱和溶液,继续向其中加入硫酸镁溶液,恰好完全反应。过滤后,得到溶质质量分数为20%的不饱和溶液。计算:
(1)蒸发水后氢氧化钠溶液的质量。
(2)加入的硫酸镁溶液中溶质质量分数。
(1)蒸发水后氢氧化钠溶液的质量。
(2)加入的硫酸镁溶液中溶质质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某同学取20g黄铜(铜、锌合金)样品放入盛有200g稀硫酸的烧杯中,恰好完全反应,测得烧杯中剩余物质的总质量为219.8g,试计算:
(1)生成氢气的质量。___________
(2)该黄铜样品中锌的质量。____________
(3)恰好完全反应后所得溶液中溶质的质量分数(计算结果精确到0.1%)。___________
(1)生成氢气的质量。___________
(2)该黄铜样品中锌的质量。____________
(3)恰好完全反应后所得溶液中溶质的质量分数(计算结果精确到0.1%)。___________
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】小明同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究。
【提出问题】这瓶NaOH溶液变质程度如何呢?
【提出猜想】小明的猜想:NaOH溶液部分变质。
【实验探究】小明设计如下实验来验证自己的猜想,请根据表中内容填写 小明实验时的现象:
【深入研究】通过实际实验,确认这瓶放置已久的NaOH溶液部分变质。现从该瓶中取了100g 溶液,向其中逐滴加入稀盐酸,至恰好不再产生气泡时共消耗稀盐酸73g,同时产生CO2气体2.2g,此时测得溶液的pH=7。
(2)恰好反应时所得溶液的质量是_______________ g。
(3)求这瓶溶液中Na2CO3的质量分数为_________ 。( 写出计算过程)
【提出问题】这瓶NaOH溶液变质程度如何呢?
【提出猜想】小明的猜想:NaOH溶液部分变质。
【实验探究】小明设计如下实验来验证自己的猜想,请根据表中内容
| 实验步骤 | 实验现象 | 结论 |
| ①取样,滴加足量的CaCl2溶液。 | 产生白色沉淀。 | NaOH溶液部分变质。 |
| ②过滤,用pH试纸测溶液的pH。 | (1)pH |
【深入研究】通过实际实验,确认这瓶放置已久的NaOH溶液部分变质。现从该瓶中取了100g 溶液,向其中逐滴加入稀盐酸,至恰好不再产生气泡时共消耗稀盐酸73g,同时产生CO2气体2.2g,此时测得溶液的pH=7。
(2)恰好反应时所得溶液的质量是
(3)求这瓶溶液中Na2CO3的质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】下图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器。
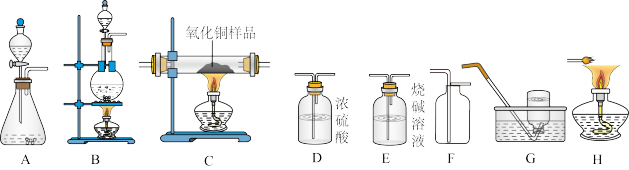
试根据题目要求,回答下列问题:
⑴请写出能用装置A制备的一种气体的化学反应方程式_____ ,该气体可选用装置 _____ 来收集(填装置序号),其选择依据是 _____ 。
⑵小颖同学欲用干燥、纯净的一氧化碳气体还原某氧化铜样品(杂质只有铜),并测定其纯度。
【查阅资料】
将草酸(H2C2O4)晶体与浓硫酸混合加热,会产生一氧化碳等气体,其反应原理为:H2C2O4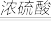 CO↑+CO2↑+H2O。
CO↑+CO2↑+H2O。
①若小颖同学选用草酸来制取CO,其发生装置她应选择_____ (填装置序号)。
【定量实验】
②小颖同学先用电子秤称取了1.00g氧化铜样品,放入装置C中的玻璃管内并组装好所有相关仪器,再将草酸分解得到的气体产物按照以下仪器的连接顺序进行实验:混合气体→D→C→E→H,最后,通过测量反应前后装置E的质量变化进行计算。(已知:CO+CuO Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是
Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是 _____ 。
③请你分析上述实验方案存在的不足之处及对应的改进方法 _____ 。
④实验改进后,小颖同学对实验所得的正确数据进行分析处理(设所发生的反应均完全进行):通过测定,当装置C中的氧化铜全部被还原后,装置E的质量增加了0.33g,则该样品中氧化铜的质量分数为_____ (结果精确至0.1%)。
⑤小黄同学提出了异议,他认为若②中实验方案不加以改进,也能正确测算出该样品中氧化铜的纯度,他的计算依据或方法为:_____ 。

试根据题目要求,回答下列问题:
⑴请写出能用装置A制备的一种气体的化学反应方程式
⑵小颖同学欲用
【查阅资料】
将草酸(H2C2O4)晶体与浓硫酸混合加热,会产生一氧化碳等气体,其反应原理为:H2C2O4
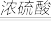 CO↑+CO2↑+H2O。
CO↑+CO2↑+H2O。①若小颖同学选用草酸来制取CO,其发生装置她应选择
【定量实验】
②小颖同学先用电子秤称取了1.00g氧化铜样品,放入装置C中的玻璃管内并组装好所有相关仪器,再将草酸分解得到的气体产物按照以下仪器的连接顺序进行实验:混合气体→D→C→E→H,最后,通过测量反应前后装置E的质量变化进行计算。(已知:CO+CuO
 Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是
Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是 ③请你分析上述实验方案存在的不足之处
④实验改进后,小颖同学对实验所得的正确数据进行分析处理(设所发生的反应均完全进行):通过测定,当装置C中的氧化铜全部被还原后,装置E的质量增加了0.33g,则该样品中氧化铜的质量分数为
⑤小黄同学提出了异议,他认为若②中实验方案不加以改进,也能正确测算出该样品中氧化铜的纯度,他的计算依据或方法为:
您最近一年使用:0次





