铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:(已知氢氧化铝能溶解在氢氧化钠溶液中,生成偏铝酸钠NaAlO2)
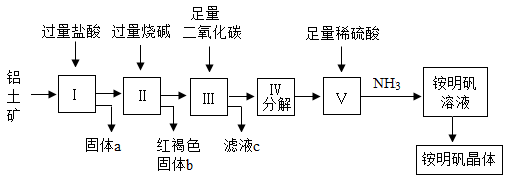
请回答下列问题:
(1)固体a的化学式为_____ ,Ⅲ中通入足量CO2气体能生成氢氧化铝和一种酸式盐。写出发生反应的化学方程式为_____ 。
(2)IV步分解指加热使氢氧化铝分解为相应的氧化物。由V制取铵明矾溶液的化学方程式为_____ ,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)_____ 、冷却结晶、过滤洗涤。
(3)以1000kg含氧化铝30.6%的铝土矿为原料制取Al2(SO4)3,需消耗含溶质质量为_____ g的98%的浓硫酸(密度1.84g·cm-1)。
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的“微粒”个数之比为1:1,则投料时铝土矿中的AI2O3和H2SO4的“微粒”个数之比为_____ 。

请回答下列问题:
(1)固体a的化学式为
(2)IV步分解指加热使氢氧化铝分解为相应的氧化物。由V制取铵明矾溶液的化学方程式为
(3)以1000kg含氧化铝30.6%的铝土矿为原料制取Al2(SO4)3,需消耗含溶质质量为
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的“微粒”个数之比为1:1,则投料时铝土矿中的AI2O3和H2SO4的“微粒”个数之比为
更新时间:2020-05-27 21:53:28
|
相似题推荐
填空与简答-流程题
|
困难
(0.15)
解题方法
【推荐1】某种干燥剂含有氧化钙、氢氧化钠和氯化钙中的两种物质。为探究其组成,化学兴趣小组取一定质量的干燥剂样品做了如下实验。
【查阅资料】稀硝酸(HNO3)具有酸的通性。
【设计实验】流程如图:

【实验分析】
(1)干燥剂样品加入水后所得的溶液显_________ (填“中性”或“酸性”或“碱性”)。
(2)生成气体B的反应的化学方程式是_________ 。
【结论与反思】
(3)若C处无沉淀,则该干燥剂的成分为_________ (写化学式)。
(4)若C处有白色沉淀生成,且沉淀质量为2.87g,则干燥剂的成分为_________ (写化学式)。写出C处生成白色沉淀的化学方程式_______________ 。
(5)该实验中,过量稀硝酸不能用过量的稀盐酸代替的原因是_________ 。
【查阅资料】稀硝酸(HNO3)具有酸的通性。
【设计实验】流程如图:

【实验分析】
(1)干燥剂样品加入水后所得的溶液显
(2)生成气体B的反应的化学方程式是
【结论与反思】
(3)若C处无沉淀,则该干燥剂的成分为
(4)若C处有白色沉淀生成,且沉淀质量为2.87g,则干燥剂的成分为
(5)该实验中,过量稀硝酸不能用过量的稀盐酸代替的原因是
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
真题
【推荐2】学习化学需要熟悉物质的性质、用途及物质间的相互转化关系。下图A一H均为初中化学常见的物质,其中A是大理石的主要成分,G是农业上常用来改良酸性土壤的一种碱的溶液,F是铁锈的主要成分。(“一”表示物质间能转化,“一”表示相连的物质能发生反应;图中部分反应物、反应条件、生成物已省略。)

(1)反应①的化学方程式是________ ,该反应过程中_______ (填“吸收”或“放出”)大量热。
(2)反应②所属基本反应类型是_______________ 反应。

(1)反应①的化学方程式是
(2)反应②所属基本反应类型是
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
【推荐3】铁及其化合物在生产生活中发挥着重要作用。
(一)铁及其化合物的应用
(1)将铁拉成铁丝等不同的形状,是利用了金属的______ 性。
(2)铁的化合物在现代更多领域发挥着重要作用。
①火星探测器发回的信息表明,火星上存在FeOOH,从而证明火星表面可能曾经存在过水,其理由为______ 。
②活性FeOOH可除去石油开采过程中的有害气体H2S,并获得S,原理如下。
FeOOH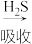 Fe2S3•H2O
Fe2S3•H2O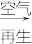 FeOOH+S
FeOOH+S
吸收过程中生成的另一种物质为氧化物,其名称为______ ,再生时发生反应的化学方程式为______ 。
(二)FeOOH的制备
用废铁屑(主要成分为Fe,含少量Fe2O3)制备FeOOH主要流程如下。
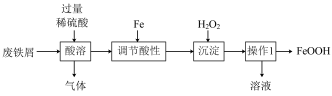
资料卡片:①Fe2O3能与稀硫酸反应,生成硫酸铁和水。
②酸溶时还发生了反应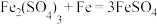 。
。
(3)酸溶时产生的气体为______ (写化学式,下同)。酸溶后所得溶液中溶质为______ 。
(4)沉淀过程中发生的反应为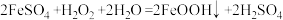 。操作1的名称是
。操作1的名称是______ ;该流程中可以循环利用的物质是______ 。
(一)铁及其化合物的应用
(1)将铁拉成铁丝等不同的形状,是利用了金属的
(2)铁的化合物在现代更多领域发挥着重要作用。
①火星探测器发回的信息表明,火星上存在FeOOH,从而证明火星表面可能曾经存在过水,其理由为
②活性FeOOH可除去石油开采过程中的有害气体H2S,并获得S,原理如下。
FeOOH
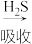 Fe2S3•H2O
Fe2S3•H2O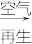 FeOOH+S
FeOOH+S吸收过程中生成的另一种物质为氧化物,其名称为
(二)FeOOH的制备
用废铁屑(主要成分为Fe,含少量Fe2O3)制备FeOOH主要流程如下。

资料卡片:①Fe2O3能与稀硫酸反应,生成硫酸铁和水。
②酸溶时还发生了反应
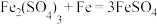 。
。(3)酸溶时产生的气体为
(4)沉淀过程中发生的反应为
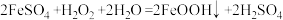 。操作1的名称是
。操作1的名称是
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐1】某可燃性气体可能是CO、H2、CH4中的一种或两种,为探究其成分,进行如下实验。(装置气密性良好,每一步均能完全反应)
(已知: )
)
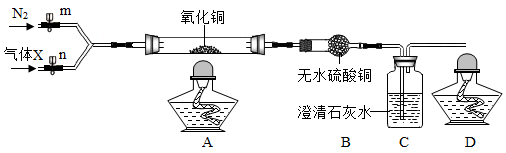
实验步骤:
Ⅰ、关闭n,打开m,通入一段时间氮气后关闭m。分别称量装置A、B、C的质量。
Ⅱ、打开n,分别点燃两处酒精灯;通入X气体观察,记录现象。
Ⅲ、停止加热,关闭n,打开m,再通一段时间的N2。再次分别称量装置A、B、C的质量。数据如下表:
回答下列问题:
(1)步骤Ⅰ中通N2的目的是______ 。
(2)步骤Ⅱ中,对“分别点燃两处酒精灯”,最适宜的操作是______ 。
a.先点燃A酒精灯,通一会儿X气体后点燃D酒精灯
b.先点燃D酒精灯,通一会儿X气体后点燃A酒精灯
c.同时点燃A、D两处酒精灯
(3)实验中装置A中的现象是______ ;装置B的作用______ 。装置C发生反应的化学方程式______ 。不能将装置B、装置C位置互换,理由是______ 。
(4)根据表中实验数据,请分析气体X的成分______ 。
(已知:
 )
)
实验步骤:
Ⅰ、关闭n,打开m,通入一段时间氮气后关闭m。分别称量装置A、B、C的质量。
Ⅱ、打开n,分别点燃两处酒精灯;通入X气体观察,记录现象。
Ⅲ、停止加热,关闭n,打开m,再通一段时间的N2。再次分别称量装置A、B、C的质量。数据如下表:
| 装置A中玻璃管(含药品)的质量 | 装置B的质量 | 装置C的质量 | |
| 反应前 | 150g | 152.6g | 254.8g |
| 反应后 | 143.6g | 156.2g | 259.2g |
(1)步骤Ⅰ中通N2的目的是
(2)步骤Ⅱ中,对“分别点燃两处酒精灯”,最适宜的操作是
a.先点燃A酒精灯,通一会儿X气体后点燃D酒精灯
b.先点燃D酒精灯,通一会儿X气体后点燃A酒精灯
c.同时点燃A、D两处酒精灯
(3)实验中装置A中的现象是
(4)根据表中实验数据,请分析气体X的成分
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
名校
解题方法
【推荐2】氢气被看做是理想的“绿色能源”,氢气的制备和储存是目前的研究热点。
I制氢
(1)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如下:

①甲烷和水蒸气反应的化学方程式是_________ 。
②600℃时加入CaO的作用是__________ 。
(2)还可利用太阳能光伏电池电解水制高纯氢,工作示意图如图甲。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接__________ (填“K1”或“K2”);改变开关连接方式,可得O2。
②利用太阳能光伏电池电解水制高纯氢的总反应化学方程式为__________ 。
Ⅱ储氢
(3)镁铝合金(Mg17Al12)是一种潜在的储氢材料,在氩气保护下,将一定化学计量比的Mg、A1单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为 ,反应后得到的混合物在一定条件下可释放出H2。
,反应后得到的混合物在一定条件下可释放出H2。
①根据完全吸氢的化学方程式计算:3.66g镁铝合金(Mg17A112)理论上能吸收氢气的质量为多少_________ ?(写出计算过程)。
②图乙为氢气球磨镁铝合金在不同温度下的放氢曲线(氢气球磨镁铝合金材料的储氢量约为3.03%),根据以上信息,下列关于镁铝合金储氢材料的说法正确的是_________ 。
a.镁铝合金的熔点介于金属镁和金属铝之间
b.镁铝合金在氩气中熔炼的目的是防止金属被氧化
c.由图可知,当温度高于260℃时,几乎所有的储存氢都能放出
d.当放氢温度由260℃升至320℃时,放氢的速度变快
I制氢
(1)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如下:

①甲烷和水蒸气反应的化学方程式是
②600℃时加入CaO的作用是
(2)还可利用太阳能光伏电池电解水制高纯氢,工作示意图如图甲。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接
②利用太阳能光伏电池电解水制高纯氢的总反应化学方程式为
Ⅱ储氢
(3)镁铝合金(Mg17Al12)是一种潜在的储氢材料,在氩气保护下,将一定化学计量比的Mg、A1单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
 ,反应后得到的混合物在一定条件下可释放出H2。
,反应后得到的混合物在一定条件下可释放出H2。①根据完全吸氢的化学方程式计算:3.66g镁铝合金(Mg17A112)理论上能吸收氢气的质量为多少
②图乙为氢气球磨镁铝合金在不同温度下的放氢曲线(氢气球磨镁铝合金材料的储氢量约为3.03%),根据以上信息,下列关于镁铝合金储氢材料的说法正确的是
a.镁铝合金的熔点介于金属镁和金属铝之间
b.镁铝合金在氩气中熔炼的目的是防止金属被氧化
c.由图可知,当温度高于260℃时,几乎所有的储存氢都能放出
d.当放氢温度由260℃升至320℃时,放氢的速度变快
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐3】用金属铁通过一系列转化,可以制备新型消毒、净水剂K2FeO4.流程如下:

请回答下列问题:
(1)固体B的成分是_____________ (用化学式表示);反应①后经过__________ 操作可分别得到固体B和溶液A.
(2)反应①、②、③中没有涉及到的化学基本反应类型是__________ .
(3)请写出反应②的化学方程式___________________________ .
(4)如果所得净水剂K2FeO4的质量为19.8kg,则理论上参加反应的铁的质量为____ kg.

请回答下列问题:
(1)固体B的成分是
(2)反应①、②、③中没有涉及到的化学基本反应类型是
(3)请写出反应②的化学方程式
(4)如果所得净水剂K2FeO4的质量为19.8kg,则理论上参加反应的铁的质量为
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
【推荐1】回答下列问题
(1)实验室有失去标签的三瓶无色溶液,已知分别是盐酸、氯化钠溶液和碳酸钠溶液中的一种,要求只用无色酚酞一种试剂鉴别它们。请完成如下实验:
①取少量三种溶液分别加入A、B、C三支试管中,各滴加2滴无色酚酞试液,若观察到B、C两支试管中的溶液为无色,则A试管中的溶液呈___________ 色。
②任取剩下的两种溶液中的一种,滴入上述实验后的A试管中,若观察到A试管中有气泡产生,则滴入的是___________ 溶液(写化学式),写出该反应的化学方程式___________ 。
(2)现有一包固体混合物A,其中可能含有NaCl、NH4Cl、Cu(NO3)2、K2SO4四种物质中的一种或多种。现按下图所示进行检验,相关的现象如图中所述(假设过程中所有发生的反应都恰好完全反应)。请你依据实验过程和产生的现象做出分析与判断:

①沉淀G的化学式是___________ ,气体B具有___________ 气味。
②滤液F中一定存在的金属离子有___________ (写出离子符号)。
③步骤④发生反应的化学方程式为___________ 。
④通过上述现象判断,该固体混合物A中一定含有的物质是___________ ,不能确定是否含有的物质是___________ ,请简要说出不能确定的原因___________ 。
(1)实验室有失去标签的三瓶无色溶液,已知分别是盐酸、氯化钠溶液和碳酸钠溶液中的一种,要求只用无色酚酞一种试剂鉴别它们。请完成如下实验:
①取少量三种溶液分别加入A、B、C三支试管中,各滴加2滴无色酚酞试液,若观察到B、C两支试管中的溶液为无色,则A试管中的溶液呈
②任取剩下的两种溶液中的一种,滴入上述实验后的A试管中,若观察到A试管中有气泡产生,则滴入的是
(2)现有一包固体混合物A,其中可能含有NaCl、NH4Cl、Cu(NO3)2、K2SO4四种物质中的一种或多种。现按下图所示进行检验,相关的现象如图中所述(假设过程中所有发生的反应都恰好完全反应)。请你依据实验过程和产生的现象做出分析与判断:

①沉淀G的化学式是
②滤液F中一定存在的金属离子有
③步骤④发生反应的化学方程式为
④通过上述现象判断,该固体混合物A中一定含有的物质是
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
名校
解题方法
【推荐2】铋(Bi)的无毒与不致癌性有很多特殊用途,其化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 Bi2S3,含杂质 PbO2等)制备 Bi2O3的工艺如下:

已知:硝酸盐分解产生氮的氧化物。
回答下列问题:
(1)Bi 位于元素周期表第六周期,与 N、P 同族,Bi 原子的最外层有______ 个电子。
(2)“浸出”时 Bi2S3与 FeCl3溶液反应的产物之一为 FeCl2,且 Bi 元素在反应前后化合价不变。该反应化学方程式为______ 。
(3)“置换”时生成单质铋的化学方程式为______ 。粗铋中含有的杂质(除 Fe 外)主要为______ (填化学式)。
(4)“浸出”、“置换”步骤中均用到的分离方法是______ ,在实验室进行此项操作需用到的玻璃仪器除了玻璃棒、烧杯外,还需要______ 。
(5)碱式硝酸铋直接灼烧也能得到 Bi2O3,上述工艺中转化为碱式碳酸铋再灼烧,除了能改良产品性状,另一优点是______ 。“母液 2”中可回收的主要物质是______ (填名称),写出它的一种用途:______ 。

已知:硝酸盐分解产生氮的氧化物。
回答下列问题:
(1)Bi 位于元素周期表第六周期,与 N、P 同族,Bi 原子的最外层有
(2)“浸出”时 Bi2S3与 FeCl3溶液反应的产物之一为 FeCl2,且 Bi 元素在反应前后化合价不变。该反应化学方程式为
(3)“置换”时生成单质铋的化学方程式为
(4)“浸出”、“置换”步骤中均用到的分离方法是
(5)碱式硝酸铋直接灼烧也能得到 Bi2O3,上述工艺中转化为碱式碳酸铋再灼烧,除了能改良产品性状,另一优点是
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
【推荐3】某化工厂用石灰石和废铜屑等设计生产石青、波尔多液的工艺流程如下:
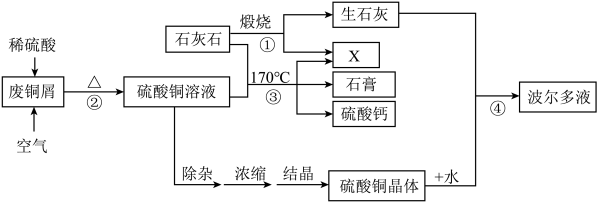
(1)X的化学式为___________ 。
(2)反应②中空气的作用是_________________ 。
(3)石青的化学式为2CuCO3·Cu(OH)2,写出反应③的化学方程式____________________________________ 。
(4)若反应④中硫酸铜、生石灰和水的化学计量数之比为1:1:1,则其化学方程式为______________ 。

(1)X的化学式为
(2)反应②中空气的作用是
(3)石青的化学式为2CuCO3·Cu(OH)2,写出反应③的化学方程式
(4)若反应④中硫酸铜、生石灰和水的化学计量数之比为1:1:1,则其化学方程式为
您最近一年使用:0次




