2019年诺贝尔化学奖授予对锂离子电池研究作出贡献的三位科学家。下图是从钴酸锂废极片【主要成分为钴酸锂(LiCoO2)中回收得到Co2O3和Li2CO3的一种工艺流程。
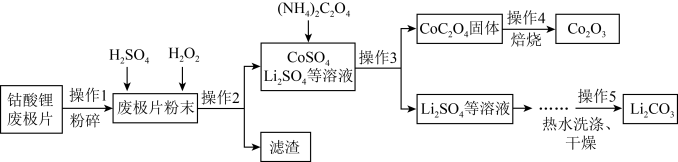
(1)操作1中,粉碎废极片的目的是_____ ;
(2)实验室中完成操作2时,需用到的玻璃仪器是_____ (填一种即可);
(3)操作4中,在高温条件下,CoC2O4在空气中反应生成Co2O3和二氧化碳,化学方程式为_____ ;
(4)操作5中,Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而_____ 。

(1)操作1中,粉碎废极片的目的是
(2)实验室中完成操作2时,需用到的玻璃仪器是
(3)操作4中,在高温条件下,CoC2O4在空气中反应生成Co2O3和二氧化碳,化学方程式为
(4)操作5中,Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而
2020·江西·中考真题 查看更多[11]
2023年湖南省娄底市中考化学猜题卷22021年山东省青岛市第九中学自主招生笔试化学试题 2021年山东省青岛市第九中学自主招生笔试化学试题(已下线)2022年中考风向标-北京-工艺流程2021年湖南省株洲市茶陵县中考模拟化学试题(已下线)必刷卷02-2021年中考化学考前信息必刷卷(临沂专用)2021年广东省广州市番禺区中考二模化学试题2021年北京市门头沟区中考一模化学试题(已下线)热点03 工艺流程题类-2021年中考化学【热点·重点·难点】专练(已下线)专题18 工艺流程图题(考点)-备战2021年中考化学考点微专题江西省2020年中考化学试题
更新时间:2020-07-19 22:10:27
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
【推荐1】如图是实验室模拟炼铁原理的装置。
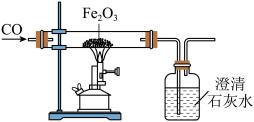
(1)实验开始时,先通一会儿一氧化碳再加热的目的是什么?
(2)写出酒精喷灯内酒精燃烧的化学方程式。
(3)从环保角度考虑、此装置有不足之处,请加以补充改正。

(1)实验开始时,先通一会儿一氧化碳再加热的目的是什么?
(2)写出酒精喷灯内酒精燃烧的化学方程式。
(3)从环保角度考虑、此装置有不足之处,请加以补充改正。
您最近一年使用:0次
【推荐2】元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:
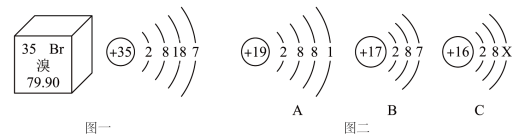
(1)溴的相对原子质量是___________ 。
(2)溴元素的化学性质与图二哪种元素的化学性质相似___________ (填序号)。
(3)溴元素与图二中A元素形成化合物的化学式为___________ :。
(4)若图二中C表示离子,则离子符号是___________ 。
(5)如图是某反应的微观示意图
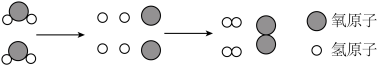
①该化学变化过程中,一定不能再分的微粒是___________ (用化学用语表示)
②该反应的化学方程式是___________ 。

(1)溴的相对原子质量是
(2)溴元素的化学性质与图二哪种元素的化学性质相似
(3)溴元素与图二中A元素形成化合物的化学式为
(4)若图二中C表示离子,则离子符号是
(5)如图是某反应的微观示意图

①该化学变化过程中,一定不能再分的微粒是
②该反应的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】学习化学使我们从五彩缤纷的宏观世界步入了充满神奇色彩的微观世界。
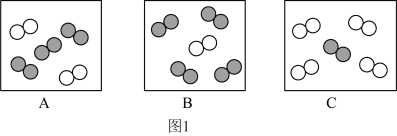
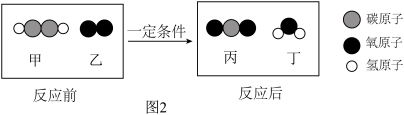
(1)请沿用科学家认识事物的方式认识“空气”,根据图1回答:
①从分类角度:空气属于_______ (填“混合物”或“纯净物”)。
②从微观角度:用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氧原子。
”表示氧原子。
a.用“ ”可表示的微粒是
”可表示的微粒是_______ (填名称)。
b.同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,图1中可表示空气微观模型的是_______ (填字母标号)。
(2)请根据图2写出反应的化学方程式:_______ 。


(1)请沿用科学家认识事物的方式认识“空气”,根据图1回答:
①从分类角度:空气属于
②从微观角度:用“
 ”表示氮原子,用“
”表示氮原子,用“ ”表示氧原子。
”表示氧原子。a.用“
 ”可表示的微粒是
”可表示的微粒是b.同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,图1中可表示空气微观模型的是
(2)请根据图2写出反应的化学方程式:
您最近一年使用:0次
【推荐1】a、b、c三种固体物质在水中的溶解度曲线如图所示。请回答:
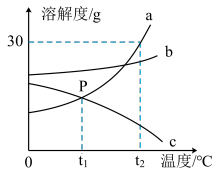
(1)P点的含义_______ 。
(2)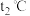 时,将20g的a物质加入到50g水中可得到溶液的质量
时,将20g的a物质加入到50g水中可得到溶液的质量_______ g。
(3)将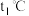 时a、b、c三种物质的饱和溶液升温至
时a、b、c三种物质的饱和溶液升温至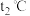 ,溶液的溶质质量分数由大到小为
,溶液的溶质质量分数由大到小为_______ 。
(4)将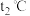 时等质量的a、b、c三种物质的饱和溶液降温至
时等质量的a、b、c三种物质的饱和溶液降温至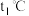 ,析出的晶体最多的物质
,析出的晶体最多的物质_______ ,所形成的溶液中溶剂的质量大小关系为_______ 。

(1)P点的含义
(2)
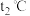 时,将20g的a物质加入到50g水中可得到溶液的质量
时,将20g的a物质加入到50g水中可得到溶液的质量(3)将
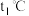 时a、b、c三种物质的饱和溶液升温至
时a、b、c三种物质的饱和溶液升温至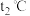 ,溶液的溶质质量分数由大到小为
,溶液的溶质质量分数由大到小为(4)将
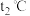 时等质量的a、b、c三种物质的饱和溶液降温至
时等质量的a、b、c三种物质的饱和溶液降温至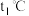 ,析出的晶体最多的物质
,析出的晶体最多的物质
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】如图是 A、B、C三种物质的溶解度曲线。请回答:
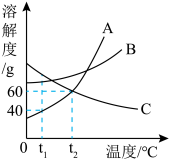
(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是_____ ;
(2)当A中混有少量B时,可用_____ 方法提纯A;
(3)t2℃时,在200g水中放入_____ 克A物质恰好形成饱和溶液,此时溶液中溶质的质量分数为_____ 。

(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是
(2)当A中混有少量B时,可用
(3)t2℃时,在200g水中放入
您最近一年使用:0次
【推荐3】为了探究物质W的溶解度随温度变化的情况,某同学在实验室进行了相关实验(具体操作、现象如图1所示)。请根据实验现象和相关数据作出相应的分析和判断:
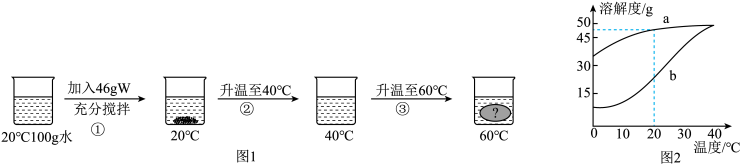
(1)根据实验操作①所产生的现象可知,W为图2中的______ (填“a”或“b”)曲线。
(2)操作①所得的溶液,其溶质的质量分数为20%,则:20℃时W的溶解度为______ g。
(3)如表为W部分温度下的溶解度,请推测实验操作③所产生的现象______ 。
(4)若在实验操作③后继续升温至:80°C,析出0.9gW,则W在80°C时的溶解度为______ g。

(1)根据实验操作①所产生的现象可知,W为图2中的
(2)操作①所得的溶液,其溶质的质量分数为20%,则:20℃时W的溶解度为
(3)如表为W部分温度下的溶解度,请推测实验操作③所产生的现象
| 温度/℃ | 40 | 60 |
| 溶解度/g | 48.8 | 46.4 |
(4)若在实验操作③后继续升温至:80°C,析出0.9gW,则W在80°C时的溶解度为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
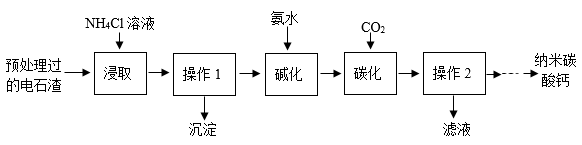
【推荐1】电石渣【主要成分为Ca(OH)2,还含有MgO等杂质】是一种工业废渣,以它为原料可生产纳米碳酸钙。
②“浸取”时的主要反应为
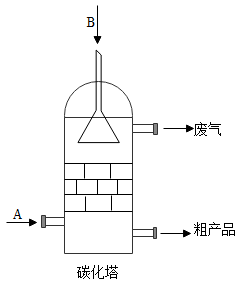
③“碳化”时的主要反应为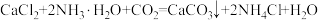
(1)制备方案中“操作1”是_______ 。
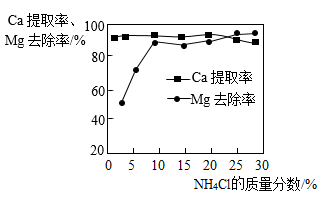
(2)在“浸取”步骤中,用不同质量分数的NH4Cl溶液浸取电石渣时,Ca元素提取率和Mg元素去除率的数值如图所示,你认为较适宜的NH4Cl质量分数是_______ 。_______ 处通入(填“A”或“B”)。
你认为碳化反应最适宜的温度是_______ ℃。
(5)“操作2”中得到的滤液中含有的溶质是_______ 。
(6)用电石渣【Ca(OH)2质量分数92.5%】制备1tCaCO3,计算所需电石渣的质量。_______
②“浸取”时的主要反应为

③“碳化”时的主要反应为
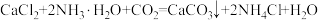
(1)制备方案中“操作1”是
(2)在“浸取”步骤中,用不同质量分数的NH4Cl溶液浸取电石渣时,Ca元素提取率和Mg元素去除率的数值如图所示,你认为较适宜的NH4Cl质量分数是
| 温度 | 反应液浑浊所需时间(单位:秒) | 反应完全所需时间(单位:分钟) |
| 20℃ | 480 | >180 |
| 40℃ | 120 | 180 |
| 60℃ | 1 | 50 |
| 80℃ | 1 | 68 |
(5)“操作2”中得到的滤液中含有的溶质是
(6)用电石渣【Ca(OH)2质量分数92.5%】制备1tCaCO3,计算所需电石渣的质量。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】早在战国时期,《周礼·考工记》就记载了我国劳动人民制取KOH以漂洗丝帛的工艺。大意是:先将干燥的木头烧成灰(含K2CO3),用其灰汁浸泡丝帛,再加入石灰即可。如图为模拟该法制取KOH的工艺流程。请回答有关问题。
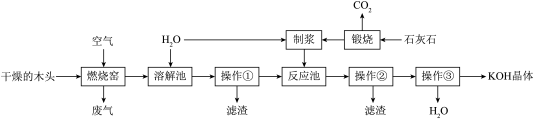
(1)我市云石山有丰富的石灰石资源,石灰石的主要成分是______ 。
(2)实验室里进行操作②、操作③均用到的玻璃仪器是______ 。
(3)“反应池”中发生主要反应的化学方程式是______ 。
(4)“制浆”中发生反应的基本反应类型是______ 。
(5)流程中可循环使用的物质是______ 。

(1)我市云石山有丰富的石灰石资源,石灰石的主要成分是
(2)实验室里进行操作②、操作③均用到的玻璃仪器是
(3)“反应池”中发生主要反应的化学方程式是
(4)“制浆”中发生反应的基本反应类型是
(5)流程中可循环使用的物质是
您最近一年使用:0次




