某工厂生产硼砂产生的固体废料,主要含有MgCO3、CaCO3、SiO2、Al2O3和Fe2O3等,其中MgCO3质量分数为63%。回收镁的工艺流程如下:
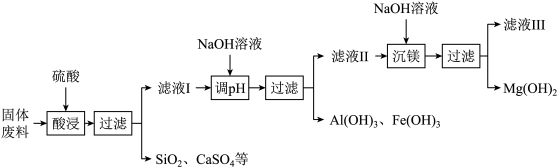
(1)“酸浸”时MgCO3发生反应的化学方程式为_________ 。
(2)“调pH”前滤液I的pH________ 7(填“>”或“<”)。
(3)滤液Ⅲ中可回收的主要物质________ (填化学式)。
(4)已知固体废料质量为m,理论上可生产Mg(OH)2的质量为______ 。
(5)某BaCO3中混有SiO2杂质,简述提纯该BaCO3的实验操作:___________ 。

(1)“酸浸”时MgCO3发生反应的化学方程式为
(2)“调pH”前滤液I的pH
(3)滤液Ⅲ中可回收的主要物质
(4)已知固体废料质量为m,理论上可生产Mg(OH)2的质量为
(5)某BaCO3中混有SiO2杂质,简述提纯该BaCO3的实验操作:
2020·广东广州·中考真题 查看更多[8]
2021年广东省广州市中考考前冲刺(四)化学试题(已下线)专题03 盐 化肥-【学以致用】备战2023年中考化学易错题型讲练(广东专用)(已下线)2023年中考风向标-广东-流程题(已下线)专题11 计算题-5年(2018-2022)中考1年模拟化学分项汇编(广州专用)(已下线)专题08 工业流程题-5年(2018-2022)中考1年模拟化学分项汇编(广州专用)2022年山东省枣庄市台儿庄区中考考前最后一卷化学试题三(已下线)专题19: 化学工艺流程题(测试)--2021年中考化学一轮复习讲练测(人教版)广东省广州市2020年中考化学试题
更新时间:2020-07-26 22:48:45
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】学习知识的目的之一是分析和解决实际的问题。
(1)为防止资源浪费,燃烧时通常将煤块变为粉末状,其原因是_________ 。
(2)在牙膏和一些药品中,常用轻质碳酸钙粉末作填充剂或载体。制取轻质碳酸钙粉末是用净化后的石灰乳(主要成分为氢氧化钙)与二氧化碳作用,制取过程中发生反应的化学方程式为_________ 。
(3)镁条在氧气中燃烧后,生成物的质量比原来镁条的质量增大,其原因是________ 。
(4)CaCl2溶液和NaHCO3溶液反应生成CaCO3。为表示这个反应写出了下列两个化学方程式:
① CaCl2 + NaHCO3=CaCO3 ↓+ NaCl + HCl;
② CaCl2 + 2NaHCO3=CaCO3 ↓+ 2NaCl + CO2 ↑+ H2O。
你认为___ (填“①”或“②”)化学方程式不合理,并简述理由_________ 。
(1)为防止资源浪费,燃烧时通常将煤块变为粉末状,其原因是
(2)在牙膏和一些药品中,常用轻质碳酸钙粉末作填充剂或载体。制取轻质碳酸钙粉末是用净化后的石灰乳(主要成分为氢氧化钙)与二氧化碳作用,制取过程中发生反应的化学方程式为
(3)镁条在氧气中燃烧后,生成物的质量比原来镁条的质量增大,其原因是
(4)CaCl2溶液和NaHCO3溶液反应生成CaCO3。为表示这个反应写出了下列两个化学方程式:
① CaCl2 + NaHCO3=CaCO3 ↓+ NaCl + HCl;
② CaCl2 + 2NaHCO3=CaCO3 ↓+ 2NaCl + CO2 ↑+ H2O。
你认为
您最近一年使用:0次
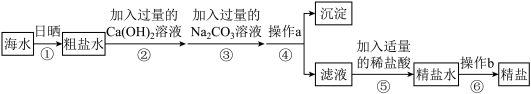
【推荐2】为了维护南海权益,我国去年宣布成立了三沙市。这是维护国家主权的象征,同时也是因为海洋资源十分丰富,有广泛的利用价值。其中通过海水晾晒即可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:

(1)根据以上信息,请写出海水中所含的主要阴离子的符号__________________ 。
(2)在上述流程中第③步加过量NaOH的目的是除去海水中的_____ (填离子符号,下同),第④步加过量Na2CO3的目的是除去海水中的 ______ 。第⑥步其实显示的是加适量盐酸,其目的是除去多余的 ____ 。
(3)请写出第②步所发生反应的化学方程式____________________________ 。
(4)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是___________ 。

(1)根据以上信息,请写出海水中所含的主要阴离子的符号
(2)在上述流程中第③步加过量NaOH的目的是除去海水中的
(3)请写出第②步所发生反应的化学方程式
(4)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】根据如图甲、乙两种物质的溶解度曲线回答相关问题:

(1)除去甲中混有的少量乙的方法是______ 。
(2)将t1℃时甲、乙两种物质的饱和溶液升温至t2℃(其他条件不变),所得溶液溶质质量分数的关系是甲______ (填“>”、“<”或“=”)乙。
(3)t2℃时,若将75g甲的饱和溶液稀释成20%,需加水的质量为______ g。

(1)除去甲中混有的少量乙的方法是
(2)将t1℃时甲、乙两种物质的饱和溶液升温至t2℃(其他条件不变),所得溶液溶质质量分数的关系是甲
(3)t2℃时,若将75g甲的饱和溶液稀释成20%,需加水的质量为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海水晒盐得到的粗盐常含有MgCl2、CaCl2等杂质,工业提纯粗盐的流程如图所示。_______ 。
(2)如果将步骤②和步骤③的顺序颠倒,则所制得的精盐水中还含有_______ 。
(3)写出步骤③中反应的化学方程式_______ 。(写一个)
(2)如果将步骤②和步骤③的顺序颠倒,则所制得的精盐水中还含有
(3)写出步骤③中反应的化学方程式
您最近一年使用:0次


 、
、 、
、  、
、 ,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如图
,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如图 杂质不溶于水、不参与反应
杂质不溶于水、不参与反应 :
:
 溶液A中溶质有
溶液A中溶质有 、
、  溶液C中溶质的质量分数
溶液C中溶质的质量分数  上述流程中,加热蒸发的目的是
上述流程中,加热蒸发的目的是  、Ⅱ、Ⅲ的实验过程中均用到的基本操作为
、Ⅱ、Ⅲ的实验过程中均用到的基本操作为 

