将锌粉加入到一定质量Mg(NO3)2、Cu(NO3)2、AgNO3的混合溶液中,充分反应后过滤,可以得到溶液和固体。
(1)写出一个可能发生反应的化学方程式_____
(2)若向固体中加入稀盐酸,有气泡产生,此时溶液中所含有的溶质是______
(3)若反应后溶液为蓝色,且反应前混合溶液质量与反应后过滤出的溶液质量相等,此时的固体成分是_____
(1)写出一个可能发生反应的化学方程式
(2)若向固体中加入稀盐酸,有气泡产生,此时溶液中所含有的溶质是
(3)若反应后溶液为蓝色,且反应前混合溶液质量与反应后过滤出的溶液质量相等,此时的固体成分是
更新时间:2020-06-27 10:38:12
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属及其制品是现代生活中不可缺少的材料和工具。
(1)“沙里淘金”说明金在自然界中以______ 形式存在(填“单质”或“化合物”)。以下金属材料属于 合金的是______ (多选、少选、错选均不得分)。
A青铜 B铝 C不锈钢 D焊锡
(2)用新工艺将不锈钢加工成柔软的金属丝,用它和棉纤维一起编制成性能优良的劳动防护服,这是利用了不锈钢的______ 性;铁栅栏喷漆不但美观而且可以防止生锈,其喷漆的防锈原理是______ ;铁锈主要成分是Fe2O3,喷漆前可用稀盐酸除去,请写出稀盐酸除锈的化学方程式:______ 。
(3)向AgNO3和 的混合溶液中加入一定量的Zn粉,充分反应后过滤,得滤渣和滤液。
的混合溶液中加入一定量的Zn粉,充分反应后过滤,得滤渣和滤液。
①若滤液为无色,则滤渣中一定含有的物质是______ ;
②若向滤渣滴加稀盐酸,无气泡产生,则滤液中所含溶质的成分可能有______ 种情况。
(1)“沙里淘金”说明金在自然界中以
A青铜 B铝 C不锈钢 D焊锡
(2)用新工艺将不锈钢加工成柔软的金属丝,用它和棉纤维一起编制成性能优良的劳动防护服,这是利用了不锈钢的
(3)向AgNO3和
 的混合溶液中加入一定量的Zn粉,充分反应后过滤,得滤渣和滤液。
的混合溶液中加入一定量的Zn粉,充分反应后过滤,得滤渣和滤液。①若滤液为无色,则滤渣中一定含有的物质是
②若向滤渣滴加稀盐酸,无气泡产生,则滤液中所含溶质的成分可能有
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】如图所示,A-H都是初中化学中常见的物质,已知:常温下,A是黑色固体单质,B是黑色固体化合物,D为红色固体单质,F为Fe2O3,它们的转化关系如图所示.按要求完成下列各题:
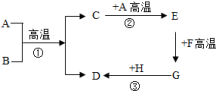
(1)写出下列物质的化学式:C________ ,E________ .
(2)写出上图中①②③反应的化学方程式:
①___________ ;
②___________ ;
③___________ .
(3)反应的①③基本反应类型都是________ ,反应②的基本反应类型是________ .

(1)写出下列物质的化学式:C
(2)写出上图中①②③反应的化学方程式:
①
②
③
(3)反应的①③基本反应类型都是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属和金属材料在生产生活中有广泛的用途。请回答下列问题:
(1)随着近年材料科学的迅猛发展,飞机外壳也运用了材料﹣﹣钛合金,“钛合金”属于______ (填“纯净物”或“混合物”)。
(2)工业上,常用一氧化碳在高温条件下还原赤铁矿(主要成分是Fe2O3)的方法炼铁,该反应的化学方程式为______ 。铁制品生锈是由于铁制品接触了空气中的______ 。
(3)向一定量的AgNO3溶液中加入一定量的锌粉和铁粉,充分反应后过滤,得到滤渣和溶液。对滤渣和滤液分析正确的有______ (填序号)。
①若滤液呈浅绿色,则滤渣中一定含有Ag,一定不含有Fe
②若滤液中只含有一种溶质,则滤渣中一定含有Ag、Fe,可能含有Zn
③若滤渣中只含有一种金属,则溶液中一定含有Zn(NO3)2、Fe(NO3)2,一定不含有AgNO3
④若向滤渣中滴加稀盐酸无体产生,则滤液中一定含有Zn(NO3)2,可能含有AgNO3、Fe(NO3)2
(1)随着近年材料科学的迅猛发展,飞机外壳也运用了材料﹣﹣钛合金,“钛合金”属于
(2)工业上,常用一氧化碳在高温条件下还原赤铁矿(主要成分是Fe2O3)的方法炼铁,该反应的化学方程式为
(3)向一定量的AgNO3溶液中加入一定量的锌粉和铁粉,充分反应后过滤,得到滤渣和溶液。对滤渣和滤液分析正确的有
①若滤液呈浅绿色,则滤渣中一定含有Ag,一定不含有Fe
②若滤液中只含有一种溶质,则滤渣中一定含有Ag、Fe,可能含有Zn
③若滤渣中只含有一种金属,则溶液中一定含有Zn(NO3)2、Fe(NO3)2,一定不含有AgNO3
④若向滤渣中滴加稀盐酸无体产生,则滤液中一定含有Zn(NO3)2,可能含有AgNO3、Fe(NO3)2
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】把铁钉放入硫酸铜溶液中,其现象为___________ 。反应的化学方程式为_________ 。位于_________ 前面金属能在酸中置换出氢,如:_________ (写出化学方程式)。在金属活动性顺序表中,位于_________ 的金属能把位于_________ 的金属从它们的化合物的水溶液中置换出来。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】黄铜是由铜和锌组成的合金,可用于制造钱币、机器零件等。利用黄铜制造各种物品的过程中,会产生大量的黄铜渣,主要含有Zn、Cu、ZnO、CuO。一种利用黄铜渣获取金属铜和硫酸锌溶液的实验流程如下:资料卡片:氧化铜、氧化锌分别跟稀硫酸反应生成硫酸铜、硫酸锌

(1)下列关于黄铜的说法正确的是______ (填序号)。
a.黄铜不能被腐蚀 b.黄铜的硬度比铜大 c.黄铜的熔点比锌高
(2)“酸溶”过程中有气体生成,写出该反应的化学方程式:______ 。
(3)“置换”过程中需要加入过量Zn的目的是______ 。
(4)为进一步提高原料利用率,得到更多的铜和硫酸锌溶液,需要对流程中的“滤渣”进行处理。向滤渣中缓慢加入______ (填“稀硫酸”或“稀盐酸”)并不断搅拌,观察到______ 时停止加入,过滤。
(5)上述流程中,能判断锌的金属活动性比铜强的事实是______ (写一条)。
(6)每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失,铁在空气中锈蚀,实际上是铁跟______ 、______ 共同作用的结果;请你提出一种防止铁制品锈蚀的方法:______ 。

(1)下列关于黄铜的说法正确的是
a.黄铜不能被腐蚀 b.黄铜的硬度比铜大 c.黄铜的熔点比锌高
(2)“酸溶”过程中有气体生成,写出该反应的化学方程式:
(3)“置换”过程中需要加入过量Zn的目的是
(4)为进一步提高原料利用率,得到更多的铜和硫酸锌溶液,需要对流程中的“滤渣”进行处理。向滤渣中缓慢加入
(5)上述流程中,能判断锌的金属活动性比铜强的事实是
(6)每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失,铁在空气中锈蚀,实际上是铁跟
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐3】人类文明发展与金属材料的使用有着密切联系。
(1)生活中使用的铝制品具有很好的抗腐蚀性,其原因是___________ (用化学方程式表示)。
(2)金可制成金箔,拉成金丝,说明金具有良好的___________ 性。
(3)现有甲、乙、丙三种金属,把甲和乙分别放入稀硫酸中,甲溶解并产生气泡,乙无明显现象;把乙和丙分别放入硝酸银溶液中,乙表面有银白色固体析出,而丙无明显变化,则这三种金属的活动性由强到弱的顺序为___________ 。
(4)某电镀厂为减少水污染及节约成本,从含有CuSO4、ZnSO4、FeSO4的废水中回收ZnSO4和有关金属,流程如图:
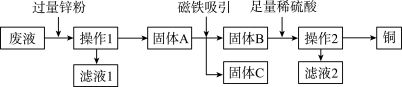
①废液中加入过量锌粉时,与CuSO4发生的化学反应方程式为___________ ,该反应的基本反应类型为___________ 反应。
②操作1的名称为___________ ,用到的玻璃仪器有烧杯,玻璃棒和___________ 。
③除水外,滤液1和滤液2还含有相同的物质,该物质是___________ (填化学式)。
(1)生活中使用的铝制品具有很好的抗腐蚀性,其原因是
(2)金可制成金箔,拉成金丝,说明金具有良好的
(3)现有甲、乙、丙三种金属,把甲和乙分别放入稀硫酸中,甲溶解并产生气泡,乙无明显现象;把乙和丙分别放入硝酸银溶液中,乙表面有银白色固体析出,而丙无明显变化,则这三种金属的活动性由强到弱的顺序为
(4)某电镀厂为减少水污染及节约成本,从含有CuSO4、ZnSO4、FeSO4的废水中回收ZnSO4和有关金属,流程如图:

①废液中加入过量锌粉时,与CuSO4发生的化学反应方程式为
②操作1的名称为
③除水外,滤液1和滤液2还含有相同的物质,该物质是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】某化学小组向Cu(NO3)2和Zn(NO3)2的混合溶液中加入一定量的Mg粉,充分反应后过滤。
(1)若向滤渣中加入稀盐酸,有气泡冒出。请分析滤渣的成分。
(2)若滤液呈蓝色,则滤液中的溶质有哪些?(写化学式)
(1)若向滤渣中加入稀盐酸,有气泡冒出。请分析滤渣的成分。
(2)若滤液呈蓝色,则滤液中的溶质有哪些?(写化学式)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】人类社会的文明进步与金属材料的发展密切相关,结合所学化学知识回答有关问题。
(1)地壳中含量最高的金属元素是_______ 。(填符号)
(2)实验室所用的石棉网中有铁丝,隔着石棉网给容器加热可达到均匀受热的目的,这主要利用铁的_______ 性。石棉网使用一段时间后,其中的铁丝容易生锈,可用稀硫酸除去,反应的化学方程式为_______ 。
(3)某兴趣小组为探究Zn、Ag、Fe、Cu四种金属的活动性,进行如图甲、乙、丙三个实验。
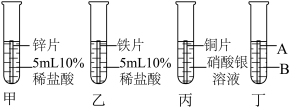
①甲中发生反应的化学方程式为_______ 。
②小组同学发现该实验无法得出四种金属的活动性顺序,于是补充丁实验,最终得出四种金属活动性顺序。则丁中金属A和溶液B分别是_______ 。
③通过实验得出四种金属活动性由强到弱的顺序是_______ 。
(4)某锌粉含有铜、镁中的一种杂质,取该样品6.5g与足量稀盐酸充分反应,生成氢气0.21g,该锌粉中含有的杂质是_______ 。另取一定量该样品放入硫酸铜溶液中,充分反应后过滤,得到滤渣和滤液。将滤渣洗浄,滴入稀硫酸,有气泡产生,则滤渣中一定含有的成分是_______ 。
(1)地壳中含量最高的金属元素是
(2)实验室所用的石棉网中有铁丝,隔着石棉网给容器加热可达到均匀受热的目的,这主要利用铁的
(3)某兴趣小组为探究Zn、Ag、Fe、Cu四种金属的活动性,进行如图甲、乙、丙三个实验。

①甲中发生反应的化学方程式为
②小组同学发现该实验无法得出四种金属的活动性顺序,于是补充丁实验,最终得出四种金属活动性顺序。则丁中金属A和溶液B分别是
③通过实验得出四种金属活动性由强到弱的顺序是
(4)某锌粉含有铜、镁中的一种杂质,取该样品6.5g与足量稀盐酸充分反应,生成氢气0.21g,该锌粉中含有的杂质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属是人类生活中的常用的材料。
(1)下列生活用品中,利用金属导热性的是______ (填字母序号)。
A 铝制易拉罐 B铜制火锅 C 铁锅 D 自行车铁架
(2)某化学兴趣小组的同学在探究铝、铜、铁三种金属的有关性质时,进行了如图实验:在A实验中发生反应的实验现象为______ 。将A实验结束后①、②试管内的物质倒入烧杯中,发现烧杯中的红色固体物质明显增多,一段时间后过滤。滤渣中:一定含有的物质是______ ,可能含有的物质是______ 。为了进一步确定可能有的物质是否存在,同学们向滤渣中滴加稀盐酸,结果没有气泡产生,那么滤液中含有金属离子的可能是______ (填写序号)
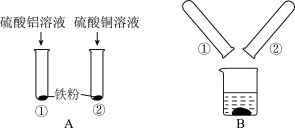
①Al3+②Al3+、Fe2+③Al3+、Fe3+④Fe2+、Cu2+⑤Al3+、Fe2+、Cu2+
(3)据有关资料报道,世界上每年因腐蚀而报废的金属设备或材料相当于年产量的20%~40%。稀盐酸常用于金属表面除锈,写出反应的化学方程式______ ,保护金属资源,人人有责,请写出一条防止铁制品生锈的方法______ 。
(1)下列生活用品中,利用金属导热性的是
A 铝制易拉罐 B铜制火锅 C 铁锅 D 自行车铁架
(2)某化学兴趣小组的同学在探究铝、铜、铁三种金属的有关性质时,进行了如图实验:在A实验中发生反应的实验现象为

①Al3+②Al3+、Fe2+③Al3+、Fe3+④Fe2+、Cu2+⑤Al3+、Fe2+、Cu2+
(3)据有关资料报道,世界上每年因腐蚀而报废的金属设备或材料相当于年产量的20%~40%。稀盐酸常用于金属表面除锈,写出反应的化学方程式
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】某同学将镁粉放入Cu(NO3)2、Ag(NO3)2的混合溶液中,测得溶液的质量随加入镁粉的质量的变化关系如图所示。

(1)写出d点时发生反应的化学方程式。
(2)a~e段溶液的质量一直减小的原因是什么?

(1)写出d点时发生反应的化学方程式。
(2)a~e段溶液的质量一直减小的原因是什么?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】向CuSO4和ZnSO4的混合溶液中加入过量的镁粉,充分反应后过滤,所得固体一定有_________ ,所得滤液的质量与原混合溶液质量相比_________ (填“增大”、“减少”或“不变”),请写出有关的化学反应方程式:_________ (任写一个).
您最近一年使用:0次




