现有一包白色粉末X,可能含有硫酸铜、硫酸钠,碳酸钠、氯化钠、硝酸钠、碳酸钙中的一种或几种,为确定其组成,进行如下实验探究
①称取质量为lg的白色粉末X加入水中充分溶解,得到无色澄清溶液。
②向X的溶液中加入稀硝酸。无气泡产生
③向步骤②反应后的溶波中加入硝酸钡溶液,无白色沉淀
④向步骤③所得溶液中加入硝酸银溶液,产生白色沉淀,将沉淀洗涤、干燥后称得质量为1.435g。
请回答下列问题。
(1)根据步骤①的现象,可推断白色粉末X中一定不含__________ (填化学式,下同)。
(2)结合步骤②③的现象可知。白色粉末X中一定不含__________ 。
(3)通过定量计算并综合分析。可确定白色粉末X的成分是__________ 。
①称取质量为lg的白色粉末X加入水中充分溶解,得到无色澄清溶液。
②向X的溶液中加入稀硝酸。无气泡产生
③向步骤②反应后的溶波中加入硝酸钡溶液,无白色沉淀
④向步骤③所得溶液中加入硝酸银溶液,产生白色沉淀,将沉淀洗涤、干燥后称得质量为1.435g。
请回答下列问题。
(1)根据步骤①的现象,可推断白色粉末X中一定不含
(2)结合步骤②③的现象可知。白色粉末X中一定不含
(3)通过定量计算并综合分析。可确定白色粉末X的成分是
更新时间:2020-07-03 19:41:36
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】实验室的废水中含有氯化钠、氯化镁和氯化钙,为了处理废水并回收氯化钠固体,某同学设计了以下方案,请根据流程图回答问题。
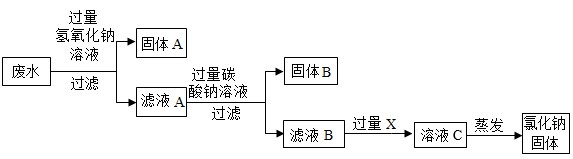
(1)写出在废水中加入过量氢氧化钠溶液时发生反应的化学方程式。__________
(2)写出滤液B中含有的溶质。__________
(3)请写出试剂X的名称__________ 。

(1)写出在废水中加入过量氢氧化钠溶液时发生反应的化学方程式。
(2)写出滤液B中含有的溶质。
(3)请写出试剂X的名称
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】分类、类比是学习化学常用的方法。
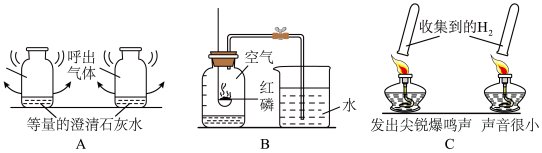
(1)在初中化学学习中,我们进行了比较物质的含量多少、测定物质的含量等不同类型的化学实验,据此将上述实验中的 A 与_______ 分为一类,分类依据是_______ 。
(2)已知镓(Ga)及其化合物应用广泛,常用于半导体、合金、磁性材料等领域。已知镓在化合物中常为+3 价,金属活动性顺序:Zn>Ga>Fe。(已知氢氧化镓是难溶于水的白色固体,且镓的硫酸盐和盐酸盐都是可溶的)请设计金属镓转化为氢氧化镓的一种方案,并用方程式表示出来(依次写出化学方程式)_______ 。

(1)在初中化学学习中,我们进行了比较物质的含量多少、测定物质的含量等不同类型的化学实验,据此将上述实验中的 A 与
(2)已知镓(Ga)及其化合物应用广泛,常用于半导体、合金、磁性材料等领域。已知镓在化合物中常为+3 价,金属活动性顺序:Zn>Ga>Fe。(已知氢氧化镓是难溶于水的白色固体,且镓的硫酸盐和盐酸盐都是可溶的)请设计金属镓转化为氢氧化镓的一种方案,并用方程式表示出来(依次写出化学方程式)
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】煤燃烧时产生的粉煤灰 主要成分为Al2O3、SiO2及少量Fe2O3等
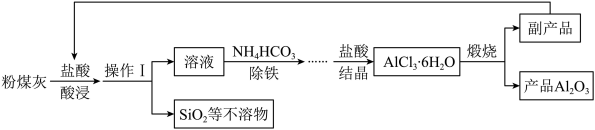
主要成分为Al2O3、SiO2及少量Fe2O3等 也是一种可利用的资源。以粉煤灰为原料制Al2O3的部分工艺流程如图:
也是一种可利用的资源。以粉煤灰为原料制Al2O3的部分工艺流程如图:
【资料】 ①SiO2既不溶于水也不溶于酸
②煅烧时发生的反应为:2AlCl3·6H2O Al2O3 + 6HCl + 9H2O
Al2O3 + 6HCl + 9H2O
(1)操作Ⅰ的名称是____________ 。
(2)写出“酸浸”步骤中盐酸与Al2O3发生反应的化学方程式__________ 。
(3)“除铁”时发生的反应为FeCl3+3NH4HCO3=3NH4Cl+X+3CO2↑,X的化学式为________ 。
(4)流程中可循环利用的物质为________ 。
(5)向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热充分反应后冷却、过滤得到滤渣和滤液。
①在滤液中加入一枚洁净的铁钉,发现铁钉表面无任何变化,则滤液中一定没有的阳离子是____ (填离子符号)。
②向滤渣中再滴入稀硫酸产生气泡,则滤渣中一定含有_________ (填名称)。反应的化学方程式为__________ 。
 主要成分为Al2O3、SiO2及少量Fe2O3等
主要成分为Al2O3、SiO2及少量Fe2O3等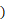 也是一种可利用的资源。以粉煤灰为原料制Al2O3的部分工艺流程如图:
也是一种可利用的资源。以粉煤灰为原料制Al2O3的部分工艺流程如图: 
【资料】 ①SiO2既不溶于水也不溶于酸
②煅烧时发生的反应为:2AlCl3·6H2O
 Al2O3 + 6HCl + 9H2O
Al2O3 + 6HCl + 9H2O(1)操作Ⅰ的名称是
(2)写出“酸浸”步骤中盐酸与Al2O3发生反应的化学方程式
(3)“除铁”时发生的反应为FeCl3+3NH4HCO3=3NH4Cl+X+3CO2↑,X的化学式为
(4)流程中可循环利用的物质为
(5)向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热充分反应后冷却、过滤得到滤渣和滤液。
①在滤液中加入一枚洁净的铁钉,发现铁钉表面无任何变化,则滤液中一定没有的阳离子是
②向滤渣中再滴入稀硫酸产生气泡,则滤渣中一定含有
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】兴趣小组的同学对一包白色粉末的成分展开了探究,已知成分可能是硫酸镁、氯化钠、碳酸钙和氢氧化钠中的一种或几种。
步骤1:取24g白色粉末,加入足量水,充分溶解后过滤,得到白色沉淀9.8g和无色滤液。
步骤2:向步骤1所得白色沉淀中加入过量的稀盐酸,沉淀完全溶解,产生1.76g气体。
步骤3:向步骤1所得无色滤液中加入过量的氯化钡溶液,充分反应后过滤,得到白色沉淀和无色滤液。
步骤4:向步骤3所得无色滤液中加入适量的硝酸银溶液,有白色沉淀产生。
结合以上探究过程,请你回答:
(1)步骤1中,白色沉淀的成分是_______ 。
(2)步骤3中,产生白色沉淀的方程式是_______ ,步骤4中,产生的白色沉淀是_______ 。
(3)该白色粉末中一定含有_______ 。
步骤1:取24g白色粉末,加入足量水,充分溶解后过滤,得到白色沉淀9.8g和无色滤液。
步骤2:向步骤1所得白色沉淀中加入过量的稀盐酸,沉淀完全溶解,产生1.76g气体。
步骤3:向步骤1所得无色滤液中加入过量的氯化钡溶液,充分反应后过滤,得到白色沉淀和无色滤液。
步骤4:向步骤3所得无色滤液中加入适量的硝酸银溶液,有白色沉淀产生。
结合以上探究过程,请你回答:
(1)步骤1中,白色沉淀的成分是
(2)步骤3中,产生白色沉淀的方程式是
(3)该白色粉末中一定含有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
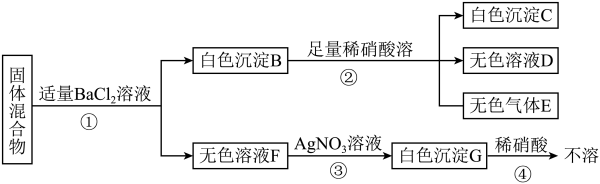
【推荐3】现有一包固体混合物A,可能含有NaC1、Na2SO4、NaNO3、CuSO4、Na2CO3等五种物质中的一种或几种。取少量A作如下实验,现象如图所示(设过程中所能发生的反应都恰好完全进行)。
(1)生成无色气体E的化学方程式为______ 。
(2)在溶液D中,肯定存在的阳离子是(写离子符号)______ 。
(3)写出步骤③中发生的一个化学反应方程式______ 。
(4)固体混合物A中一定存在物质是(写化学式)______ ,一定不存在的物质是(写化学式)______ 。
(5)若要确定是否含有NaCl,可将步骤①的BaCl2溶液换为______ 溶液。
(1)生成无色气体E的化学方程式为
(2)在溶液D中,肯定存在的阳离子是(写离子符号)
(3)写出步骤③中发生的一个化学反应方程式
(4)固体混合物A中一定存在物质是(写化学式)
(5)若要确定是否含有NaCl,可将步骤①的BaCl2溶液换为
您最近一年使用:0次