下图为氯化钠、碳酸钠在水中的溶解度曲线。请回答下列问题:
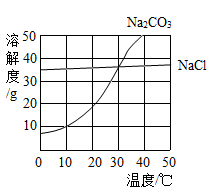
(1)30℃时,氯化钠的溶解度______ 碳酸钠的溶解度(填写“>”、“<”或“=”);
(2)10℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是______________ 溶液;
(3)将30℃时相同质量的两种物质的饱和溶液,分别降温到10℃,晶体析出较多的是____ 。
(4)要使接近饱和的碳酸钠溶液变为饱和溶液,可采取的一种措施是_____________ 。
(5) 如下图所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是________ (填字母序号)。
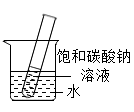
A. 氢氧化钠 B. 生石灰 C. 硝酸铵 D. 浓硫酸

(1)30℃时,氯化钠的溶解度
(2)10℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是
(3)将30℃时相同质量的两种物质的饱和溶液,分别降温到10℃,晶体析出较多的是
(4)要使接近饱和的碳酸钠溶液变为饱和溶液,可采取的一种措施是
(5) 如下图所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是

A. 氢氧化钠 B. 生石灰 C. 硝酸铵 D. 浓硫酸
2012·广东广州·中考模拟 查看更多[1]
(已下线)2012年广东省广州市花都区中考一模化学试卷
更新时间:2016-11-28 10:07:35
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2023年“世界水日”的主题为“Accelerating Change”(加速变革)
(1)我国是淡水资源非常有限的国家,爱护水资源是每个公民的责任和义务。下列行为属于浪费水的是___________(填字母)。
(2)自来水厂对天然水净化处理得到自来水的过程中,下列操作:
a.过滤 b.吸附 c.消毒 d.蒸馏,其中没有用到的是___________ (填字母)。
(3)下列各组物质,只用水就可以鉴别的是___________(填字母)。
(1)我国是淡水资源非常有限的国家,爱护水资源是每个公民的责任和义务。下列行为属于浪费水的是___________(填字母)。
| A.洗手擦香皂时不关上水龙头 | B.用淘米水浇花 |
| C.用洗衣水冲厕所 | D.用自来水不断为西瓜冲水降温 |
a.过滤 b.吸附 c.消毒 d.蒸馏,其中没有用到的是
(3)下列各组物质,只用水就可以鉴别的是___________(填字母)。
| A.氯化钾、碳酸钙、硫酸钾 | B.氯化钠、氢氧化钠、硝酸铵 |
| C.氯化钠、硫酸铜、高锰酸钾 | D.酒精、花生油、菜籽油 |
您最近一年使用:0次
【推荐2】“珍爱生命,健康生活”。家庭小药箱在关键时候可以发挥作用。
(1)“美林”的主要成分是布洛芬(化学式为C13H18O2),布洛芬分子中碳、氧原子的个数比为___________ 。
(2)某种创可贴使用时,按中间凸起的小囊区,让内部的水与___________ (填“NaOH”或“NH4NO3”)混合,使温度降低,达到快速止血的作用。

(3)“补液盐”通常含有氯化钠、氯化钾、碳酸氢钠、葡萄糖等。上述物质中含有的金属元素为___________ (填元素符号,写一种即可)。
(4)氢氧化镁片是一种治疗胃病的药物,它能中和胃里过多的胃酸,其反应的化学方程式是___________ 。
(1)“美林”的主要成分是布洛芬(化学式为C13H18O2),布洛芬分子中碳、氧原子的个数比为
(2)某种创可贴使用时,按中间凸起的小囊区,让内部的水与

(3)“补液盐”通常含有氯化钠、氯化钾、碳酸氢钠、葡萄糖等。上述物质中含有的金属元素为
(4)氢氧化镁片是一种治疗胃病的药物,它能中和胃里过多的胃酸,其反应的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下表为氯化钠和硝酸钾的溶解度(单位:克/100克水):
(1)20℃时,氯化钠的溶解度为_______________ 。
(2)溶解度受温度影响较大的物质是_______________ 。
(3)20℃时,将20g氯化钠放入50g水中,充分溶解,所得溶液为_______________ (选填“饱和溶液”和“不饱和溶液”),溶液质量为_______________ g;
(4)20℃时,向20gKNO3固体不断加水,在下图中画出所得溶液与加水的质量关系图像_______________ 。

(5)混有少量氯化钠的硝酸钾样品100g,经测定其中含氯化钠约5%,为了得到纯净且质量较多的硝酸钾,甲乙丙同学分别设计了如下三种实验方案提纯硝酸钾:
甲方案:20℃时,将固体混合物加入15mL水中,并充分搅拌、溶解、过滤;
乙方案:加入100mL水中溶解,加热蒸发至有晶体析出停止加热,冷却至20℃,过滤;
丙方案:20℃时,投入10mL水中,加热至80℃,趁热过滤。
请你选出合适的方案并简述理由:___________________________ 。
| 温度 物质 | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ | 100℃ |
| 氯化钠 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | 39.2 |
| 硝酸钾 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 246 |
(1)20℃时,氯化钠的溶解度为
(2)溶解度受温度影响较大的物质是
(3)20℃时,将20g氯化钠放入50g水中,充分溶解,所得溶液为
(4)20℃时,向20gKNO3固体不断加水,在下图中画出所得溶液与加水的质量关系图像

(5)混有少量氯化钠的硝酸钾样品100g,经测定其中含氯化钠约5%,为了得到纯净且质量较多的硝酸钾,甲乙丙同学分别设计了如下三种实验方案提纯硝酸钾:
甲方案:20℃时,将固体混合物加入15mL水中,并充分搅拌、溶解、过滤;
乙方案:加入100mL水中溶解,加热蒸发至有晶体析出停止加热,冷却至20℃,过滤;
丙方案:20℃时,投入10mL水中,加热至80℃,趁热过滤。
请你选出合适的方案并简述理由:
您最近一年使用:0次
【推荐2】跨学科研究小组制定了以“水和溶液”为主题的研究项目。
(1)水质净化。自制简易净水器可以选择去底倒置的可乐瓶作为容器,现提供四种材料。

其中④号材料的作用是______ 。容器中 a、b 处应放置的材料(材料间用纱布隔开)最合理的顺序为______ (选填“①②”或“②①”)。
(2)配制溶液。20℃时,取一包硫酸铜粉末(密封包装)加入 100g 水中,充分溶解后发现有固体剩余。
①此时该溶液为______ (填“饱和”或“不饱和”)溶液。
②若采用加热方法(忽略水蒸发)使剩余固体完全溶解后,溶液的溶质质量分数将______ (填“变大”“变小”或“不变”)。
③已知:20℃时,硫酸铜的溶解度为 20.5 g。若再加入 100g 水可使剩余固体完全溶解(忽略温度变化),可推测该包硫酸铜粉末质量 m 的取值范围是______ 。
④不宜在铁制容器中配制硫酸铜溶液的原因是______ (用化学方程式表示)。
(1)水质净化。自制简易净水器可以选择去底倒置的可乐瓶作为容器,现提供四种材料。

其中④号材料的作用是
(2)配制溶液。20℃时,取一包硫酸铜粉末(密封包装)加入 100g 水中,充分溶解后发现有固体剩余。
①此时该溶液为
②若采用加热方法(忽略水蒸发)使剩余固体完全溶解后,溶液的溶质质量分数将
③已知:20℃时,硫酸铜的溶解度为 20.5 g。若再加入 100g 水可使剩余固体完全溶解(忽略温度变化),可推测该包硫酸铜粉末质量 m 的取值范围是
④不宜在铁制容器中配制硫酸铜溶液的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】水是一种常见的溶剂,也是重要的资源。
(1)农业上用 NaCl 固体和一定质量的水配制 50g16%NaCl 溶液用于选种,配制过程中需要用到的玻璃仪器有烧杯、量筒、滴管和________ (填仪器名称)。
(2)“生命吸管”将太湖水转变为饮用水的过程示意图如下:

①“活性炭”可将太湖水中色素和异味除去,这是利用活性炭的_____ (填“物理”或“化学”)性质。
②“离子交换树脂”将硬水软化的反应之一是: ,由此可知一个 Ca2+可交换出
,由此可知一个 Ca2+可交换出________ 个 Na+。
(3)天宫课堂“点水成冰”实验中用到了醋酸钠,20℃时按下表配制醋酸钠的溶液(在标有序号的试管中,按表中的数据加入醋酸钠和水,再充分振荡)。
已知:20℃时醋酸钠溶解度为 124g,60℃时,醋酸钠溶解度为 140g。则下列说法正确的是_____(填字母)。
(1)农业上用 NaCl 固体和一定质量的水配制 50g16%NaCl 溶液用于选种,配制过程中需要用到的玻璃仪器有烧杯、量筒、滴管和
(2)“生命吸管”将太湖水转变为饮用水的过程示意图如下:

①“活性炭”可将太湖水中色素和异味除去,这是利用活性炭的
②“离子交换树脂”将硬水软化的反应之一是:
 ,由此可知一个 Ca2+可交换出
,由此可知一个 Ca2+可交换出(3)天宫课堂“点水成冰”实验中用到了醋酸钠,20℃时按下表配制醋酸钠的溶液(在标有序号的试管中,按表中的数据加入醋酸钠和水,再充分振荡)。
| 序号 | 试管① | 试管② | 试管③ | 试管④ |
| 醋酸钠的质量/g | 10 | 60 | 140 | 160 |
| 水的质量/g | 10 | 50 | 100 | 100 |
| A.试管③和④中的溶液为饱和溶液 |
| B.试管①和②溶液中溶质质量分数相等 |
| C.试管③中溶液里溶质和溶剂的质量比为 7:5 |
| D.将试管④升温至 60℃,溶质质量分数增大(不考虑水分蒸发) |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下图是甲、乙两种固体物质的溶解度曲线。

(1)t1℃时,甲的溶解度____ 乙的溶解度(选填“大于”“等于”或“小于”);
(2)要使接近饱和的甲溶液变为饱和溶液,可采取的方法是_______ (只填一种);
(3)甲、乙各Wg分别加入到两只盛有100g水的烧杯中,充分搅拌,在t3℃时所得乙溶液为_______ 溶液(选填“饱和”或“不饱和”)。

(1)t1℃时,甲的溶解度
(2)要使接近饱和的甲溶液变为饱和溶液,可采取的方法是
(3)甲、乙各Wg分别加入到两只盛有100g水的烧杯中,充分搅拌,在t3℃时所得乙溶液为
您最近一年使用:0次
【推荐2】溶液在生产生活中有重要的用途。
(1)甲、乙两种不含结晶水的固体的溶解度曲线如图所示。

①图中M点的含义是______ 。
②N点对应的甲溶液中溶质与溶液的质量比为______ ;当温度升高后,该溶液中溶质的质量分数将_____________ (填“增大”、“减小”或“不变”)。
(2)实验室现有质量分数为98%的浓硫酸,用该浓硫酸50g配制质量分数为20%的稀硫酸,需要水的质量是______ ,计算依据是______ 。
(1)甲、乙两种不含结晶水的固体的溶解度曲线如图所示。

①图中M点的含义是
②N点对应的甲溶液中溶质与溶液的质量比为
(2)实验室现有质量分数为98%的浓硫酸,用该浓硫酸50g配制质量分数为20%的稀硫酸,需要水的质量是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】我国化学家侯德榜创立的“侯氏制碱法”是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl。NH4Cl和NaCl的溶解度曲线如图所示。

(1)t2℃时NaCl的溶解度_____ NH4Cl的溶解度(填“>”、“<”或“=”)。
(2)t2℃时,向90g水中加入45gNH4Cl,经充分溶解,所得溶液中溶质与溶剂的质量之比为_____ 。
(3)将t2℃时NH4Cl饱和溶液的温度降到t1℃,溶液中NH4Cl的质量分数会_____ (填“变大”“变小”“不变”之一)。
(4)t1℃时,一小试管内盛有NH4Cl的饱和溶液,试管底部还存有少许NH4Cl固体,将小试管放入盛有水的烧杯中,然后将多量的NaOH固体加入烧杯的水中,观察到小试管内的固体物质逐渐溶解,原因是_____ 。
(5)碳酸氢钠受热会分解为碳酸钠、二氧化碳和水,写出该反应方程式:_____ 。
(6)将15克含有碳酸钠、碳酸氢钠的混合物加热完全反应,反应后的固体剩余物与200克质量分数为3.65%的稀盐酸混合后恰好完全反应,则反应所得二氧化碳的质量为多少克?

(1)t2℃时NaCl的溶解度
(2)t2℃时,向90g水中加入45gNH4Cl,经充分溶解,所得溶液中溶质与溶剂的质量之比为
(3)将t2℃时NH4Cl饱和溶液的温度降到t1℃,溶液中NH4Cl的质量分数会
(4)t1℃时,一小试管内盛有NH4Cl的饱和溶液,试管底部还存有少许NH4Cl固体,将小试管放入盛有水的烧杯中,然后将多量的NaOH固体加入烧杯的水中,观察到小试管内的固体物质逐渐溶解,原因是
(5)碳酸氢钠受热会分解为碳酸钠、二氧化碳和水,写出该反应方程式:
(6)将15克含有碳酸钠、碳酸氢钠的混合物加热完全反应,反应后的固体剩余物与200克质量分数为3.65%的稀盐酸混合后恰好完全反应,则反应所得二氧化碳的质量为多少克?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】根据所学知识,回答下列问题。
(1)铁锈的主要成分为Fe2O3,通常可以用稀盐酸将其除去。写出稀盐酸除去铁制品表面铁锈的反应化学方程式:_____________ ;
(2)市售硫酸多为98%的浓硫酸,实验室常将浓硫酸稀释成稀硫酸使用。现有浓硫酸100g要将其稀释成20%的稀硫酸,需要加水________ g;稀释操作时,必须将___________ ,否则会造成危险。
(1)铁锈的主要成分为Fe2O3,通常可以用稀盐酸将其除去。写出稀盐酸除去铁制品表面铁锈的反应化学方程式:
(2)市售硫酸多为98%的浓硫酸,实验室常将浓硫酸稀释成稀硫酸使用。现有浓硫酸100g要将其稀释成20%的稀硫酸,需要加水
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
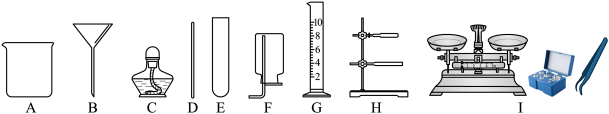
【推荐2】规范使用仪器是实验成功的保障,结合如图所示仪器,回答问题。
(1)加热少量液体需要的仪器有__ (填仪器序号),图中还缺少的仪器是__ 。
(2)若用仪器A和D稀释浓硫酸,则D的作用是___ ,若用仪器A和D进行过滤操作,还必须用到上述的一种玻璃仪器是__ (填名称)。
(3)要称量11.6g的氢氧化钠固体,应该选择的仪器有__ (填仪器名称),还必须用的仪器是__ (填名称)。
(4)下列测定稀硫酸pH的操作正确的是 (写字母序号)。

(1)加热少量液体需要的仪器有
(2)若用仪器A和D稀释浓硫酸,则D的作用是
(3)要称量11.6g的氢氧化钠固体,应该选择的仪器有
(4)下列测定稀硫酸pH的操作正确的是 (写字母序号)。
| A.将pH试纸直接插入稀硫酸中 | B.根据试纸显示的颜色估算出溶液的pH |
| C.用玻璃棒蘸取少量稀硫酸,滴在pH试纸上 | D.先将pH试纸用蒸馏水润湿 |
您最近一年使用:0次




