化学小组的同学在收集满CO2的集气瓶中放入燃烧的钠,钠继续燃烧,充分反应后生成黑色的碳和一种白色固体。
【作出猜想】白色固体的成分可能为:①氧化钠;②碳酸钠;③氧化钠和碳酸钠的混合物;④氢氧化钠;⑤碳酸氢钠。
请指出以上不合理的猜想是____________ 。
【查阅资料】氧化钠为白色粉末,能和水反应生成氢氧化钠。
【实验探究】取少量白色固体溶于水,将溶液分成两份,一份加入酚酞溶液,溶液变红;另一份先加入过量的CaC12溶液,出现白色沉淀,过滤,向滤液中滴加酚酞溶液,无明显现象。
【得出结论】白色固体的成分为_________ (填化学式)。钠在二氧化碳中燃烧的化学方程式为_________ 。
【作出猜想】白色固体的成分可能为:①氧化钠;②碳酸钠;③氧化钠和碳酸钠的混合物;④氢氧化钠;⑤碳酸氢钠。
请指出以上不合理的猜想是
【查阅资料】氧化钠为白色粉末,能和水反应生成氢氧化钠。
【实验探究】取少量白色固体溶于水,将溶液分成两份,一份加入酚酞溶液,溶液变红;另一份先加入过量的CaC12溶液,出现白色沉淀,过滤,向滤液中滴加酚酞溶液,无明显现象。
【得出结论】白色固体的成分为
更新时间:2020/09/07 12:47:30
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】在做“火龙生字“趣味实验时,先用毛笔蘸热饱和硝酸钾(KNO3)溶液在白纸上书写字母 “K”,晾干(白纸上出现硝酸钾晶体),再用带火星的木条接触字母“K”,白纸上写过字母的地方燃烧并迅速蔓延,留下“K”形的黑色痕迹(如下图)。为了弄清楚“火龙生字”的原因,兴趣小组同学进行了如下探究:
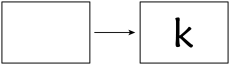
【提出问题】为什么附有硝酸钾晶体的地方遇火星燃烧?
【查阅资料】硝酸钾受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质.
【猜想与假设】硝酸钾受热分解生成的气体单质是什么?
猜想一:二氧化氮
猜想二:氮气
猜想三:氧气
猜想四:氢气
小明同学认为猜想一不正确,理由是___________________________ ,小芳同学认为猜想四不正确,理由是__________________________________________________ .
【设计实验】结合氮气与氧气的性质,设计简单的实验方案证明猜想二与猜想三的正确性,你设计的方案是_______________________________________________________________ ,可能观察到的现象是_____________________________________________________ 或___________________ 。
【解释与结论】通过实验证明猜想三正确,则硝酸钾受热分解的化学方程式是__________ ,白纸上写过字的地方遇火燃烧的原因是 ________________________________________________ 。

【提出问题】为什么附有硝酸钾晶体的地方遇火星燃烧?
【查阅资料】硝酸钾受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质.
【猜想与假设】硝酸钾受热分解生成的气体单质是什么?
猜想一:二氧化氮
猜想二:氮气
猜想三:氧气
猜想四:氢气
小明同学认为猜想一不正确,理由是
【设计实验】结合氮气与氧气的性质,设计简单的实验方案证明猜想二与猜想三的正确性,你设计的方案是
【解释与结论】通过实验证明猜想三正确,则硝酸钾受热分解的化学方程式是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】天然气的主要成分是甲烷(CH4),老师在课堂上播放甲烷燃烧实验的视频中玻璃导管口火焰呈黄色,始终未观察到蓝色火焰,化学兴趣小组的同学对甲烷的制取和燃烧现象展开了探究。
[提出问题)①实验室如何制取甲烷?②制取的甲烷燃烧火焰为什么呈黄色?
[查阅资料]①无水醋酸钠(CH4COONa)与碱石灰混合共热,加热过猛会生成丙酮。②丙酮,易溶于水,常温下为无色、易挥发液体,沸点56.33°C,燃烧时火焰呈黄色或橙色。③含钠元素的物质被灼烧时产生黄色火焰。
实验探究一 :探究无水醋酸钠与氢氧化钠的最佳质量比
[实验方案]分别将无水醋酸钠和碱石灰(氧化钙与氢氧化钠的质量比为1:1)研细、干燥,并将它们按不同比例充分混合装入试管中进行实验。记录五分钟收集到的甲烷体积作为实际产量,并计算产率,以产率高低作为选择最佳质量比的标准。相关数据如下表:
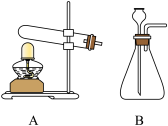
[问题分析]
(1)实验时,可以按图中_____ (选填“A”或“B”)组装发生装置。
(2)加热无水醋酸钠与碱石灰的混合物时,生成物中只有甲烷和碳酸钠,说明碱石灰中的氧化钙并未参与反应,理论依据是_____ 。无水醋酸钠与氢氧化钠发生反应的化学方程式是_____ 。
(3)分析表中数据可以得出的结论是______ 。
实验探究二:探究实验室制取的甲烷燃烧火焰呈黄色的原因
[提出猜想]
猜想一:玻璃中含有钠元素,甲烷燃烧时,玻璃管被灼烧产生黄色火焰。
猜想二:甲烷燃烧不充分而产生黄色火焰。
猜想三:______ 。
[进行实验]针对猜想,小浔和小阳分别进行下列实验:
[交流讨论]
(4)小章:根据小浔的实验现象,可以说明猜想一也不合理。他的理由是_______ 。
(5)小豫:根据小阳的实验方案及其现象,不足以说明加热无水醋酸钠和碱石灰制得的气体中混入了丙酮,导致该混合物燃烧时产生黄色火焰。因为反应物无水醋酸钠和碱石灰中______ 混入甲烷中,导致收集到的甲烷气体不纯,产生黄色火焰。
[提出问题)①实验室如何制取甲烷?②制取的甲烷燃烧火焰为什么呈黄色?
[查阅资料]①无水醋酸钠(CH4COONa)与碱石灰混合共热,加热过猛会生成丙酮。②丙酮,易溶于水,常温下为无色、易挥发液体,沸点56.33°C,燃烧时火焰呈黄色或橙色。③含钠元素的物质被灼烧时产生黄色火焰。
实验探究一 :探究无水醋酸钠与氢氧化钠的最佳质量比
[实验方案]分别将无水醋酸钠和碱石灰(氧化钙与氢氧化钠的质量比为1:1)研细、干燥,并将它们按不同比例充分混合装入试管中进行实验。记录五分钟收集到的甲烷体积作为实际产量,并计算产率,以产率高低作为选择最佳质量比的标准。相关数据如下表:
| 编号 | 无水醋酸钠(g) | 氢氧化钠(g) | 五分钟产量( mL) | 产率(%) |
| 1 | 2.5 | 1.0 | 384 | 68.57 |
| 2 | 2.5 | 1.50 | 476 | 69.79 |
| 3 | 2.5 | 1.75 | 438 | 64.22 |
| 4 | 2.5 | 2.00 | 435 | 63.78 |
| 5 | 2.5 | 2.25 | 402 | 58.94 |
| 6 | 2.5 | 2.50 | 396 | 58.06 |
| 7 | 2.5 | 2.75 | 360 | 52.78 |
| 8 | 2.5 | 3.00 | 304 | 44.57 |

[问题分析]
(1)实验时,可以按图中
(2)加热无水醋酸钠与碱石灰的混合物时,生成物中只有甲烷和碳酸钠,说明碱石灰中的氧化钙并未参与反应,理论依据是
(3)分析表中数据可以得出的结论是
实验探究二:探究实验室制取的甲烷燃烧火焰呈黄色的原因
[提出猜想]
猜想一:玻璃中含有钠元素,甲烷燃烧时,玻璃管被灼烧产生黄色火焰。
猜想二:甲烷燃烧不充分而产生黄色火焰。
猜想三:
[进行实验]针对猜想,小浔和小阳分别进行下列实验:
| 实验方案 | 实验现象 | 实验结论 | |
| 小浔 | 将已收集到的天然气用玻璃管导出,点燃并观察火焰颜色 | 导管口火焰呈蓝色,一段时间后,火焰略显黄色 | 猜想二不合理 |
| 小阳 | 先将加热无水醋酸钠和碱石灰制得的气体验纯并经冰水冷却后,再点燃(如图),观察火焰颜色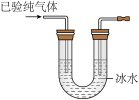 | 猜想三合理 | |
[交流讨论]
(4)小章:根据小浔的实验现象,可以说明猜想一也不合理。他的理由是
(5)小豫:根据小阳的实验方案及其现象,不足以说明加热无水醋酸钠和碱石灰制得的气体中混入了丙酮,导致该混合物燃烧时产生黄色火焰。因为反应物无水醋酸钠和碱石灰中
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】化学兴趣小组中某同学表演了“水能生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小李很感兴趣,于是,他和同学们进行探究:
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成;②反应过程中可能有热量放出
【实验装置】如图所示:
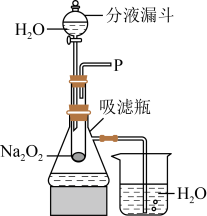
实验一:探究反应后生成的气体是什么?
①打开右装置图中分液漏斗的活塞,控制滴加液体的速度,其作用是______ ,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是______ 。
②实验中还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______ 。
实验二:继续探究反应后生成的另一种物质是什么?
①小张猜想另一种物质是Na2CO3小李认为不可能。小李的依据是______ 。
②在老师的指导下,小李取反应后所得的溶液于试管中,滴入无色酚酞溶液,发现酚酞溶液变红,老师告诉同学们,这说明溶液呈碱性,溶液中含有OH-。
【表达】由实验探究的结果,请写出过氧化钠和水反应的化学方程式______ 。
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成;②反应过程中可能有热量放出
【实验装置】如图所示:

实验一:探究反应后生成的气体是什么?
①打开右装置图中分液漏斗的活塞,控制滴加液体的速度,其作用是
②实验中还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:
实验二:继续探究反应后生成的另一种物质是什么?
①小张猜想另一种物质是Na2CO3小李认为不可能。小李的依据是
②在老师的指导下,小李取反应后所得的溶液于试管中,滴入无色酚酞溶液,发现酚酞溶液变红,老师告诉同学们,这说明溶液呈碱性,溶液中含有OH-。
【表达】由实验探究的结果,请写出过氧化钠和水反应的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组为探究碳酸氢钠的化学性质,设计如下图所示三个实验。
实验一:探究碳酸氢钠溶液的酸碱性。用pH试纸测得碳酸氢钠溶液的pH=9,由此得出结论是碳酸氢钠溶液呈_________ 。
实验二:探究碳酸氢钠是否与酸反应。取少量固体放入试管中,滴加足量的稀盐酸,观察到试管中的现象是__________ ,说明碳酸氢钠能与酸发生化学反应。
实验三:为探究碳酸氢钠的热稳定性。
(1)小组同学按如图进行实验。充分加热后,大试管口有水珠出现,试管内有白色固体残留,小试管中澄清石灰水变浑浊,说明碳酸氢钠受热易分解。实验结束后,先进行的操作是_________ (填选项字母)。

A.熄灭酒精灯 B.把导管从石灰水中拿出
(2)小组同学对实验三试管内残留的白色固体成分又进行了探究。
【提出问题】该固体的成分是什么?
【提出猜想】猜想一:NaOH 猜想二: Na2CO3猜想三:NaOH和Na2CO3
【实验验证】小明同学取少量加热后的固体产物于烧杯中,用足量蒸馏水溶解,再向溶液中滴入几滴酚酞液,溶液变红,由此他得出猜想一正确,但其他同学很快予以否定,否定的理由是__________ 。
为了进一步得出结论,小亮和小光同学分别取小明实验后的溶液于试管中,进行如下表所示实验。
根据上述实验结论,写出碳酸氢钠受热分解的化学方程式__________ 。
【反思评价】小组同学认为,小光的实验操作和现象无法确定猜想二成立,理由是_________ 。
实验一:探究碳酸氢钠溶液的酸碱性。用pH试纸测得碳酸氢钠溶液的pH=9,由此得出结论是碳酸氢钠溶液呈
实验二:探究碳酸氢钠是否与酸反应。取少量固体放入试管中,滴加足量的稀盐酸,观察到试管中的现象是
实验三:为探究碳酸氢钠的热稳定性。
(1)小组同学按如图进行实验。充分加热后,大试管口有水珠出现,试管内有白色固体残留,小试管中澄清石灰水变浑浊,说明碳酸氢钠受热易分解。实验结束后,先进行的操作是

A.熄灭酒精灯 B.把导管从石灰水中拿出
(2)小组同学对实验三试管内残留的白色固体成分又进行了探究。
【提出问题】该固体的成分是什么?
【提出猜想】猜想一:NaOH 猜想二: Na2CO3猜想三:NaOH和Na2CO3
【实验验证】小明同学取少量加热后的固体产物于烧杯中,用足量蒸馏水溶解,再向溶液中滴入几滴酚酞液,溶液变红,由此他得出猜想一正确,但其他同学很快予以否定,否定的理由是
为了进一步得出结论,小亮和小光同学分别取小明实验后的溶液于试管中,进行如下表所示实验。
| 同学 | 实验操作 | 现象 | 结论 |
| 小亮 | 滴加过量氯化钙溶液,振荡,静置 | 试管中 | 猜想二成立 |
| 小光 | 滴加过量稀盐酸,振荡,静置 | 试管中产生气泡,溶液由红色变成无色 | 猜想二成立 |
【反思评价】小组同学认为,小光的实验操作和现象无法确定猜想二成立,理由是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组在探究物质的性质实验活动中进行了如图所示的实验。
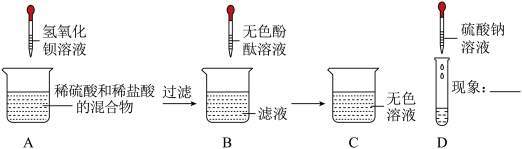
A烧杯中生成白色沉淀的化学反应方程式为_______ ,B烧杯中滤液一定不含的离子是______ 。小组同学对C烧杯中溶液的成分产生了兴趣。进行了下面探究。
【提出问题】C烧杯溶液中含有什么离子? (不考虑酚酞)
【活动探究】
甲同学用试管取少量C中溶液,向试管中滴入硫酸钠溶液,观察到______ ,分析出溶液中一定有Ba2+存在。
乙同学继续了甲同学的实验,他继续向试管中加入一种试剂,观察到了明显的实验的现象,得出结论:乙同学加入的试剂可能是_______ 。通过以上实验探究你认为溶液中含有的离子为______ 。
【总结与反思】通过上述探究过程可知,在分析和探究反应后溶液中离子成分时,首先可根据_____ 来推断出:不能与其它离子反应的离子一定存在,然后加入适当的试剂证明______ 是否存在,才能得出正确结论。

A烧杯中生成白色沉淀的化学反应方程式为
【提出问题】C烧杯溶液中含有什么离子? (不考虑酚酞)
【活动探究】
甲同学用试管取少量C中溶液,向试管中滴入硫酸钠溶液,观察到
乙同学继续了甲同学的实验,他继续向试管中加入一种试剂,观察到了明显的实验的现象,得出结论:乙同学加入的试剂可能是
【总结与反思】通过上述探究过程可知,在分析和探究反应后溶液中离子成分时,首先可根据
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
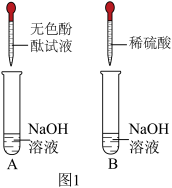
【推荐3】九年级同学在化学实验操作训练中,进行了氢氧化钠和氢氧化钙溶液的鉴别实验。为进一步探究氢氧化钠的化学性质,做了以下实验:
(1)A试管中的现象是_____ 。
为探究B试管中反应后溶液中溶质的成分,同学们进行了以下探究。
【猜想与假设】
(2)猜想一:Na2SO4
猜想二:Na2SO4、H2SO4
猜想三:_______ 。
(3)完成并记录以下实验:
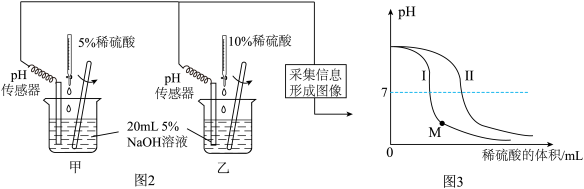
为探究氢氧化钠溶液与稀硫酸反应过程中pH的变化,甲、乙两组同学按图2所示装置进行实验,测定出溶液pH变化如图3所示。
_______ (填“I”或“Ⅱ”)。若取M点对应溶液滴加紫色石蕊试液,现象是_____ 。
(5)氢氧化钠溶液久置在空气中会变质,其原因是____________ (用化学方程式表示);向部分变质的氢氧化钠溶液中加入适量_____ 溶液可除去杂质。
(1)A试管中的现象是
为探究B试管中反应后溶液中溶质的成分,同学们进行了以下探究。
【猜想与假设】
(2)猜想一:Na2SO4
猜想二:Na2SO4、H2SO4
猜想三:
(3)完成并记录以下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量B试管中反应后的溶液,滴加碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
| ②另取少量B试管中反应后的溶液,滴加硝酸镁溶液 | 猜想一不成立,猜想三成立 |
为探究氢氧化钠溶液与稀硫酸反应过程中pH的变化,甲、乙两组同学按图2所示装置进行实验,测定出溶液pH变化如图3所示。
(5)氢氧化钠溶液久置在空气中会变质,其原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
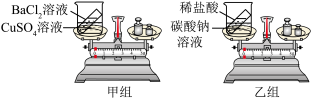
【推荐1】在实验室开放日,为验证质量守恒定律,甲乙两组同学分别设计了以下实验,并进行了规范的操作和细致的观察。请参与并完成相关问题:
【进行实验】
(1)甲组同学在实验过程中发现,化学反应前后天平平衡,成功验证了质量守恒定律,其化学方程式为____________________ 。
(2)乙组同学在实验过程中发现天平指针向右倾斜,其原因是_____________________ 。此反应______________ (选填“遵循”或“不遵循”)质量守恒定律。
【实验结论】
(3)在验证质量守恒定律时,对于有气体参加或生成的化学反应,一定要在_____ 装置中进行。
【发现问题】实验过后,两组同学对乙组烧杯中的废液进行了探究。废液中所含溶质是什么?
【猪想与假设】
(4)猜想Ⅰ:只有NaCl
猜想Ⅱ:NaCl、Na2CO3和HCl
猜想Ⅲ:NaCl和HCl
猜想Ⅳ:______
【交流讨论】
(5)经过讨论,甲组问学认为,猜想Ⅱ是错误的,原因是_____ (用化学方程式回答)。
【实验与结论】
(6)甲组同学先将少量废液滴入试管中,然后滴入酚酞溶液,现象为________ ,原因是____________________ ,则猜想Ⅳ正确。乙组同学将少量废液滴入试管中,然后滴入________ 溶液,现象为产生白色沉淀,则猜想Ⅳ正确。
【拓展与应用】
(7)若想验证猜想Ⅲ正确,不能选择的试剂是 。
(8)若猜想Ⅲ正确,想得到废液中的氯化钠固体,根据盐酸的性质,无须另加试剂,只需对废液进行_______ 操作即可。
【进行实验】
(1)甲组同学在实验过程中发现,化学反应前后天平平衡,成功验证了质量守恒定律,其化学方程式为
(2)乙组同学在实验过程中发现天平指针向右倾斜,其原因是
【实验结论】
(3)在验证质量守恒定律时,对于有气体参加或生成的化学反应,一定要在
【发现问题】实验过后,两组同学对乙组烧杯中的废液进行了探究。废液中所含溶质是什么?
【猪想与假设】
(4)猜想Ⅰ:只有NaCl
猜想Ⅱ:NaCl、Na2CO3和HCl
猜想Ⅲ:NaCl和HCl
猜想Ⅳ:
【交流讨论】
(5)经过讨论,甲组问学认为,猜想Ⅱ是错误的,原因是
【实验与结论】
(6)甲组同学先将少量废液滴入试管中,然后滴入酚酞溶液,现象为
【拓展与应用】
(7)若想验证猜想Ⅲ正确,不能选择的试剂是 。
| A.紫色石蕊溶液 | B.铁粉 | C.氢氧化钠溶液 | D.碳酸钾溶液 |
(8)若猜想Ⅲ正确,想得到废液中的氯化钠固体,根据盐酸的性质,无须另加试剂,只需对废液进行
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠和氯化铵(NH4Cl),再加热碳酸氢钠即可制得纯碱(Na2CO3)。某化学兴趣小组对纯碱的一些性质及用途开展了以下探究。
【初步探究】“侯氏制碱法”原理中,饱和氯化钠溶液吸收的两种气体是_____ 、_____ (写化学式),写出碳酸氢钠受热分解的化学方程式:_____ 。
【继续探究】为了进一步了解Na2CO3溶液呈碱性的原因,小组同学进行了以下实验。
【查阅资料】①Na2CO3溶液呈碱性,是因为溶液中存在较多的OH-。
②Na2CO3在水中全部解离出Na+和 。
。
③CaCl2溶液呈中性,Ca2+、Cl-对溶液的酸碱性没有影响。
④碳酸氢钠溶液显碱性。
【猜想假设】猜想一:_____ 。
猜想二:Na+与H2O作用,产生较多的OH-,使溶液呈碱性。
猜想三: 和H2O作用,产生较多的OH-,使溶液呈碱性。
和H2O作用,产生较多的OH-,使溶液呈碱性。
【实验探究】
【结论与拓展】结合以上探究,运用所学知识,并在老师的指导下,小组同学得知 和H2O作用,除了产生较多的OH-,还应该产生另一种阴离子,请写出该阴离子的符号:
和H2O作用,除了产生较多的OH-,还应该产生另一种阴离子,请写出该阴离子的符号:_____ 。
【深入探究】探究纯碱的用途
【查阅资料】Na2CO3可用于生产洗涤剂,广泛用于生活洗涤、酸类中和以及食品加工等。Na2CO3溶液呈碱性,可清洗油污,溶液碱性越强,去油污效果越好。
【实验探究】兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。
用不同温度的水,配制溶质质量分数分别为2%、6%和10%的Na2CO3溶液,并测定溶液pH,记录数据如下表:
【实验结论】
(1)实验①④⑦对比,可得出的结论是_____ 。
(2)要证明温度对Na2CO3溶液的碱性的影响,可选择的3个实验的编号是_____ 。
【拓展应用】
(3)下列物质可用于去油污的是_____ 。(填字母序号)
A.NaCl B.NaOH C.CaCl2 D.K2CO3
【初步探究】“侯氏制碱法”原理中,饱和氯化钠溶液吸收的两种气体是
【继续探究】为了进一步了解Na2CO3溶液呈碱性的原因,小组同学进行了以下实验。
【查阅资料】①Na2CO3溶液呈碱性,是因为溶液中存在较多的OH-。
②Na2CO3在水中全部解离出Na+和
 。
。③CaCl2溶液呈中性,Ca2+、Cl-对溶液的酸碱性没有影响。
④碳酸氢钠溶液显碱性。
【猜想假设】猜想一:
猜想二:Na+与H2O作用,产生较多的OH-,使溶液呈碱性。
猜想三:
 和H2O作用,产生较多的OH-,使溶液呈碱性。
和H2O作用,产生较多的OH-,使溶液呈碱性。【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| a.向试管中加入一定量的 蒸馏水滴入2滴酚酞溶液 | 溶液无明显变化猜 | 想一不成立 |
| b. | 溶液无明显变化 | 想二不成立 |
| c.①向试管中加入一定量的 Na2CO3溶液滴入2滴酚酞溶液。 ②往①所得溶液中逐滴加入CaCl2溶液至过量 | ①溶液由无色变红色② | 猜想三成立 |
 和H2O作用,除了产生较多的OH-,还应该产生另一种阴离子,请写出该阴离子的符号:
和H2O作用,除了产生较多的OH-,还应该产生另一种阴离子,请写出该阴离子的符号:【深入探究】探究纯碱的用途
【查阅资料】Na2CO3可用于生产洗涤剂,广泛用于生活洗涤、酸类中和以及食品加工等。Na2CO3溶液呈碱性,可清洗油污,溶液碱性越强,去油污效果越好。
【实验探究】兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。
用不同温度的水,配制溶质质量分数分别为2%、6%和10%的Na2CO3溶液,并测定溶液pH,记录数据如下表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
| 溶液温度(℃) | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 40 | 70 |
| 溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
(1)实验①④⑦对比,可得出的结论是
(2)要证明温度对Na2CO3溶液的碱性的影响,可选择的3个实验的编号是
【拓展应用】
(3)下列物质可用于去油污的是
A.NaCl B.NaOH C.CaCl2 D.K2CO3
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】某化学兴趣小组的同学在做氢氧化钙与盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应。于是他们对反应后溶液中的溶质大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告。
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性
(1)【猜想与假设】猜想Ⅰ:溶液中的溶质只有_____________________ ;
猜想Ⅱ:溶液中的溶质有CaCl2、HCl;
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2;
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl。
(2)请写出该反应的化学方程式________________________________ 。经过讨论,同学们直接得出猜想____ 是不正确的。为了验证余下的哪一种猜想是正确的,同学们又做了以下实验。
(3)【进行实验】
(4)产生气泡的化学方程式为_____________________ 。
(5)还可以单独用来证明上述正确的猜想的物质是:( )
A.Fe2O3 B.紫色石蕊溶液 C.无色酚酞溶液 D.锌粒 E.氢氧化钠溶液
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性
(1)【猜想与假设】猜想Ⅰ:溶液中的溶质只有
猜想Ⅱ:溶液中的溶质有CaCl2、HCl;
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2;
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl。
(2)请写出该反应的化学方程式
(3)【进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量反应后的溶液于试管中,滴加酚酞溶液 | | 猜想Ⅲ不正确 |
| ②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钙 | 有气泡产生 | 猜想 猜想 |
(4)产生气泡的化学方程式为
(5)还可以单独用来证明上述正确的猜想的物质是:
A.Fe2O3 B.紫色石蕊溶液 C.无色酚酞溶液 D.锌粒 E.氢氧化钠溶液
您最近一年使用:0次



