小宇用配制的10%的CuSO4溶液测定一瓶NaOH溶液中溶质的质量分数。
(1)下图是配制CuSO4溶液的操作过程,正确的顺序是_________(填序号)。
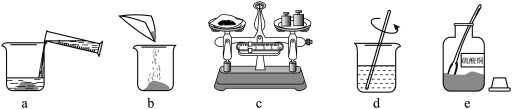
(2)取NaOH溶液25g,向其中加入10%的CuSO4溶液40g时恰好完全反应。则NaOH溶液中溶质的质量分数为______。
(1)下图是配制CuSO4溶液的操作过程,正确的顺序是_________(填序号)。

(2)取NaOH溶液25g,向其中加入10%的CuSO4溶液40g时恰好完全反应。则NaOH溶液中溶质的质量分数为______。
2014·陕西·中考真题 查看更多[8]
陕西省2014届中考化学试题2020年陕西省西安市碑林区西北工大附中中考二模化学试题(已下线)【万唯原创】2015年安徽省中考化学试题研究卷九年级题型研究题型五(已下线)【万唯原创】2018年陕西省中考化学试题研究卷九年级讲解册题型研究题型七(已下线)2014年陕西省初中毕业学业考试(已下线)【万唯原创】2015年山西省中考化学面对面卷讲解册第二部分重点专题突破专题七陕西省西安市铁一中学2018年中考三模化学试题2022年云南省昆明市安宁市中考二模化学试题
更新时间:2019-09-23 19:39:18
|
相似题推荐
计算题
|
较难
(0.4)
名校
【推荐1】化学实验小组同学用大理石(含杂质20%,杂质不含钙,且不参与反应)和稀盐酸制取CO2,将60g稀盐酸分成4份,依次加入装有一定量的大理石的容器中,收集到的气体总质量如下:
(1)实验_____(填序号)中酸被反应完全。
(2)m=_____。
(3)求所取大理石的质量(写出计算过程)。
(4)小申另取碳酸钠粉末和足量稀盐酸来制取CO2,请在下图中结合已有图像绘制出碳酸钠和足量稀盐酸反应的图像。

| 实验序号 | 1 | 2 | 3 | 4 |
| 加入稀盐酸质量/g | 15 | 30 | 45 | 60 |
| 产生CO2的质量/g | 1.1 | 2.2 | m | 3.52 |
(2)m=_____。
(3)求所取大理石的质量(写出计算过程)。
(4)小申另取碳酸钠粉末和足量稀盐酸来制取CO2,请在下图中结合已有图像绘制出碳酸钠和足量稀盐酸反应的图像。

您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某实验小组探究了温度对反应速率的影响。实验装置如图1所示,用纯金属锌和足量稀硫酸在不同温度下进行反应(见下表),实验中使用传感器装置测算生成氢气的质量,绘制氢气质量随时间变化的曲线,如2所示

(1)根据实验探究目的,从曲线a、b中,可得出结论是 。
(2)请计算实验Ⅰ条件下金属锌完全反应时,生成氢气的质量______(写出具体计算过程)。
(3)在图2中画出曲线c的大致位置及趋势_______。
(4)实验结束后,反应后得到的废液的处理方法是______。

| 实验编号 | 金属锌的质量(g) | 反应温度(℃) | 对应曲线 |
| Ⅰ | 3.25 | 30 | a |
| Ⅱ | 3.25 | 25 | b |
| Ⅲ | 3.25 | 20 | C(待绘制) |
(1)根据实验探究目的,从曲线a、b中,可得出结论是 。
(2)请计算实验Ⅰ条件下金属锌完全反应时,生成氢气的质量______(写出具体计算过程)。
(3)在图2中画出曲线c的大致位置及趋势_______。
(4)实验结束后,反应后得到的废液的处理方法是______。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】根据如图所示的实验过程和提供的数据进行计算:

(1)原混合物中NaCl的质量;
(2)AgNO3溶液的溶质质量分数。(精确到0.1%)

(1)原混合物中NaCl的质量;
(2)AgNO3溶液的溶质质量分数。(精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】为了测定含有氯化钾和碳酸钾的化肥中氯化钾的含量,取5g混合物和11.1%的氯化钙溶液做如下实验:
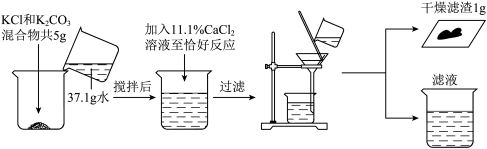
(1)写出上述反应的化学方程式_____;
(2)请列出能与氯化钙反应的物质的质量(x)的比例式_____;
(3)该化肥样品中氯化钾的纯度为_____;
(4)过滤后,最终滤液中溶质的质量分数为_____;
(5)若按上述过程用此化肥样品100t,可以生产出纯净的氯化钾_____t。

(1)写出上述反应的化学方程式_____;
(2)请列出能与氯化钙反应的物质的质量(x)的比例式_____;
(3)该化肥样品中氯化钾的纯度为_____;
(4)过滤后,最终滤液中溶质的质量分数为_____;
(5)若按上述过程用此化肥样品100t,可以生产出纯净的氯化钾_____t。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某中学化学课外活动小组对某工厂排放的含少量硫酸的废水进行抽样检测。取一定量的废水,用质量分数为1%的氢氧化钡溶液与之反应(其它物质不与氢氧化钡反应),当恰好完全反应时,消耗氢氧化钡溶液的质量为171g,过滤后,测得滤液的质量为268.67g。(不考虑过滤时滤液质量损失)(计算结果保留二位小数)【温馨提示:氢氧化钡与硫酸反应的化学方程式为:Ba(OH)2 + H2SO4 = BaSO4↓ + 2H2O】求:
⑴反生成沉淀的质量为多少?
⑵该工厂排放的废水中所含硫酸的溶质的质量分数为多少?
⑴反生成沉淀的质量为多少?
⑵该工厂排放的废水中所含硫酸的溶质的质量分数为多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】为测定某硝酸铵肥料的纯度(杂质中不含氮元素,但可溶于水),某化学兴趣小组设计了如图所示的实验。

反应过程中锥形瓶中溶液质量的变化如下表所示:(忽略氨气在水中的溶解)
(1)m的值为_______ 。
(2)硝酸铵恰好完全反应时,消耗氢氧化钠溶液的质量为_______ g。
(3)计算该硝酸铵肥料的纯度_______ 。(写出具体解答过程)
(4)该反应中氢氧化钠溶液的溶质质量分数为_______ ;若用氢氧化钠固体配制该溶液,在配制过程中,用量筒取水时俯视读数,会造成其溶质质量分数_______ (选填“偏大”、“不变”或“偏小”)。

反应过程中锥形瓶中溶液质量的变化如下表所示:(忽略氨气在水中的溶解)
| 氢氧化钠溶液的质量/g | 20 | 40 | 80 | 100 |
| 锥形瓶中溶液的质量/g | 218.3 | 236.6 | 274.9 | m |
(2)硝酸铵恰好完全反应时,消耗氢氧化钠溶液的质量为
(3)计算该硝酸铵肥料的纯度
(4)该反应中氢氧化钠溶液的溶质质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】普通黄铜是由铜和锌组成的二元黄铜,该金属材料具有强度高、耐腐蚀性强、可塑性强、耐磨性强等特点,其中,含锌量在36%~46%之间的黄铜性能最为优越,称为两相(α+β)黄铜,某研究性小组用14.6%稀盐酸测定黄铜的组成(所有计算结果精确到小数点后1位)。
(1)用36.5%浓盐酸配制100g 14.6%稀盐酸。
①计算:需要浓盐酸的质量为 g,需要水的质量为 g。
②量取浓盐酸和水:量取36.5%的浓盐酸时如果俯视读数,会导致所配溶液溶质质量分数 14.6%(填“大于”、“小于”或“等于”)。
(2)测定黄铜样品中铜的质量分数。称取黄铜样品20g,100g14.6%的稀盐酸分4次加入到样品中,测得数据记录如下表。
试通过计算回答:
①该黄铜中锌的质量分数为 。
②第二次反应结束时所得溶液中溶质的质量分数。(计算结果精确到0.1%)
(1)用36.5%浓盐酸配制100g 14.6%稀盐酸。
①计算:需要浓盐酸的质量为 g,需要水的质量为 g。
②量取浓盐酸和水:量取36.5%的浓盐酸时如果俯视读数,会导致所配溶液溶质质量分数 14.6%(填“大于”、“小于”或“等于”)。
(2)测定黄铜样品中铜的质量分数。称取黄铜样品20g,100g14.6%的稀盐酸分4次加入到样品中,测得数据记录如下表。
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀盐酸的质量(g) | 25 | 25 | 25 | 25 |
| 剩余固体质量(g) | 16.75 | 13.50 | 12.00 | 12.00 |
试通过计算回答:
①该黄铜中锌的质量分数为 。
②第二次反应结束时所得溶液中溶质的质量分数。(计算结果精确到0.1%)
您最近一年使用:0次
【推荐3】称取氯化钠和氯化钡的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入一定浓度的Na2SO4溶液至过量,当加入124.8gNa2SO4溶液时恰好完全反应,反应生成沉淀的质量与所加入的Na2SO4溶液的质量关系如下图所示。试回答下列问题:

小提示:固体混合物中的氯化钠不参与反应。
(1)完全反应后生成沉淀______ g。
(2)配制一定浓度的Na2SO4溶液时,在用量筒量取水的体积时仰视读数,其它操作正确,则所配溶液中溶质的质量分数________ (填“偏大”“没影响”“偏小”)
(3)如何证明所加入的Na2SO4溶液已过量:________ (写出操作、现象)。
(4)恰好完全反应时所得溶液中溶质的质量分数是多少?

小提示:固体混合物中的氯化钠不参与反应。
(1)完全反应后生成沉淀
(2)配制一定浓度的Na2SO4溶液时,在用量筒量取水的体积时仰视读数,其它操作正确,则所配溶液中溶质的质量分数
(3)如何证明所加入的Na2SO4溶液已过量:
(4)恰好完全反应时所得溶液中溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐1】取氯化钡和盐酸的混合溶液100g于烧杯中,向其中滴加碳酸钠溶液,产生气体或沉淀的质量与加入的碳酸钠溶液质量的关系如图所示,请回答:
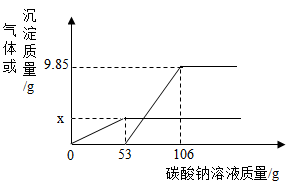
(1)产生沉淀的质量为_______________g。
(2)x的值为_______________。
(3)求所用碳酸钠溶液中溶质的质量分数(请写出计算过程)。

(1)产生沉淀的质量为_______________g。
(2)x的值为_______________。
(3)求所用碳酸钠溶液中溶质的质量分数(请写出计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐2】实验室有一部分被氧化成氧化镁的镁粉样品、未知浓度盐酸和40%的氢氧化钠溶液。兴趣小组同学为分析样品中金属镁的质量百分含量和计算盐酸的质量分株,进行如下探究:
(1)用盐酸溶解样品(样品混合均匀),测定生成氢气质量。实验数据如下表所示:
镁粉样品中金属镁的质量百分含量为_________________。
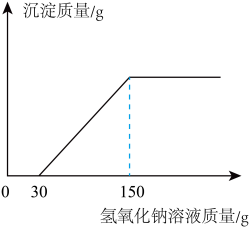
(2)向实验Ⅲ后的溶液中加入40%的氢氧化钠溶液,生成沉淀的质量随加入氢氧化钠溶液质量的变化关系如图所示。计算盐酸的质量分数为_______________。(写出计算过程)
(1)用盐酸溶解样品(样品混合均匀),测定生成氢气质量。实验数据如下表所示:
| 实验序号 | 所取样品质量(g) | 所加盐酸质量(g) | 生成氢气质量(g) |
| Ⅰ | 16.0 | 60.0 | 0.5 |
| Ⅱ | 16.0 | 130.0 | 1.0 |
| Ⅲ | 16.0 | 150.0 | 1.0 |
(2)向实验Ⅲ后的溶液中加入40%的氢氧化钠溶液,生成沉淀的质量随加入氢氧化钠溶液质量的变化关系如图所示。计算盐酸的质量分数为_______________。(写出计算过程)

您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】氢氧化钡可用作杀虫剂。实验室中有一瓶含有少量氢氧化钠的氢氧化钡样品,某化学兴趣小组的同学为测定该样品中氢氧化钡的质量分数,进行了以下实验:分别取120 g样品,平均分成6份加入烧杯中,分别加入80g水溶解,再加入碳酸钠溶液充分反应,对反应后的混合物进行如图所示的操作:

测得六组实验数据如下表所示,试计算:(钡的相对原子质量为137)
(1)m的值为______________。
(2)样品中氢氧化钡的质量分数____________。
(3)将恰好反应的液体配制成溶质质量分数为10%的氢氧化钠溶液以便实验室使用,需要再称取____________克氢氧化钠固体?

测得六组实验数据如下表所示,试计算:(钡的相对原子质量为137)
| 实验组数 | 第一组 | 第二组 | 第三组 | 第四组 | 第五组 | 第六组 |
| 加入碳酸钠溶液的质量/g | 25 | 50 | 75 | 100 | 125 | 150 |
| 天平示数/g | 3.94 | 7.88 | 11.82 | 15.76 | m | 19.70 |
(2)样品中氢氧化钡的质量分数____________。
(3)将恰好反应的液体配制成溶质质量分数为10%的氢氧化钠溶液以便实验室使用,需要再称取____________克氢氧化钠固体?
您最近一年使用:0次




