向Ba(OH)2溶液中先滴加一定量CuSO4溶液,直至沉淀质量为m克,再不断滴加H2SO4溶液。整个过程中,产生沉淀的质量与加入溶液的质量关系如图所示。回答下列问题
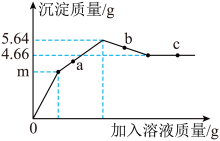
(1)a点对应溶液pH_____(选填“>”、“=”或“<”)7.
(2)取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是_____。
(3)通过计算确定m的值。

(1)a点对应溶液pH_____(选填“>”、“=”或“<”)7.
(2)取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是_____。
(3)通过计算确定m的值。
更新时间:2020-08-15 21:27:27
|
相似题推荐
计算题
|
较难
(0.4)
真题
名校
【推荐1】为测定硫酸钠和硫酸镁固体混合物中硫酸镁的质量分数。某同学取固体混合物26.2g,向其中加入219.6g水,使其完全溶解配制成混合溶液。将200g一定溶质质量分数的氢氧化钠溶液平均分成5等份,依次加入到上述混合溶液中,生成沉淀的质量与加入氢氧化钠溶液的质量关系如下表:
试分析计算。
(1)m的值为_____。
(2)固体混合物中硫酸镁的质量分数。_____(结果保留0.1%)
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数。_____
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 氢氧化钠溶液质量/g | 40 | 40 | 40 | 40 | 40 |
| 产生沉淀质量/g | 1.45 | 2.9 | m | 5.8 | 5.8 |
(1)m的值为_____。
(2)固体混合物中硫酸镁的质量分数。_____(结果保留0.1%)
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数。_____
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】化学课上,老师拿来一包氧化铜和铜的固体混合物,兴趣小组的同学取18g该混合物于烧杯中,将一定质量分数的稀硫酸平分5次加入到烧杯中,充分反应,记录相关数据如下表所示:
计算
(1)表中a的值为 。
(2)所用稀硫酸的溶质质量分数是多少?(写出计算过程,结果精确到0.1%)
(3)在坐标中画出加入稀硫酸的质量与某些物质物理量的相应曲线关系(纵坐标为某固体的质量),标注必要的数据。

| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入稀硫酸的质量/g | 30 | 60 | 90 | 120 | 150 |
| 剩余固体的质量/g | 16 | a | 12 | 11 | 11 |
(1)表中a的值为 。
(2)所用稀硫酸的溶质质量分数是多少?(写出计算过程,结果精确到0.1%)
(3)在坐标中画出加入稀硫酸的质量与某些物质物理量的相应曲线关系(纵坐标为某固体的质量),标注必要的数据。

您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,某化学小组同学进行如图所示的实验。请回答下列问题:

(1)实验中发生反应的化学方程式为__________。
(2)求解混合物中发生反应物质的质量(x)的比例式为__________。
(3)石灰石样品中碳酸钙的质量分数为__________。
(4)所得溶液中溶质质量分数为__________。
(5)若用36.5%的浓盐酸配制100g上述实验所用的稀盐酸,所需浓盐酸的质量为__________。
(6)若工厂需要生产1120t含杂质20%的生石灰,理论上需要上述石灰石的质量为__________。

(1)实验中发生反应的化学方程式为__________。
(2)求解混合物中发生反应物质的质量(x)的比例式为__________。
(3)石灰石样品中碳酸钙的质量分数为__________。
(4)所得溶液中溶质质量分数为__________。
(5)若用36.5%的浓盐酸配制100g上述实验所用的稀盐酸,所需浓盐酸的质量为__________。
(6)若工厂需要生产1120t含杂质20%的生石灰,理论上需要上述石灰石的质量为__________。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】为测定氧化铜和铜的混合物的组成情况,风华实验小组进行了如下实验:

其中反应①、反应②均为恰好完全反应,请回答下列问题:
(1)反应②中发生的化学方程式为______________。
(2)由氧化铜的质量求解生成的水的质量(x)的比例式为_________________。
(3)混合物中氧元素和铜元素的质量最简整数比为__________________。
(4)在滴加氢氧化钠溶液的过程中,烧杯中各溶质质量的变化情况为_______________。
(5)a的数值为______________。

其中反应①、反应②均为恰好完全反应,请回答下列问题:
(1)反应②中发生的化学方程式为______________。
(2)由氧化铜的质量求解生成的水的质量(x)的比例式为_________________。
(3)混合物中氧元素和铜元素的质量最简整数比为__________________。
(4)在滴加氢氧化钠溶液的过程中,烧杯中各溶质质量的变化情况为_______________。
(5)a的数值为______________。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】现有碳酸钠和氯化钠的固体混合物14.9g,加入95.1水,固体完全溶解,向该溶液中加入氯化钙溶液,所得溶液质量与加入氯化钙溶液的质量的关系如图所示。请计算:

(1)恰好完全反应时,生成沉淀质量是______ 。
(2)恰好完全反应时,所得溶液中溶质的质量分数是多少?

(1)恰好完全反应时,生成沉淀质量是
(2)恰好完全反应时,所得溶液中溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】侯氏制碱法生产的碳酸钠中常含有少量的氯化钠。某学习小组对其组成展开探究。取碳酸钠和氯化钠的混合物样品24g,加入100g水使其完全溶解,再加入96g过量的氯化钙溶液,反应过程中生成沉淀的质量与氯化钙溶液的质量关系如图所示:______ g。
(2)计算样品中Na2CO3的质量分数?(写出计算过程,结果保留一位小数)。
(3)取混合物样品12g,加入足量的稀盐酸,将生成的二氧化碳通入盛有8g炽热碳粉的密闭容器中充分反应,在下图中画出二氧化碳的质量与容器中固体质量变化的关系图。

(2)计算样品中Na2CO3的质量分数?(写出计算过程,结果保留一位小数)。
(3)取混合物样品12g,加入足量的稀盐酸,将生成的二氧化碳通入盛有8g炽热碳粉的密闭容器中充分反应,在下图中画出二氧化碳的质量与容器中固体质量变化的关系图。

您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】取氯化钙和氯化钠的混合物10g,加入40g水使其完全溶解,再加入50g碳酸钠溶液恰好完全反应,过滤,得95g滤液(不考虑实验过程中质量损失),计算:
(1)所加碳酸钠溶液的溶质质量分数;
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%).
(1)所加碳酸钠溶液的溶质质量分数;
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%).
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】取氯化钙和盐酸的混合溶液51.88g,逐滴滴加10.6%的碳酸钠溶液。所加入碳酸钠溶液的质量和混合溶液pH变化关系如图所示,回答下列问题:
(1)CD段溶液pH>7的原因是___________ 。
(2)计算充分反应至C点时所得溶液中溶质的质量分数(写出计算过程,计算结果精确至0.1%)。

(1)CD段溶液pH>7的原因是
(2)计算充分反应至C点时所得溶液中溶质的质量分数(写出计算过程,计算结果精确至0.1%)。

您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】江津区水泥厂要采购一批石灰石,将以它为原料生产水泥。为了检验石灰石的纯度,该厂技术员取了 10 g 石灰石样品并把 60 g 稀盐酸平均分成四次加入,充分反应后,获得有关数据如下:(杂质不反应也不溶于水)
请计算:
(1)表格中Y 的数值为_____。
(2)该石灰石样品中碳酸钙的纯度为_____如果要用质量分数为 36.5%的浓盐酸来配制所需的 60 g 稀盐酸,求所需的浓盐酸的质量_____。
稀盐酸的用量 | 剩余固体的质量 |
第一次加入15g | 7.5g |
第二次加入15g | Y |
第三次加入15g | 2.5g |
第四次加入15g | 1.5g |
(1)表格中Y 的数值为_____。
(2)该石灰石样品中碳酸钙的纯度为_____如果要用质量分数为 36.5%的浓盐酸来配制所需的 60 g 稀盐酸,求所需的浓盐酸的质量_____。
您最近一年使用:0次



