以镁矿石(主要成分 MgCO3、SiO2)为原料生产 MgO 的工艺流程如下:
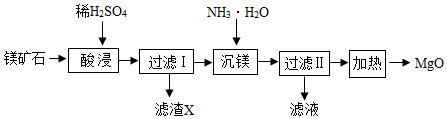
注SiO2难溶于水和常见的酸;“沉镁”过程中有 Mg(OH)2生成。
(1)滤渣 X 的主要成分为_____ (填化学式)。
(2)实验室中用图 1 所示装置进行过滤。
①该装置中玻璃棒的作用是_____ 。
②若过滤时滤液出现浑浊,可能的原因是_____ 。
(3)沉镁时 MgSO4与 NH3·H2O 发生反应,写出该反应的化学方程式_____ 。
(4)已知在不同温度下,充分加热等质量的 Mg(OH)2,加热温度与固体残留率的关系如图2。加热时温度至少要达到 350℃,原因是_____ 。


注SiO2难溶于水和常见的酸;“沉镁”过程中有 Mg(OH)2生成。
(1)滤渣 X 的主要成分为
(2)实验室中用图 1 所示装置进行过滤。
①该装置中玻璃棒的作用是
②若过滤时滤液出现浑浊,可能的原因是
(3)沉镁时 MgSO4与 NH3·H2O 发生反应,写出该反应的化学方程式
(4)已知在不同温度下,充分加热等质量的 Mg(OH)2,加热温度与固体残留率的关系如图2。加热时温度至少要达到 350℃,原因是

更新时间:2020-09-28 22:55:54
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某兴严小组在实验室用废渣(主要成分为CaCO3,还含有C、CuO、MgO等少量杂质)来制取CaCl2,过程如图所示:

(1)滤渣I的主要成分为_______ (填化学式)。
(2)写出“除铜、镁”时发生反应的化学方程式_______ 。(写一个)
(3)为不产生副产品,可用_______ (填化学式)溶液代替NaOH溶液开展实验。

(1)滤渣I的主要成分为
(2)写出“除铜、镁”时发生反应的化学方程式
(3)为不产生副产品,可用
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】疫情期间,常用84消毒液(主要成分为NaClO)进行环境消毒。利用粗盐(含CaCl2、MgCl2、Na2SO4、泥沙等杂质)制“84”消毒液的流程如下:

(1)溶液E中要加入适量稀盐酸,其目的是除去过量的除杂试剂,写出发生反应的一个化学方程式为______ 。
(2)次氯酸钠溶液能与空气中的CO2反应而变质,因此“84”消毒液应______ 储存。

(1)溶液E中要加入适量稀盐酸,其目的是除去过量的除杂试剂,写出发生反应的一个化学方程式为
(2)次氯酸钠溶液能与空气中的CO2反应而变质,因此“84”消毒液应
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】石灰石在生产生活中有广泛的用途。
(1)煅烧石灰石可制得活性CaO,反应的化学方程式为___________________ 。
(2)为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等分,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如下图所示。可知:CaO与水反应会_________ 热量(填“放出”或“吸收”);上述温度中,______ ℃煅烧所得CaO活性最高。要得出正确结论,煅烧时还需控制的条件是________ 。
(3)以电石渣(主要成分为Ca(OH)2,还含有少量MgO等杂质)为原料制备高纯CaCO3的流程如下:

①如图为NH4Cl浓度对钙、镁浸出率的影响:
(浸出率= ×100%)
×100%)

可知:较适宜的NH4Cl溶液的质量分数为________ ;浸取时主要反应的化学方程式为________________
②流程中方框内部分若改用_______________ 溶液(填化学式),可一步得到与原流程完全相同的生成物。
③流程中方框内部分若改用Na2CO3溶液,也能得到高纯CaCO3,试从生成物的角度分析原流程的优点:
a.NH3可循环利用; b.________________ 。
(1)煅烧石灰石可制得活性CaO,反应的化学方程式为
(2)为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等分,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如下图所示。可知:CaO与水反应会
(3)以电石渣(主要成分为Ca(OH)2,还含有少量MgO等杂质)为原料制备高纯CaCO3的流程如下:

①如图为NH4Cl浓度对钙、镁浸出率的影响:
(浸出率=
 ×100%)
×100%)
可知:较适宜的NH4Cl溶液的质量分数为
②流程中方框内部分若改用
③流程中方框内部分若改用Na2CO3溶液,也能得到高纯CaCO3,试从生成物的角度分析原流程的优点:
a.NH3可循环利用; b.
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行。
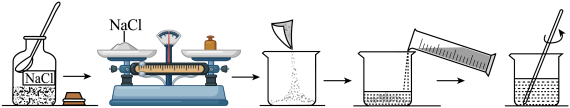
请回答下列问题:
(1)计算配制100g溶质质量分数为5%的氯化钠溶液所需:
氯化钠___________ g,水___________ g。
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应________ 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节平衡螺母
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是____________ 。

请回答下列问题:
(1)计算配制100g溶质质量分数为5%的氯化钠溶液所需:
氯化钠
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节平衡螺母
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是
您最近一年使用:0次
【推荐2】根据所学知识回答下列几个小题:

(1)图1是水的电解实验图,图中与电池正极相连的试管内收集到的气体应该为___________ (填化学式)。
(2)用洗涤剂去除油污,是利用洗涤剂的___________ 作用
(3)实验室硬水软化的方法是:___________ 。
(4)图2为水的净化过程中的过滤操作。其中玻璃棒的作用是___________ 。

(1)图1是水的电解实验图,图中与电池正极相连的试管内收集到的气体应该为
(2)用洗涤剂去除油污,是利用洗涤剂的
(3)实验室硬水软化的方法是:
(4)图2为水的净化过程中的过滤操作。其中玻璃棒的作用是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】粗盐中常含有泥沙、氯化钙和硫酸镁等杂质。为制得纯净的氯化钠固体,某化学兴趣小组进行了如下操作。

(1)若玻璃棒在上述某操作中的作用是搅拌,防止因局部温度过高,造成液滴飞溅,写出该操作的名称。
(2)写出一个在以上操作中有碱生成的化学反应方程式。
(3)为验证溶液B中所含杂质,该小组取少量溶液B,先滴加酚酞溶液,而后加入足量的CaCl2溶液,充分反应后过滤;观察到产生白色沉淀,过滤后溶液仍呈红色。
得出结论:溶液B中含有氢氧化钠、碳酸钠杂质。请说明该结论合理的原因。

(1)若玻璃棒在上述某操作中的作用是搅拌,防止因局部温度过高,造成液滴飞溅,写出该操作的名称。
(2)写出一个在以上操作中有碱生成的化学反应方程式。
(3)为验证溶液B中所含杂质,该小组取少量溶液B,先滴加酚酞溶液,而后加入足量的CaCl2溶液,充分反应后过滤;观察到产生白色沉淀,过滤后溶液仍呈红色。
得出结论:溶液B中含有氢氧化钠、碳酸钠杂质。请说明该结论合理的原因。
您最近一年使用:0次



