做完“铁在氧气里燃烧”实验后,某兴趣小组有一些疑惑不解的问题,于是他们进行了以下探究活动,请你一同参与。
【问题】细铁丝在氧气中燃烧为什么会“火星四射”?
【查阅资料1】①日常生活中的钢铁制品都含有少量碳杂质。
②含碳细铁丝燃烧时,其中的炭粒生成的CO2气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”的现象。
【设计实验】为了探究细铁丝在纯氧中燃烧产生“火星四射”现象的原因,该小组同学设计的实验方案是:取长短粗细相同的含碳细铁丝和不含碳的细铁丝,分别在足量的氧气中燃烧,观察现象。你认为他们的方案_________ (填“合理”或“不合理”)。
【实验探究】小明做细铁丝在氧气中的燃烧实验时,他把细铁丝绕成螺旋状,一端系在一根铁丝上,另一端系上一根火柴。点燃火柴后迅速把铁丝连同火柴一起插入集气瓶下部(没有接触到水,如图所示),但不见铁丝燃烧,反复实验均未成功。
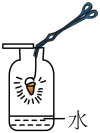
该同学认为可能导致失败的原因主要有三种:
A铁丝表面有锈迹,影响了反应的进行;
B点燃火柴后立即将它伸入瓶内,火柴燃烧消耗了氧气,不利于铁丝的燃烧;
C火柴燃烧时有大量的热量放出,将铁丝和火柴迅速伸至集气瓶下部,因热胀冷缩之故。瓶内氧气会膨胀逸出,使铁丝无法燃烧。
针对假设A应作出的实验改进为(1)____________ ;
针对假设B应作出的实验改进为(2)___________ ;
针对假设C应作出的实验改进为(3)___________ ;
【查阅资料2】①黑色的Fe3O4和红色的Fe2O3的分解温度、铁的熔点见表:
②Fe2O3高温时分解成Fe3O4
③FeO不稳定,容易被空气中的氧气氧化成Fe2O3
【理论探讨】根据铁丝燃烧的实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在_________ 之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产物是Fe3O4。
【拓展延伸】有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色_________ ,就说明包装盒破损进气,这样售货员就能及时发现并处理。
【问题】细铁丝在氧气中燃烧为什么会“火星四射”?
【查阅资料1】①日常生活中的钢铁制品都含有少量碳杂质。
②含碳细铁丝燃烧时,其中的炭粒生成的CO2气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”的现象。
【设计实验】为了探究细铁丝在纯氧中燃烧产生“火星四射”现象的原因,该小组同学设计的实验方案是:取长短粗细相同的含碳细铁丝和不含碳的细铁丝,分别在足量的氧气中燃烧,观察现象。你认为他们的方案
【实验探究】小明做细铁丝在氧气中的燃烧实验时,他把细铁丝绕成螺旋状,一端系在一根铁丝上,另一端系上一根火柴。点燃火柴后迅速把铁丝连同火柴一起插入集气瓶下部(没有接触到水,如图所示),但不见铁丝燃烧,反复实验均未成功。

该同学认为可能导致失败的原因主要有三种:
A铁丝表面有锈迹,影响了反应的进行;
B点燃火柴后立即将它伸入瓶内,火柴燃烧消耗了氧气,不利于铁丝的燃烧;
C火柴燃烧时有大量的热量放出,将铁丝和火柴迅速伸至集气瓶下部,因热胀冷缩之故。瓶内氧气会膨胀逸出,使铁丝无法燃烧。
针对假设A应作出的实验改进为(1)
针对假设B应作出的实验改进为(2)
针对假设C应作出的实验改进为(3)
【查阅资料2】①黑色的Fe3O4和红色的Fe2O3的分解温度、铁的熔点见表:
②Fe2O3高温时分解成Fe3O4
③FeO不稳定,容易被空气中的氧气氧化成Fe2O3
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度℃ | 1538 | 1400 | 一 |
| 熔点/℃ | 一 | 一 | 1535 |
【拓展延伸】有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色
更新时间:2020-10-28 18:33:10
|
【知识点】 铁在氧气中燃烧及其实验解读
相似题推荐
科学探究题
|
较易
(0.85)
解题方法
【推荐1】实验是学习化学的一条重要途径,同学们想对铁丝在氧气中燃烧的现象进行探究。

【提出问题】铁丝在氧气中为什么会产生火星四射现象?
【查阅资料】
a.纯铁丝燃烧无火星四射现象;
b.含碳细铁丝燃烧时,其中的碳粒生成的二氧化碳气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”现象。
【设计实验】
取纯铁丝和含碳量分别为0.1%、0.32%、0.52%、0.69%的铁丝(直径均为0.20mm)分别在氧气中进行实验。
(1)铁丝的末端系一根火柴的作用______ ;集气瓶底部放少量水的目的 ______ ;
(2)铁丝为什么要绕成螺旋状______ ;
(3)铁丝在氧气中燃烧的文字表达式______ ;
(4)下表是实验中所记录的实验现象。
【得出结论】
铁丝燃烧喷射火星情况与其含碳量的关系为__________ 。

【提出问题】铁丝在氧气中为什么会产生火星四射现象?
【查阅资料】
a.纯铁丝燃烧无火星四射现象;
b.含碳细铁丝燃烧时,其中的碳粒生成的二氧化碳气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”现象。
【设计实验】
取纯铁丝和含碳量分别为0.1%、0.32%、0.52%、0.69%的铁丝(直径均为0.20mm)分别在氧气中进行实验。
(1)铁丝的末端系一根火柴的作用
(2)铁丝为什么要绕成螺旋状
(3)铁丝在氧气中燃烧的文字表达式
(4)下表是实验中所记录的实验现象。
| 含碳量 | 纯铁丝 | 0.1% | 0.32% | 0.52% | 0.69% |
| 实验现象 | 无火星四射现象,熔断 | 有短暂火星四射现象 | 火星四射现象明显 | 燃烧比0.32%的剧烈,火星四射更明显 | 燃烧比0.52%的剧烈,火星四射更明显 |
铁丝燃烧喷射火星情况与其含碳量的关系为
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐2】某化学兴趣小组同学依据教材实验对化学反应前后物质的总质量变化进行了探究。
[实验装置设计]甲、乙、丙小组同学分别设计如图装置:

[步骤与探究](1)甲组同学取一根打磨干净的细铁丝和一个石棉网,将它们一起放在托盘天平上用砝码平衡,取下铁丝,将铁丝放在充满氧气的集气瓶中点燃,燃烧结束并冷却至室温后将所得的物质与石棉网起再放回托盘天平上称量,天平指针向左偏转。铁丝燃烧的现象是________________ 。
(2)乙组同学取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,可观察到天平指针_______________ (填“ 向左偏转”、“向右偏转”或“指向中间”)。
(3)丙组同学将过氧化氢溶液挤入锥形瓶中发生反应。通过观察实验过程中天平指针的现象,得出的结论是参加化学反应的各物质的质量总和________________ (填“ 大于”、“等于”或“小于”)反应后生成的各物质的质量总和。写出装置中发生反应的化学方程式________________ 。
[实验分析](4)三组同学经过讨论分析,认为丙组的实验结论是正确的,请从原子的角度解释________ 。
[反思与交流](5)通过甲、乙、丙小组实验的探究,你得到的启示是利用有气体生成或参加的反应进行探究质量守恒定律的实验时,反应应在________________ 容器中进行。
[实验装置设计]甲、乙、丙小组同学分别设计如图装置:

[步骤与探究](1)甲组同学取一根打磨干净的细铁丝和一个石棉网,将它们一起放在托盘天平上用砝码平衡,取下铁丝,将铁丝放在充满氧气的集气瓶中点燃,燃烧结束并冷却至室温后将所得的物质与石棉网起再放回托盘天平上称量,天平指针向左偏转。铁丝燃烧的现象是
(2)乙组同学取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,可观察到天平指针
(3)丙组同学将过氧化氢溶液挤入锥形瓶中发生反应。通过观察实验过程中天平指针的现象,得出的结论是参加化学反应的各物质的质量总和
[实验分析](4)三组同学经过讨论分析,认为丙组的实验结论是正确的,请从原子的角度解释
[反思与交流](5)通过甲、乙、丙小组实验的探究,你得到的启示是利用有气体生成或参加的反应进行探究质量守恒定律的实验时,反应应在
您最近一年使用:0次
科学探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学兴趣小组进行“铁丝在氧气中燃烧”的实验,并进行了一些探究活动。
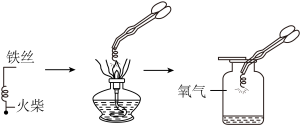
【实验回顾】铁丝在氧气中燃烧实验的示意图如图,实验前要将铁丝打磨,原因是______ ;图中螺旋状铁丝的末端系一根火柴的作用是______ ;铁丝应由上向下缓慢伸进盛有氧气的集气瓶中,原因是______ ;集气瓶中先放一些水的作用是______ 。铁丝燃烧的符号表达式为______ 。
【探究一】铁丝燃烧是否需要纯氧?
【设计实验1】取直径为0.38mm的铁丝,分别在体积分数为90%、70%、60%、55%的氧气中实验。实验现象如表所示:
【结论】就0.38mm铁丝而言,铁丝燃烧对氧气体积分数的要求是______ (“>”“=”或“<”)55%,且氧气浓度越大,燃烧现象越______ (填“剧烈”或“不剧烈”)。
【讨论】实验中所用集气瓶的容积为125mL,铁丝燃烧实验时集气瓶中需留25mL水,如果需收集100mL体积分数为80%的氧气,其操作方法是先在集气瓶中装______ mL水,然后用排水法收集,直到剩下25mL水(空气中氧气的体积分数计为20%)。
【探究二】兴趣小组同学又产生新的猜想,铁丝燃烧,是否和铁本身的颗粒大小有关?
【设计实验2】他们用还原铁粉、纳米铁粉在空气中进行实验,实验操作及现象如表:
由此实验你能得出的结论是:______ 。
【探究三】铁丝燃烧为什么会火星四射?
【资料】生活中常见的铁都不是纯净的铁,都含有一定量的碳
【设计实验3】小明将直径都为0.38mm的纯镁条和不同含碳量的铁丝放入氧气中燃烧,实验现象记录如表,请你分析完成下表:
【结论】通过以上实验,说明铁丝燃烧产生火星四射现象和含碳量______ (填“有关”或“无关”)。

【实验回顾】铁丝在氧气中燃烧实验的示意图如图,实验前要将铁丝打磨,原因是
【探究一】铁丝燃烧是否需要纯氧?
【设计实验1】取直径为0.38mm的铁丝,分别在体积分数为90%、70%、60%、55%的氧气中实验。实验现象如表所示:
| O2体积分数 | 90% | 70% | 60% | 55% |
| 实验现象 | 燃烧剧烈、燃烧时间长,效果好 | 燃烧比90%弱,燃烧时间短,实验成功 | 燃烧比70%弱,燃烧时间更短,实验成功 | 难以燃烧,只是发红 |
【讨论】实验中所用集气瓶的容积为125mL,铁丝燃烧实验时集气瓶中需留25mL水,如果需收集100mL体积分数为80%的氧气,其操作方法是先在集气瓶中装
【探究二】兴趣小组同学又产生新的猜想,铁丝燃烧,是否和铁本身的颗粒大小有关?
【设计实验2】他们用还原铁粉、纳米铁粉在空气中进行实验,实验操作及现象如表:
| 还原铁粉 | 纳米铁粉 | |
| 粒径大小(nm) | 1000 | 20-200 |
| 实验操作和现象 | 直接洒在燃着的酒精灯外焰上,有火星 | 直接从密封容器中洒落在石棉网上,有火星 |
【探究三】铁丝燃烧为什么会火星四射?
【资料】生活中常见的铁都不是纯净的铁,都含有一定量的碳
【设计实验3】小明将直径都为0.38mm的纯镁条和不同含碳量的铁丝放入氧气中燃烧,实验现象记录如表,请你分析完成下表:
| 物质 | 纯镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时的现象 | 剧烈燃烧,无火星 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 |
您最近一年使用:0次



