A—G是初中化学常见的物质,它们之间的关系如图所示,其中①是中和反应,乙是一种红色粉末,“→”表示物质间的转化关系,“ ”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出
”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出 )
)
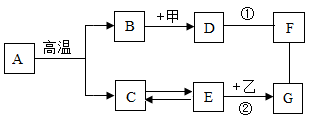
回答下列问题:
(1)A的化学式是_________ ;
(2)B D的基本反应类型:
D的基本反应类型:__________ ;
(3)写出反应②的化学方程式:__________ .
 ”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出
”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出 )
)
回答下列问题:
(1)A的化学式是
(2)B
 D的基本反应类型:
D的基本反应类型:(3)写出反应②的化学方程式:
更新时间:2020-11-25 21:48:17
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】物质A~F都是初中化学中的常见物质,它们有如图所示的转化关系。回答下列问题D为液态氧化物,E为红色固体单质,C为气态氧化物,F能使澄清石灰水变浑浊。

(1)则A、B、E的化学式为:A______ 、B_________ 、E_________
(2)写出下列反应化学方程式:A+B:_______ ;B+C:_______ 。

(1)则A、B、E的化学式为:A
(2)写出下列反应化学方程式:A+B:
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】下列是初中化学常见物质间的转化关系,这些物质由碳、氢、氧元素组成的,其中,甲、乙为单质,A、B、C、D为化合物,且A与B的组成元素相同,C与D的组成元素也相同,其余反应条件、部分反应物已略去,试推断:

(1)转化①的化学方程式为____________ ;
(2)转化①转化②均属于______________ (填基本反应类型);
(3)选择图中物质实现转化③,则物质C的化学式为____________ 。

(1)转化①的化学方程式为
(2)转化①转化②均属于
(3)选择图中物质实现转化③,则物质C的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】多角度认识物质能帮助我们更全面地了解物质世界。以金属为例回答下列问题:
(1)认识金属元素的存在
①在自然界中,大多数金属以化合物存在,而金、铂等极少数金属因为化学性质___________ (填“活泼”或“不活泼”)却能以单质存在。
②常见铁矿石有:黄铁矿(主要成分FeS2)、磁铁矿(主要成分Fe3O4)等。这两种铁矿石的主要成分含铁元素质量分数较大的是___________ 。
(2)认识金属的性质
用粗木棍在涂有蜡的锌板上写“茂”、名”两个字,露出下面的锌板。向“茂”字上滴加CuSO4溶液,向“名”字上滴加稀盐酸。
茂名
①“茂”字上的现象是___________ 。
②“名”字上的现象是___________ ,用化学方程式解释:___________ 。
(3)认识金属的制备
工业上,金属铁可由CO和Fe2O3在高温下发生反应制得。反应中CO的作用是___________ ,反应中化合价降低的元素是___________ 。
(1)认识金属元素的存在
①在自然界中,大多数金属以化合物存在,而金、铂等极少数金属因为化学性质
②常见铁矿石有:黄铁矿(主要成分FeS2)、磁铁矿(主要成分Fe3O4)等。这两种铁矿石的主要成分含铁元素质量分数较大的是
(2)认识金属的性质
用粗木棍在涂有蜡的锌板上写“茂”、名”两个字,露出下面的锌板。向“茂”字上滴加CuSO4溶液,向“名”字上滴加稀盐酸。
茂名
①“茂”字上的现象是
②“名”字上的现象是
(3)认识金属的制备
工业上,金属铁可由CO和Fe2O3在高温下发生反应制得。反应中CO的作用是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】盐酸和稀硫酸的特性(个性)
(1)稀硫酸的特性(含有 )
)
含有 的溶液能与
的溶液能与 等(含
等(含 的溶液)反应生成不溶于稀硝酸的
的溶液)反应生成不溶于稀硝酸的______ ;通常用此反应来鉴别某物质中含有 。
。
(2)盐酸的特性(含有 )
)
含有 的溶液能与
的溶液能与 溶液反应生成不溶于稀硝酸的
溶液反应生成不溶于稀硝酸的______ ;通常用此反应来鉴别某物质中含有 。
。
(3)硝酸的特性
无色、有刺激性的液体,易挥发,见光易分解,通常密封保存在棕色瓶中、硝酸具有氧化性,所以与金属反应不生成______ 而生成水。
(1)稀硫酸的特性(含有
 )
)含有
 的溶液能与
的溶液能与 等(含
等(含 的溶液)反应生成不溶于稀硝酸的
的溶液)反应生成不溶于稀硝酸的 。
。(2)盐酸的特性(含有
 )
)含有
 的溶液能与
的溶液能与 溶液反应生成不溶于稀硝酸的
溶液反应生成不溶于稀硝酸的 。
。(3)硝酸的特性
无色、有刺激性的液体,易挥发,见光易分解,通常密封保存在棕色瓶中、硝酸具有氧化性,所以与金属反应不生成
您最近一年使用:0次
【推荐3】阅读下面的科普短文,回答相关问题。
我们的胃液呈酸性,是因为胃腺壁细胞能分泌出盐酸。胃酸在人体的消化吸收中发挥着重要作用,如为胃蛋白酶提供适宜的酸性环境,分解食物中的结缔组织和肌纤维使其易于被消化吸收。深受人们喜欢的早餐食品燕麦中常添加颗粒极小的铁粉,它既可以作为双吸剂 (能与氧气和水蒸气反应,起到干燥和减缓食品变质的作用),还可 以作为人体补铁剂。要把铁粉变为人体需要的、能吸收的营养元素,就离不开胃酸的帮助。
健康人胃液的pH在0.9~1.5,胃液的pH不仅影响人的消化吸收功能,还对伴随食物进入胃内的各类病菌的繁殖有影响。某医院对99位胃溃疡和十二指肠溃疡等患者胃液的pH及胃液中的病菌进行了检测,结果如下表:
胃酸过多会对胃黏膜具有侵蚀作用,并使人感觉反酸或烧心。治疗胃酸过多的药主要有两大类:一是抑酸药,能抑制胃酸分泌,但本身不能和胃酸反应;二是抗酸药,能直接与胃酸反应,常见的抗酸药有碳酸氢钠、氢氧化铝、氧化镁、氢氧化镁和碳酸钙等。胃溃疡患者若服用不合适的抗酸药,会因胃内气体压力增大而引起胃穿孔。患者如长期使用抗酸药,很可能刺激胃酸分泌过多。因此,应遵医嘱合理使用抗酸类和抑酸类药物。 依据文章内容,回答下列问题。
(1)燕麦中的铁粉遇胃酸发生反应的化学方程式为_______ 。
(2)常见的抗酸药中,胃溃疡患者不宜服用的抗酸药是_______ 。
(3)关于文中提到的几种抗酸药,所属的物质类别有_______ 种。
(4)根据文章,下列说法正确的是 (填字母序号)。
我们的胃液呈酸性,是因为胃腺壁细胞能分泌出盐酸。胃酸在人体的消化吸收中发挥着重要作用,如为胃蛋白酶提供适宜的酸性环境,分解食物中的结缔组织和肌纤维使其易于被消化吸收。深受人们喜欢的早餐食品燕麦中常添加颗粒极小的铁粉,它既可以作为双吸剂 (能与氧气和水蒸气反应,起到干燥和减缓食品变质的作用),还可 以作为人体补铁剂。要把铁粉变为人体需要的、能吸收的营养元素,就离不开胃酸的帮助。
健康人胃液的pH在0.9~1.5,胃液的pH不仅影响人的消化吸收功能,还对伴随食物进入胃内的各类病菌的繁殖有影响。某医院对99位胃溃疡和十二指肠溃疡等患者胃液的pH及胃液中的病菌进行了检测,结果如下表:
| 分组 | 胃液的pH | 受检患者人数 | 胃液中检出病菌的人数及比例 |
| A | ≤2.0 | 7 | 0 |
| B | 2.0~4.0 | 13 | 3(23.1%) |
| C | 4.0~6.0 | 26 | 17(65.4%) |
| D | >6.0 | 53 | 45(84.9%) |
(1)燕麦中的铁粉遇胃酸发生反应的化学方程式为
(2)常见的抗酸药中,胃溃疡患者不宜服用的抗酸药是
(3)关于文中提到的几种抗酸药,所属的物质类别有
(4)根据文章,下列说法正确的是 (填字母序号)。
| A.适量使用碳酸钙可治疗胃酸过多,同时还可为人体补充微量元素钙 |
| B.在使用抗酸药时不是用量越多越好 |
| C.胃酸能帮助人体消化吸收食物,所以胃液pH越小越利于人体健康 |
| D.胃液pH越大越有利于病菌生存 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】请用化学用语填空。
(1)2个镁离子______ ;
(2)标出KIO3中碘元素的化合价______ ;
(3)医用酒精中的溶质______ ;
(4)白磷的二硫化碳溶液中的溶剂______ ;
(5)食醋中含有的酸______ ;
(6)不含金属元素的碱______ ;
(7)生石灰作干燥剂的原理(用化学方程式表示)______ 。
(1)2个镁离子
(2)标出KIO3中碘元素的化合价
(3)医用酒精中的溶质
(4)白磷的二硫化碳溶液中的溶剂
(5)食醋中含有的酸
(6)不含金属元素的碱
(7)生石灰作干燥剂的原理(用化学方程式表示)
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】A~H是初中化学中常见的物质,下图为这些物质的相互转化关系图,其中E为黑色固体,H为蓝色沉淀,部分生成物与反应条件已省略。请回答下列问题:

(1)B和水反应属于___________ (填“放热”或“吸热”)反应;F物质的俗称是___________ (写一种)。
(2)写出C物质的一种用途:___________ 。
(3)H的化学式为___________ ;在相互转化过程中没有涉及的基本反应类型是___________ ;
(4)E→G反应的化学方程式为___________ 。

(1)B和水反应属于
(2)写出C物质的一种用途:
(3)H的化学式为
(4)E→G反应的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐3】A-G是初中化学常见的物质,由氢、碳、氧、钙、铁中的一种或几种组成。已知A是一种红色固体,C是常见的金属,D有助燃性,A、B、E、F都是氧化物,G是含钙的化合物,物质之间的相互反应及转化关系如图所示,图中“→”表示转化关系,“ — ”表示能相互反应。 (部分反应物、生成物或反应条件已略去)。

请回答下列问题
(1)分别写出物质E、G的化学式:_______ ________ .
(2)写出C、D发生剧烈氧化时的现象__________________
(3)写出A-B发生反应的化学方程式_________________________________
(4) 物质F可以是__________ ,也可以是 __________ .

请回答下列问题
(1)分别写出物质E、G的化学式:
(2)写出C、D发生剧烈氧化时的现象
(3)写出A-B发生反应的化学方程式
(4) 物质F可以是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】已知某种干电池的内部黑色糊状填充物含炭黑、二氧化锰、氯化铵和氯化锌。下列是回收利用干电池得到二氧化锰和氯化铵固体的流程:

有关数据见表:
(1)操作I中用到的玻璃仪器有_____ 、玻璃棒和漏斗;
(2)固体M的成分为_____ ,操作Ⅲ的简便方法为_____ 。
(3)操作Ⅱ的过程包括冷却结晶、过滤、洗涤、干燥。溶液B的溶质为_____ ;洗涤时最好选用下列物质中的_____ 作为洗涤液。
A 冰水 B 氯化铵饱和溶液 C 氯化锌饱和溶液 D 氯化钠饱和溶液
(4)施肥时不能将熟石灰与氯化铵混合施用的原因是_____ (用化学方程式回答)。

有关数据见表:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 | |
(1)操作I中用到的玻璃仪器有
(2)固体M的成分为
(3)操作Ⅱ的过程包括冷却结晶、过滤、洗涤、干燥。溶液B的溶质为
A 冰水 B 氯化铵饱和溶液 C 氯化锌饱和溶液 D 氯化钠饱和溶液
(4)施肥时不能将熟石灰与氯化铵混合施用的原因是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
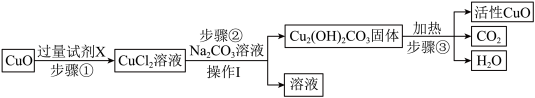
【推荐2】活性氧化铜可用于印刷电路板制造,由普通氧化铜制备活性氧化铜的工艺流程如下:_______ 。
(2)步骤①中与CuO反应的试剂X是_______ (填化学式)。
(3)步骤②加入Na2CO3溶液时有气泡产生,请用化学方程式解释_______ 。
(4)步骤②得到的溶液中一定含有的溶质有_______ 。
(5)写出步骤③发生反应的化学方程式_______ 。
(2)步骤①中与CuO反应的试剂X是
(3)步骤②加入Na2CO3溶液时有气泡产生,请用化学方程式解释
(4)步骤②得到的溶液中一定含有的溶质有
(5)写出步骤③发生反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】A~E均为初中化学常见物质,其中B是一种常用溶剂,D、E的水溶液均能使无色酚酞溶液变红,且E能用于制造玻璃。它们之间的转化关系如图所示。(“一”表示物质之间可以发生反应,“→”表示物质之间可以一步实现转化)

请回答下列问题:
(1)C的化学式是_____________ 。
(2)E→D的化学方程式是___________ ,该反应能够发生的理由是___________ 。
(3)A→B的化学方程式是___________________________ 。

请回答下列问题:
(1)C的化学式是
(2)E→D的化学方程式是
(3)A→B的化学方程式是
您最近一年使用:0次




