为除去食盐溶液中的SO42-、Ca2+、Mg2+,进行下列操作:①过滤;②加适量稀盐酸;③加过量NaOH溶液;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。合理的操作顺序是:
| A.⑤③④①② | B.⑤④③②① | C.③④⑤①② | D.④③⑤①② |
更新时间:2020-05-06 21:17:09
|
相似题推荐
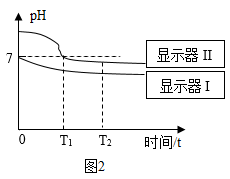
【推荐1】用图 1 装置进行 CO2的制取及性质实验。实验开始,向锥形瓶中加入一定量的稀盐酸,图 2 表示实验过程中装置 H 和 I 中的溶液 pH 变化曲线。下列说法不正确的是



| A.图 1 中能说明 CO2能与 NaOH 溶液反应的现象 H 中无现象,I 中有白色沉淀 |
B.图 2 中,0~T1时,显示器Ⅱ测得 pH 不断变小的原因之一是  |
| C.反应结束后,装置 H 的溶液中有 5 种微粒 |
| D.根据显示器Ⅰ的 pH 变化曲线可知氯化钡溶液呈中性 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐2】能正确反映对应变化关系的图像是
A.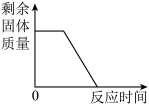 加热一定质量的高锰酸钾固体 加热一定质量的高锰酸钾固体 |
B.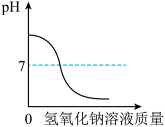 向一定量的稀硫酸中滴加氢氧化钠溶液至过量 向一定量的稀硫酸中滴加氢氧化钠溶液至过量 |
C. 一定温度下,向不饱和硝酸钠溶液中不断加入硝酸钠固体,充分搅拌 一定温度下,向不饱和硝酸钠溶液中不断加入硝酸钠固体,充分搅拌 |
D. 分别向同质量、同质量分数的稀盐酸中不断加入碳酸镁和氧化镁固体 分别向同质量、同质量分数的稀盐酸中不断加入碳酸镁和氧化镁固体 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
名校
解题方法
【推荐1】由于粗盐中含有少量MgC12、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。下列说法正确的是
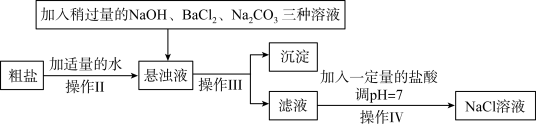
| A.过量的Na2CO3溶液的作用只是除去粗盐中的CaC12 |
| B.通过操作Ⅲ所得滤液中的溶质有NaOH、Na2CO3 |
| C.若操作IV中加入过量的盐酸,蒸发氯化钠溶液也可得到的纯净的氯化钠 |
| D.操作III和IV颠倒顺序,对最后的结果没有任何影响 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐2】粗盐中通常含泥沙、CaCl2、MgCl2及硫酸盐等杂质,粗盐经过处理可以得到纯净的氯化钠,流程如下图所示,下列有关说法正确的是
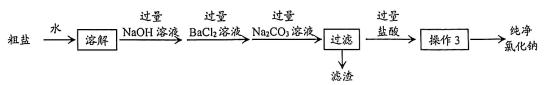

| A.“操作3”为降温结晶 |
| B.加入过量盐酸的目的只是为了除去过量的碳酸钠 |
| C.若8 g粗盐经过上述处理后得到纯净NaCl质量可能大于8 g |
D.过滤后滤液中的主要离子有:Na+、Ca2 +、Cl-、 、OH- 、OH- |
您最近一年使用:0次
选择题-选择题组
|
较难
(0.4)
解题方法
【推荐3】阅读下列资料,完成下面小题。
海洋是地球上最大的储水库,其储水量约占全球总储水量的 96.5%。海水中蕴藏着丰富的化学资源,人类正运用各种方法,对海水进行科学的开发和综合利用。工业流程如下图所示:
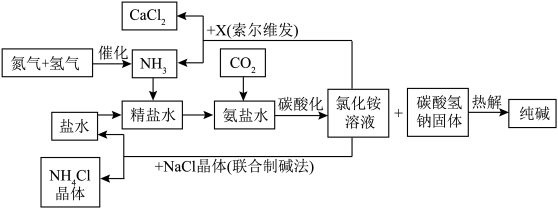
1.下列有关海水资源开发和利用的描述中,正确的是
2.侯德榜发明了制碱与制氨结合的联合制碱法,为纯碱和氮肥工业技术发展作出了杰出的贡献。 下列叙述不正确的是
3.“侯氏制碱法”生产纯碱的主要反应是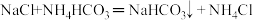 。如图是三种物质的溶解度曲线。下列选项的叙述正确的是
。如图是三种物质的溶解度曲线。下列选项的叙述正确的是

海洋是地球上最大的储水库,其储水量约占全球总储水量的 96.5%。海水中蕴藏着丰富的化学资源,人类正运用各种方法,对海水进行科学的开发和综合利用。工业流程如下图所示:

1.下列有关海水资源开发和利用的描述中,正确的是
| A.海水淡化:蒸馏法淡化海水是利用海水中各组分的颗粒大小不同 |
| B.海水晒盐:蒸发结晶池得到粗盐,剩余的母液为氯化钠的饱和溶液 |
| C.粗盐提纯:除去粗盐中泥沙等难溶性杂质,先将固体溶解再蒸发结晶 |
| D.粗盐精制:除去粗盐中可溶性杂质 Na2SO4,可选用足量 Ba(NO3)2溶液 |
| A.合成氨原料中 N2、H2中常含有 CO2和水蒸气,反应前要净化。在实验室可采用先通足量氢氧化钠溶液,再通过足量浓硫酸 |
| B.氨碱工业中,为增大二氧化碳在氨碱水中的溶解度,可减小压强 |
| C.“索尔维法”中将氯化铵溶液与 X 混合产生大量废弃物 CaCl2,X 为 Ca(OH)2 |
| D.联合制碱法中实现了 NaCl 的回收再利用,大大提高了产率 |
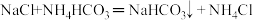 。如图是三种物质的溶解度曲线。下列选项的叙述正确的是
。如图是三种物质的溶解度曲线。下列选项的叙述正确的是 
| A.NaCl 中混有少量 NH4Cl,可用降温结晶提纯 NaCl |
| B.60℃,NH4Cl 的溶液的溶质质量分数一定大于 NaHCO3溶液的溶质质量分数 |
| C.析出 NaHCO3晶体的原因可能是同温下 NaHCO3的溶解度远小于 NH4Cl |
| D.20℃时,100g 水中加入 5.85g NaCl 和 7.9g NH4HCO3固体,肯定有 NaHCO3晶体析出 |
您最近一年使用:0次



