氯化钠是一种重要的资源,在海水中储量丰富。海水晒盐得到的粗盐中含不溶性杂质,制成精盐的操作流程如下:
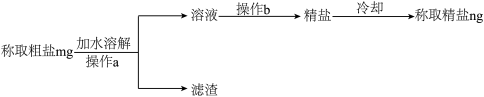
I.称取mg粗盐样品;称量时,在___________ (填仪器名称)上放一张称量纸,然后按去皮键,用___________ (填仪器名称)取粗盐加到称量纸上,直到天平显示mg。
II.操作a的名称是___________ ;操作b的名称是___________ ,此操作中玻璃棒的作用是___________ 。
III.溶解过程中适量水的目的是___________ 。
A保证氯化钠全部溶解
B提高实验效率
C加快固体溶解速度
D使滤液澄清

I.称取mg粗盐样品;称量时,在
II.操作a的名称是
III.溶解过程中适量水的目的是
A保证氯化钠全部溶解
B提高实验效率
C加快固体溶解速度
D使滤液澄清
20-21九年级上·上海青浦·期中 查看更多[3]
上海市青浦区青浦区实验中学2020-2021学年九年级上学期期中化学试题(已下线)实验活动8 粗盐中难溶性杂质的去除-2020-2021学年九年级化学下册同步基础知识速练(人教版)第十一单元盐和化肥实验活动8粗盐中难溶性杂质的去除2023步步升
更新时间:2020-12-14 14:04:28
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】海洋中蕴含丰富的资源。
(1)海水淡化
①海水淡化是解决淡水资源不足的重要方法,下列方法中,可以使海水淡化的是_______ (填字母序号)
A.过滤 B.吸附 C.沉降 D.蒸馏
②用化学方法区分蒸馏水和海水可采用的试剂是___________ 。
(2)利用海水制取纯碱和金属镁的流程如图所示,试回答问题:

①1925年我国化学家___________ 创立了联合制碱法,促进了世界制碱技术的发展。
②步骤Ⅰ粗盐形成精盐水的过程中需除去泥沙。除去泥沙需要经过溶解、过滤、蒸发三个步骤。均要用到玻璃棒,其中玻璃棒在蒸发中的作用是___________ 。
③步骤Ⅱ中吸氨的目的是___________ 。
④其第Ⅲ步反应的化学方程式为___________ 。
⑤在工业生产中为了减低成本,步骤Ⅳ中所加试剂最好选择的是___________ 。
⑥步骤第Ⅵ步反应的化学方程式为___________ 。
步骤Ⅰ粗盐形成精盐水的过程中还要除去MgCl2、CaCl2、Na2SO4杂质除杂流程如图:

(3)加入试剂的目的及反应原理
步骤②的目的是除去___________ ,反应的化学方程式为___________ ;
步骤③的目的是除去___________ ,反应的化学方程式为___________ ;
步骤④的目的是除去CaCl2和BaCl2,反应的化学方程式分别为___________ ;___________ ;
步骤⑥的目的是除去NaOH和Na2CO3,反应的化学方程式分别为___________ ;___________ 。
(1)海水淡化
①海水淡化是解决淡水资源不足的重要方法,下列方法中,可以使海水淡化的是
A.过滤 B.吸附 C.沉降 D.蒸馏
②用化学方法区分蒸馏水和海水可采用的试剂是
(2)利用海水制取纯碱和金属镁的流程如图所示,试回答问题:

①1925年我国化学家
②步骤Ⅰ粗盐形成精盐水的过程中需除去泥沙。除去泥沙需要经过溶解、过滤、蒸发三个步骤。均要用到玻璃棒,其中玻璃棒在蒸发中的作用是
③步骤Ⅱ中吸氨的目的是
④其第Ⅲ步反应的化学方程式为
⑤在工业生产中为了减低成本,步骤Ⅳ中所加试剂最好选择的是
⑥步骤第Ⅵ步反应的化学方程式为
步骤Ⅰ粗盐形成精盐水的过程中还要除去MgCl2、CaCl2、Na2SO4杂质除杂流程如图:

(3)加入试剂的目的及反应原理
步骤②的目的是除去
步骤③的目的是除去
步骤④的目的是除去CaCl2和BaCl2,反应的化学方程式分别为
步骤⑥的目的是除去NaOH和Na2CO3,反应的化学方程式分别为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海洋是巨大的资源宝库,从海洋中可以获得很多物质。
(1)通过晾晒海水能制得粗盐,但得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等)。
①实验室中粗盐提纯的一些步骤中的一些做法正确的是____________
A 溶解:用玻璃棒搅拌以加速溶解
B 过滤:利用过滤操作将粗盐水中的杂质全部除尽
C 蒸发:等蒸发皿中水分蒸干便停止加热
D 计算产率:将精盐直接转移到天平的托盘上称量
②过滤操作中玻璃棒的末端要轻轻的斜靠在____________ 一边。蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作是_______________ 。
③下列操作可能导致精盐产率偏高的是_______________ (填字母)。
a.食盐没有完全溶解即过滤
b.过滤时液面高于滤纸边缘
c.器皿上粘有的精盐没有全部转移到天平上称量
(2)海水中含有丰富的镁,目前世界上生产的镁60%来自于海水。分离出食盐的海水称作苦卤水,其中含有丰富的MgCl2。工业上以苦卤水为原料制取金属镁的流程如下:

①写出沉淀槽中发生反应的化学方程式:_______________ 、_______________ 。
②Y与Z反应后的产物溶于水可得X溶液,从而实现了Y的循环利用,则Z的化学式为_______________ ,X溶液的名称是_______________ 。
③烘干后得到的MgCl2中可能含有的杂质是_______________ 。
(1)通过晾晒海水能制得粗盐,但得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等)。
①实验室中粗盐提纯的一些步骤中的一些做法正确的是
A 溶解:用玻璃棒搅拌以加速溶解
B 过滤:利用过滤操作将粗盐水中的杂质全部除尽
C 蒸发:等蒸发皿中水分蒸干便停止加热
D 计算产率:将精盐直接转移到天平的托盘上称量
②过滤操作中玻璃棒的末端要轻轻的斜靠在
③下列操作可能导致精盐产率偏高的是
a.食盐没有完全溶解即过滤
b.过滤时液面高于滤纸边缘
c.器皿上粘有的精盐没有全部转移到天平上称量
(2)海水中含有丰富的镁,目前世界上生产的镁60%来自于海水。分离出食盐的海水称作苦卤水,其中含有丰富的MgCl2。工业上以苦卤水为原料制取金属镁的流程如下:

①写出沉淀槽中发生反应的化学方程式:
②Y与Z反应后的产物溶于水可得X溶液,从而实现了Y的循环利用,则Z的化学式为
③烘干后得到的MgCl2中可能含有的杂质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组同学欲除去固体氯化钠中混有的杂质氯化钙,设计实验方案流程如图:

(1)步骤①加水的目的是______________ 。
(2)步骤②中发生反应的化学方程式为______________ 。
(3)加入过量盐酸对得到的氯化钠纯度______________ (填“有”或“无”)影响;操作b的名称是 ______________ ,其中玻璃棒的作用是 ______________ 。

(1)步骤①加水的目的是
(2)步骤②中发生反应的化学方程式为
(3)加入过量盐酸对得到的氯化钠纯度
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】实验室中有一包由 KCl、MgSO4,和CaCl2组成的固体很合物,某校研究性学习小组的同学为了除去其中的MgSO4和CaCl2,得到纯净的 KCl,设计了如下实验方案。请你回答下列问题:

(1)X 溶液与 Ba(OH) 溶液反应的化学方程式是
溶液反应的化学方程式是_____
(2)Y 溶液中溶质的化学式是_____
(3)该实验中盐酸的作用是_____
(4)蒸发过程中玻璃棒的作用是_____
(5)原固体样品中含KClm1g,最后到KCl的固体 m2g,则 m1_____ m2(填“>”、“<”或“=”)

(1)X 溶液与 Ba(OH)
 溶液反应的化学方程式是
溶液反应的化学方程式是(2)Y 溶液中溶质的化学式是
(3)该实验中盐酸的作用是
(4)蒸发过程中玻璃棒的作用是
(5)原固体样品中含KClm1g,最后到KCl的固体 m2g,则 m1
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】地球是一颗美丽的蓝色星球,海水占了全球水资源的97%。海水资源的开发和利用具有非常广阔的前景。海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如图:
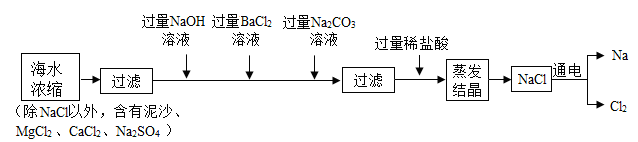
(1)加入过量Na2CO3溶液的目的是除去______ 。
(2)写出流程中制备钠的化学方程式______ ,若制得 23 kg金属钠,至少需要NaCl的质量为______ kg。
(3)实验所得NaCl质量______ 浓缩海水中的氯化钠质量(选填“大于”、“小于”或“等于”)。

(1)加入过量Na2CO3溶液的目的是除去
(2)写出流程中制备钠的化学方程式
(3)实验所得NaCl质量
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐。粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。
提示:氢氧化钙微溶于水
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验。

[交流与表达]
(1)实验步骤③的目的是_ 。
(2)实验操作X的名称是_ 。
(3)实验步骤⑤用蒸发溶剂的方法获取食盐晶体,在蒸发食盐溶液的过程中要使用玻璃棒,作用是________ 。
[反思与评价]
(4)有同学认为原实验方案不完善,做出这种评价的依据是________ 。
(5)为了完善原实验方案,你设计的实验是_ (仅写出补充部分的实验操作)。
(6)如果用完善后的实验方案完成实验,最终所得实验的产率要偏_____ (填“高”或“低”)。
提示:氢氧化钙微溶于水
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验。

[交流与表达]
(1)实验步骤③的目的是
(2)实验操作X的名称是
(3)实验步骤⑤用蒸发溶剂的方法获取食盐晶体,在蒸发食盐溶液的过程中要使用玻璃棒,作用是
[反思与评价]
(4)有同学认为原实验方案不完善,做出这种评价的依据是
(5)为了完善原实验方案,你设计的实验是
(6)如果用完善后的实验方案完成实验,最终所得实验的产率要偏
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用海水提取粗盐的过程如下图所示,回答有关问题。
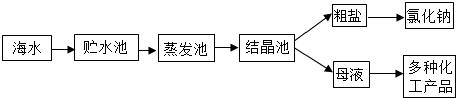
(1)一定质量的海水,通过贮水池引入到蒸发池,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量会______ (填“增大”、“不变”或“减小”)。
(2)粗盐中含有的难溶性杂质,在实验室里可以通过溶解、过滤、蒸发等操作将其去除,这些操作中都会用到仪器是______ 。
(3)用氯化钠固体配制100g质量分数为20%的氯化钠溶液。配制时,涉及以下实验步骤:A.称量及量取B.计算C.溶解D.装瓶贴标签。其正确的实验步骤顺序是______ (填字母)。

(1)一定质量的海水,通过贮水池引入到蒸发池,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量会
(2)粗盐中含有的难溶性杂质,在实验室里可以通过溶解、过滤、蒸发等操作将其去除,这些操作中都会用到仪器是
(3)用氯化钠固体配制100g质量分数为20%的氯化钠溶液。配制时,涉及以下实验步骤:A.称量及量取B.计算C.溶解D.装瓶贴标签。其正确的实验步骤顺序是
您最近一年使用:0次



