实验室可用氢氧化钠溶液吸收二氧化碳(2NaOH+CO2=Na2CO3+H2O),现有 100g 质量分数为16%的氢氧化钠溶液,可吸收二氧化碳的质量是多少?
更新时间:2020-12-23 08:58:24
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。CO2加氢制甲醇的总反应可表示为:CO2+3H2 CH3OH+H2O,若制得甲醇16t,计算减少CO2的质量(写出计算过程及结果)。
CH3OH+H2O,若制得甲醇16t,计算减少CO2的质量(写出计算过程及结果)。
 CH3OH+H2O,若制得甲醇16t,计算减少CO2的质量(写出计算过程及结果)。
CH3OH+H2O,若制得甲醇16t,计算减少CO2的质量(写出计算过程及结果)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】工业领域利用高效能催化剂制备过氧化氢的原理: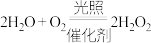 ,一定量的氧气与足量的水充分反应,能制备10吨68%的
,一定量的氧气与足量的水充分反应,能制备10吨68%的 溶液,试计算:
溶液,试计算:
(1)10吨68%的 溶液中
溶液中 的质量为
的质量为______ 吨。
(2)理论上需要消耗氧气的质量为多少?
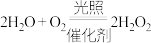 ,一定量的氧气与足量的水充分反应,能制备10吨68%的
,一定量的氧气与足量的水充分反应,能制备10吨68%的 溶液,试计算:
溶液,试计算:(1)10吨68%的
 溶液中
溶液中 的质量为
的质量为(2)理论上需要消耗氧气的质量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】工业纯碱中含少量氯化钠。兴趣小组分别采用不同的方法测定工业纯碱样品中碳酸钠的质量分数。
(1)方法一:差量法。称取W克样品与足量的稀盐酸充分反应,生成的二氧化碳通过装有试剂X的乙装置,并利用测量乙装置增加的质量,求得样品中碳酸钠的质量分数。该方法中试剂X可选用___________。
(2)方法二:沉淀法。利用氯化钙与纯碱反应生成沉淀,然后称量出沉淀的质量,现称取15克样品完全溶解于水中配成60克样品溶液,取三个烧杯分三次进行实验,每次加入30克氯化钙溶液充分反应,过滤、洗涤、干燥所得的沉淀质量记录如表。
①如表所示,哪几个烧杯内样品中的纯碱完全反应___________ 。
②请计算样品中碳酸钠的质量分数__________ ?

(1)方法一:差量法。称取W克样品与足量的稀盐酸充分反应,生成的二氧化碳通过装有试剂X的乙装置,并利用测量乙装置增加的质量,求得样品中碳酸钠的质量分数。该方法中试剂X可选用___________。
| A.氢氧化钠 |
| B.氢氧化钡 |
| C.氯化钡 |
| D.饱和碳酸氢钠溶液 |
| 烧杯1 | 烧杯2 | 烧杯3 | |
| 样品溶液(克) | 10 | 20 | 30 |
| 氯化钙溶液(克) | 30 | 30 | 30 |
| 沉淀质量(克) | 2 | 4 | 5 |
②请计算样品中碳酸钠的质量分数

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】氧化铁和炭粉的混合物35.6 g加热后恰好完全反应,将生成的气体通入过量的澄清石灰水中,气体全部被吸收,可得到白色沉淀30 g,试求原混合物中氧化铁和炭粉各多少g?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取10g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
试回答下列问题:
(1)题目表格中,m=______。
(2)黄铜样品中锌的质量分数为______。
(3)计算所用稀硫酸中硫酸的质量分数是多少?
| 加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
| 第1次 | 10 | m |
| 第2次 | 10 | 7.4 |
| 第3次 | 10 | 6.1 |
| 第4次 | 10 | 5.6 |
| 第5次 | 10 | 5.6 |
试回答下列问题:
(1)题目表格中,m=______。
(2)黄铜样品中锌的质量分数为______。
(3)计算所用稀硫酸中硫酸的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】学校兴趣小组的同学为了测定某黄铜(铜锌合金)样品中铜的质量分数,取10g该黄铜样品于烧杯中,向其中逐滴滴加100g稀硫酸,产生的气体质量随加入稀硫酸质量的变化关系如图所示。

请完成下列分析及计算:
(1)当稀硫酸滴加至100g时,烧杯中的溶质有______ (填化学式)。
(2)计算该稀硫酸的溶质质量分数。

请完成下列分析及计算:
(1)当稀硫酸滴加至100g时,烧杯中的溶质有
(2)计算该稀硫酸的溶质质量分数。
您最近一年使用:0次


 。根据化学反应方程式计算,生成24g氧气需硝酸钾的质量是多少?
。根据化学反应方程式计算,生成24g氧气需硝酸钾的质量是多少?



