某气体由H2、CO中的一种或两种组成,某化学兴趣小组对该气体的组成进行探究。
【提出问题】该气体由什么物质组成?
【提出假设】猜想Ⅰ:只有氢气;
猜想Ⅱ:只有一氧化碳;
猜想Ⅲ:___________ ;
【提供信息】由H2、CO中的一种或两种组成的气体均能在氧气中安静地燃烧。
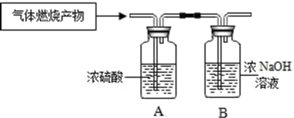
【设计实验】将该气体在氧气中完全燃烧的产物依次通过装置A、B,根据装置A、B中物质质量的变化情况来推测该气体的组成。(浓硫酸具有吸水性,NaOH能与二氧化碳反应从而吸收二氧化碳)
【现象与结论】
【分析讨论】
(1)装置A质量增加,说明气体燃烧的产物中有___________ 生成,推知该气体成分中一定含有___________ 元素;装置B质量增加,说明该气体燃烧的产物中有___________ 生成,推知该气体成分中一定含有___________ 元素。
(2)若用石灰水代替浓NaOH溶液,B中能观察到的现象是___________ ,反应的化学方程式为:___________ 。
【反思】若某纯净物完全燃烧,将其产物依次通过该套实验装置A、装置B,发现装置A、B的质量都增加了,则该纯净物可能是___________ (任写一种物质的化学式或名称)。

【提出问题】该气体由什么物质组成?
【提出假设】猜想Ⅰ:只有氢气;
猜想Ⅱ:只有一氧化碳;
猜想Ⅲ:
【提供信息】由H2、CO中的一种或两种组成的气体均能在氧气中安静地燃烧。
【设计实验】将该气体在氧气中完全燃烧的产物依次通过装置A、B,根据装置A、B中物质质量的变化情况来推测该气体的组成。(浓硫酸具有吸水性,NaOH能与二氧化碳反应从而吸收二氧化碳)
【现象与结论】
| 现象 | 结论 |
| ①装置A质量增加,装置B质量无变化 | 猜想 |
| ②装置A质量 | 猜想Ⅱ成立 |
| ③装置A质量增加,装置B质量 | 猜想Ⅲ成立 |
(1)装置A质量增加,说明气体燃烧的产物中有
(2)若用石灰水代替浓NaOH溶液,B中能观察到的现象是
【反思】若某纯净物完全燃烧,将其产物依次通过该套实验装置A、装置B,发现装置A、B的质量都增加了,则该纯净物可能是
更新时间:2020-12-19 19:29:42
|
相似题推荐
科学探究题
|
较易
(0.85)
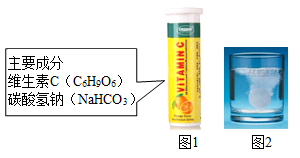
【推荐1】某化学兴趣小组的同学们意外发现把一种保健品维 泡腾片(主要成分如图1所示)溶于水,有许多气泡产生(如图2所示),它们对气泡的成分产生了好奇,于是进行了如下探究活动。
泡腾片(主要成分如图1所示)溶于水,有许多气泡产生(如图2所示),它们对气泡的成分产生了好奇,于是进行了如下探究活动。
【猜想与假设】丽萍同学认为:该气体可能是 、
、 、
、  、
、 、
、 。
。
王涛同学认为:不可能含有 ,因为
,因为 ______ 。
李强同学认为:不可能含有 和
和 ,因为从药品安全角度考虑,
,因为从药品安全角度考虑, 有毒,
有毒, 
______ 。
该组同学认为:该气体可能含有 、
、 中的一种或两种。
中的一种或两种。
【实验与现象】
①将气体通入澄清石灰水中,澄清石灰水变浑浊;
②将带火星的木条伸入该气体中,木条没有复燃。
【结论与拓展】
(1)由实验①可知,该气体肯定含有______ 。写出该反应的化学方程式 ______ 。
(2)由实验②______ (选填“能”或“不能”)确定该气体中不含氧气,理由是 ______ 。若要证明有氧气,请你帮助设计方法: ______ 。
 泡腾片(主要成分如图1所示)溶于水,有许多气泡产生(如图2所示),它们对气泡的成分产生了好奇,于是进行了如下探究活动。
泡腾片(主要成分如图1所示)溶于水,有许多气泡产生(如图2所示),它们对气泡的成分产生了好奇,于是进行了如下探究活动。
【猜想与假设】丽萍同学认为:该气体可能是
 、
、 、
、  、
、 、
、 。
。王涛同学认为:不可能含有
 ,因为
,因为 李强同学认为:不可能含有
 和
和 ,因为从药品安全角度考虑,
,因为从药品安全角度考虑, 有毒,
有毒, 
该组同学认为:该气体可能含有
 、
、 中的一种或两种。
中的一种或两种。【实验与现象】
①将气体通入澄清石灰水中,澄清石灰水变浑浊;
②将带火星的木条伸入该气体中,木条没有复燃。
【结论与拓展】
(1)由实验①可知,该气体肯定含有
(2)由实验②
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐2】天然气的主要成分是甲烷(CH4),某化学小组对甲烷在纯氧中燃烧的产物产生兴趣,于是进行如下探究。
【提出问题】甲烷在纯氧中燃烧的产物中含有哪些物质?
【猜想与假设】甲:CO2、H2O;乙:CO、H2O;丙:NH3、CO2、H2O;丁:CO2、CO、H2O
【查阅资料】无水CuSO4遇水变蓝
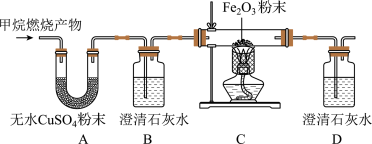
【实验探究】将甲烷燃烧的产物依次通过下列装置(装置中物质均足量)。
(1)天然气属于________________ 物(填“纯净”或“混合”)。
(2)甲同学认为丙同学的猜想是不合理的,理由是____________________________ 。
(3)实验中用纯净的O2而不用空气的原因是_________________________________ 。
(4)实验中观察到装置A的实验现象_______________ ,说明有水生成,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,C发生反应的化学方程式_________________ ,由此推断________ 同学的猜想成立;B中澄清石灰水变浑浊的化学方程式为_________________ 。
(5)请指出该实验的一个不足之处:_____________________ 。
(6)实验中A装置和B装置的顺序不能对调,原因是_______________________ 。
【反思与交流】
(7)为尽量避免不完全燃烧产生有毒的CO气体而污染环境,含碳元素的物质燃烧时必须满足的条件是___________________________________ 。
【提出问题】甲烷在纯氧中燃烧的产物中含有哪些物质?
【猜想与假设】甲:CO2、H2O;乙:CO、H2O;丙:NH3、CO2、H2O;丁:CO2、CO、H2O
【查阅资料】无水CuSO4遇水变蓝
【实验探究】将甲烷燃烧的产物依次通过下列装置(装置中物质均足量)。

(1)天然气属于
(2)甲同学认为丙同学的猜想是不合理的,理由是
(3)实验中用纯净的O2而不用空气的原因是
(4)实验中观察到装置A的实验现象
(5)请指出该实验的一个不足之处:
(6)实验中A装置和B装置的顺序不能对调,原因是
【反思与交流】
(7)为尽量避免不完全燃烧产生有毒的CO气体而污染环境,含碳元素的物质燃烧时必须满足的条件是
您最近一年使用:0次
科学探究题
|
较易
(0.85)
【推荐3】小耿同学在某门户网站上看到一段震撼的视频,将大块的钠扔入湖水中瞬间产 生爆炸。于是,他对钠和水的反应产生了强烈的好奇,并在老师和同学的帮助下进行相关探究。
【查阅资料】
①钠是一种活泼金属,常温下不与煤油反应,能与氧气、水等物质发生反应,与水剧烈反应能生成一种可燃性气体。
②钠的密度是0.97g/cm3,煤油的密度是0.8g/cm3,水的密度是1g/cm3。
【实验探究】
在小扈同学的启发下,小耿同学设计了如图1所示的一套钠与水反应的实验装置(夹持仪器 已略)。
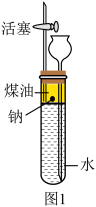
【实验步骤】
①检查装置气密性;
②向大试管中加入一定体积煤油;
③用小刀切一小块钠,放入大试管,塞上橡皮塞;
④打开活塞,通过长颈漏斗向试管中加入水,使煤油的液面升至胶塞,关闭活塞,观察现象。
请回答下列问题:
(1)步骤①中检查该装置气密性的方法是___ 。
(2)步骤②中煤油的作用是___ 。
(3)实验中长颈漏斗的作用除了可以方便添加液体,还能___ 。
【实验反思】实验结束后,小戴同学对于剩余溶液的溶质成分产生了好奇,并在老师的指导下运用如图2所示的装置进行探究,在此基础上,绘出了如图3所示的图象。
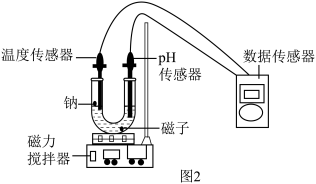

根据图3回答下列问题:
(4)钠和水的反应属于___ 反应(填“吸热”或者“放热”)。
(5)小乐同学认为通过图3就可以初步判断剩余溶液的溶质为___ ,理由是___ 。
【实验拓展】
(6)写出钠和水反应的化学方程式为___ 。
(7)小季同学将图1试管中的水换成足量的硫酸铜溶液,观察到产生了气泡和一种蓝色沉淀,反应后,溶液中SO42﹣的质量分数___ (填“变大”、“不变”或者“变小”)。
【查阅资料】
①钠是一种活泼金属,常温下不与煤油反应,能与氧气、水等物质发生反应,与水剧烈反应能生成一种可燃性气体。
②钠的密度是0.97g/cm3,煤油的密度是0.8g/cm3,水的密度是1g/cm3。
【实验探究】
在小扈同学的启发下,小耿同学设计了如图1所示的一套钠与水反应的实验装置(夹持仪器 已略)。

【实验步骤】
①检查装置气密性;
②向大试管中加入一定体积煤油;
③用小刀切一小块钠,放入大试管,塞上橡皮塞;
④打开活塞,通过长颈漏斗向试管中加入水,使煤油的液面升至胶塞,关闭活塞,观察现象。
请回答下列问题:
(1)步骤①中检查该装置气密性的方法是
(2)步骤②中煤油的作用是
(3)实验中长颈漏斗的作用除了可以方便添加液体,还能
【实验反思】实验结束后,小戴同学对于剩余溶液的溶质成分产生了好奇,并在老师的指导下运用如图2所示的装置进行探究,在此基础上,绘出了如图3所示的图象。


根据图3回答下列问题:
(4)钠和水的反应属于
(5)小乐同学认为通过图3就可以初步判断剩余溶液的溶质为
【实验拓展】
(6)写出钠和水反应的化学方程式为
(7)小季同学将图1试管中的水换成足量的硫酸铜溶液,观察到产生了气泡和一种蓝色沉淀,反应后,溶液中SO42﹣的质量分数
您最近一年使用:0次
【推荐1】蔗糖是生活中常见的一种物质,某兴趣小组对“蔗糖的组成”进行了探究。
【提出猜想】小组同学认为绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气,葡萄糖进一步转化为蔗糖,故蔗糖中一定含有碳、氢元素,可能含有氧元素。
【实验探究】
方案一:小明将蔗糖放在氧气中燃烧,检验生成物中有水和二氧化碳得出结论“蔗糖是由碳、氢、氧三种元素组成的”。小刚认为该方案不合理,实验只能说明蔗糖中一定含有碳,氢元素,不能确定是否含有氧元素,理由是__________ 。
方案二:用如图所示装置进行实验,实验开始先通入一会儿氮气,然后关闭弹簧夹,点燃酒精灯给 蔗糖加强热。
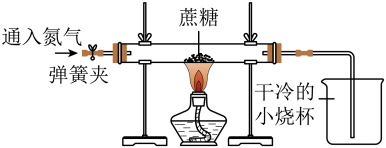
(1)观察到________ 出现,说明蔗糖中含有氢元素和氧元素。
(2)观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,并继续利用上图所示装置,另选试剂进行了验证单质碳的实验。实验过程和现象如下:
写出上述实验过程中,烧杯中反应的化学方程式________ 。
【实验结论】蔗糖是由碳、氢、氧三种元素组成的。
【拓展交流】
(1)方案二中,先通入一会儿氮气的原因是_______ 。
(2)查阅资料得知蔗糖的化学式为C12H22O11。小红发现:蔗糖分子中氢原子的数目是氧原子数目的2倍,但是,蔗糖中氧元素质量却是氢元素质量的8倍,导致出现这种情况的原因是______ 。
【提出猜想】小组同学认为绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气,葡萄糖进一步转化为蔗糖,故蔗糖中一定含有碳、氢元素,可能含有氧元素。
【实验探究】
方案一:小明将蔗糖放在氧气中燃烧,检验生成物中有水和二氧化碳得出结论“蔗糖是由碳、氢、氧三种元素组成的”。小刚认为该方案不合理,实验只能说明蔗糖中一定含有碳,氢元素,不能确定是否含有氧元素,理由是
方案二:用如图所示装置进行实验,实验开始先通入一会儿氮气,然后关闭弹簧夹,点燃酒精灯给 蔗糖加强热。

(1)观察到
(2)观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,并继续利用上图所示装置,另选试剂进行了验证单质碳的实验。实验过程和现象如下:
| 实验过程 | 实验现象 |
| 小烧杯中加入足量的澄清石灰水,往硬纸玻璃管中通入氧气,点燃酒精灯 | (一)硬纸玻璃管中的黑色固体剧烈燃烧,发出白光; (二) |
【实验结论】蔗糖是由碳、氢、氧三种元素组成的。
【拓展交流】
(1)方案二中,先通入一会儿氮气的原因是
(2)查阅资料得知蔗糖的化学式为C12H22O11。小红发现:蔗糖分子中氢原子的数目是氧原子数目的2倍,但是,蔗糖中氧元素质量却是氢元素质量的8倍,导致出现这种情况的原因是
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐2】某化学兴趣小组将铁钉放在硫酸铜溶液中,得到了紫红色的铜,但把金属钠放到硫酸铜溶液中,实验并非如想象的有紫红色铜析出,而是生成一种蓝色沉淀,并放出气体,同学们非常好奇,于是进行实验探究。
【提出问题】金属钠放到硫酸铜溶液中到底发生了怎样的化学反应?
【猜想与假设】
猜想一:只发生了钠与硫酸铜反应;
猜想二:只发生了钠与水反应;
猜想三:发生了钠与水反应后,生成的物质再与硫酸铜反应。
【查阅资料】钠是非常活泼的金属,能与水发生剧烈反应,并放出气体,生成的溶液显碱性。
【设计并进行实验】
(1)实验一:把一小块擦干净的金属钠放到装有少量蒸馏水的试管中,点燃生成的气体,听到“噗”的一声后燃烧起来,说明有______ (填气体的化学式)生成。
实验二:在剩余的溶液中滴加硫酸铜溶液,发现有蓝色沉淀。
【实验总结】
(2)实验一中发生的化学反应属于四大基本反应类型中的______ 反应;实验二中发生反应的化学方程式是______ ;由此可知,猜想______ 是正确的。
【实验拓展】
(3)该兴趣小组又将一小块擦干净的金属钠放入盛有FeCl3溶液的烧杯中,观察到与钠在硫酸铜溶液中类似的实验现象(生成一种红褐色沉淀,并放出气体),请尝试猜测红褐色沉淀可能是什么物质,并写出其对应的化学式______ 。
【反思交流】
(4)在金属活动性顺序中,活动性较强的金属______ (填“一定”或“不一定”)能将位于其后面的金属从它的盐溶液中置换出来。
【提出问题】金属钠放到硫酸铜溶液中到底发生了怎样的化学反应?
【猜想与假设】
猜想一:只发生了钠与硫酸铜反应;
猜想二:只发生了钠与水反应;
猜想三:发生了钠与水反应后,生成的物质再与硫酸铜反应。
【查阅资料】钠是非常活泼的金属,能与水发生剧烈反应,并放出气体,生成的溶液显碱性。
【设计并进行实验】
(1)实验一:把一小块擦干净的金属钠放到装有少量蒸馏水的试管中,点燃生成的气体,听到“噗”的一声后燃烧起来,说明有
实验二:在剩余的溶液中滴加硫酸铜溶液,发现有蓝色沉淀。
【实验总结】
(2)实验一中发生的化学反应属于四大基本反应类型中的
【实验拓展】
(3)该兴趣小组又将一小块擦干净的金属钠放入盛有FeCl3溶液的烧杯中,观察到与钠在硫酸铜溶液中类似的实验现象(生成一种红褐色沉淀,并放出气体),请尝试猜测红褐色沉淀可能是什么物质,并写出其对应的化学式
【反思交流】
(4)在金属活动性顺序中,活动性较强的金属
您最近一年使用:0次
【推荐3】在学习生活中常见的盐一课时,学生用Na2CO3和NaHCO3两种固体,分别与稀盐酸发生反应。

(1)NaHCO3与稀盐酸反应的化学方程式为_______ 。
【观察现象】Na2 CO3和NaHCO3两种固体,分别与稀盐酸发生反应。NaHCO3的反应更加剧烈一些。
【发现问题】为什么NaHCO3的反应更剧烈?
【进行实验】
(2)用如图所示操作,取浓度相同的Na2CO3溶液和NaHCO3溶液,分别滴加浓度_______ 的稀盐酸;
(3)观察到Na2CO3溶液刚滴入稀盐酸时,并没有气泡产生,发生的反应为:
_______ 。
(4)取浓度相同的Na2 CO3溶液和NaHCO3溶液,分别滴加少量浓度相同的CaCl2溶液。
观察到在Na2 CO3溶液中立即产生白色沉淀,而在NaHCO3溶液中没有明显现象,根据复分解反应的发生条件,分析在NaHCO3溶液中滴加少量CaCl2溶液没有明显现象的原因是_______ 。
【查阅资料】①碳酸钠与碳酸氢钠的溶解度如下表所示:
②碳酸钠溶液中通入CO2会发生反应: ;
;
(5)向饱和的碳酸钠溶液中不断通入CO2会观察到的现象是______ t。
(6)用饱和的碳酸钠溶液制取NaHCO3的产率最高的温度是______ 。

(1)NaHCO3与稀盐酸反应的化学方程式为
【观察现象】Na2 CO3和NaHCO3两种固体,分别与稀盐酸发生反应。NaHCO3的反应更加剧烈一些。
【发现问题】为什么NaHCO3的反应更剧烈?
【进行实验】
(2)用如图所示操作,取浓度相同的Na2CO3溶液和NaHCO3溶液,分别滴加浓度
(3)观察到Na2CO3溶液刚滴入稀盐酸时,并没有气泡产生,发生的反应为:

(4)取浓度相同的Na2 CO3溶液和NaHCO3溶液,分别滴加少量浓度相同的CaCl2溶液。
观察到在Na2 CO3溶液中立即产生白色沉淀,而在NaHCO3溶液中没有明显现象,根据复分解反应的发生条件,分析在NaHCO3溶液中滴加少量CaCl2溶液没有明显现象的原因是
【查阅资料】①碳酸钠与碳酸氢钠的溶解度如下表所示:
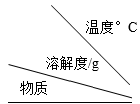 | 20 | 30 | 40 | 50 | 60 |
| 碳酸钠 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
| 碳酸氢钠 | 9.6 | 11.1 | 12.7 | 14.45 | 16.4 |
 ;
;(5)向饱和的碳酸钠溶液中不断通入CO2会观察到的现象是
(6)用饱和的碳酸钠溶液制取NaHCO3的产率最高的温度是
您最近一年使用:0次
科学探究题
|
较易
(0.85)
【推荐1】如图所示的实验中,通入的气体A是氢气和一氧化碳中的一种或两种,黑色粉末B是氧化铜和木炭粉中的一种或两种。实验中观察到的现象是:黑色粉末变红色,无水硫酸铜变蓝色,澄清石灰水变浑浊。
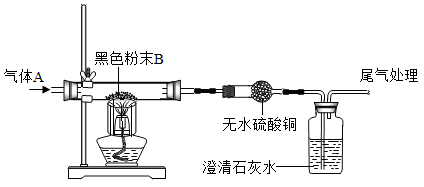
(1) 若气体A为纯净物,则A是____ , 黑色粉末B是___ 。
(2)若固体B为纯净物,则A是____ , 黑色粉末是CuO。

(1) 若气体A为纯净物,则A是
(2)若固体B为纯净物,则A是
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐2】随着环保意识的提高,人们对空气质量越来越关注。某实践活动小组在老师的带领下,对空气质量检测等开展了一系列项目式学习。
活动一:了解空气质量指数所表示的含义
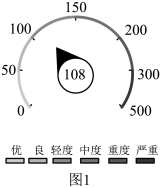
空气质量指数(Air Quality Index,简称AQ1)是定量描述空气质量状况的指数,分为六级,相对应空气质量的六个级别,其数值越大,说明空气污染状况越严重。
【思考分析】
(1)如图1是该日太原市的空气质量情况,该日的空气质量为__________ (填“优”“良”或“轻度污染”)。
(2)空气中二氧化硫(SO2)、二氧化氮(NO)的主要来源是_______ ,所引起的环境问题是_______ 。
活动二:认识微型空气质量“检测站”
【查询网络】微型空气质量检测系统用于实时、准确检测室外空气污染物,其结构如图2。
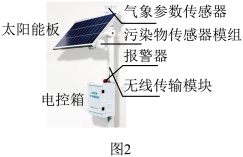
【交流思考】
(3)为防止金属电控箱表面锈蚀可进行的操作是______ 。太阳能板工作时进行的能量转化是_______ 。
活动三;调查微型空气质量“检测站”
【进行实践】同学们找到一个微型空气质量检测站,观察并记录不同时间显示的数据如表:
【交流思考】
(4)除显示器显示的内容外,还需要检测的空气污染物有________ (写一种)。
活动四:进行实践
同学们对某工厂附近的空气质量感到好奇,调研发现工厂为了获得充足的能量,长期采用燃煤技术。于是同学们猜测该废气中含有二氧化硫。
【查阅资料】二氧化硫是有刺激性气味的气体,能使澄清石灰水变浑浊,也能使品红溶液褪色。
(5)【设计并进行实验】
【反思评价】
(6)不选用澄清石灰水检验二氧化硫的原因是______ (用化学方程式表示)。
活动五:提出空气质量改进方案
【分享成果】
(7)“绿水青山就是金山银山。”为了保护人类赖以生存的空气,请你和兴趣小组同学思考,我们自己在校园中能做什么?___________ 。
活动一:了解空气质量指数所表示的含义
空气质量指数(Air Quality Index,简称AQ1)是定量描述空气质量状况的指数,分为六级,相对应空气质量的六个级别,其数值越大,说明空气污染状况越严重。
【思考分析】
(1)如图1是该日太原市的空气质量情况,该日的空气质量为

(2)空气中二氧化硫(SO2)、二氧化氮(NO)的主要来源是
活动二:认识微型空气质量“检测站”
【查询网络】微型空气质量检测系统用于实时、准确检测室外空气污染物,其结构如图2。

【交流思考】
(3)为防止金属电控箱表面锈蚀可进行的操作是
活动三;调查微型空气质量“检测站”
【进行实践】同学们找到一个微型空气质量检测站,观察并记录不同时间显示的数据如表:
| 二氧化氮/µg | 臭氧/µg | 一氧化碳/µg |
| 22.0 | 158.0 | 3.26 |
(4)除显示器显示的内容外,还需要检测的空气污染物有
活动四:进行实践
同学们对某工厂附近的空气质量感到好奇,调研发现工厂为了获得充足的能量,长期采用燃煤技术。于是同学们猜测该废气中含有二氧化硫。
【查阅资料】二氧化硫是有刺激性气味的气体,能使澄清石灰水变浑浊,也能使品红溶液褪色。
(5)【设计并进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| 收集一瓶工厂排放的气体,加入品红溶液,振荡 | 废气中含有二氧化硫 |
【反思评价】
(6)不选用澄清石灰水检验二氧化硫的原因是
活动五:提出空气质量改进方案
【分享成果】
(7)“绿水青山就是金山银山。”为了保护人类赖以生存的空气,请你和兴趣小组同学思考,我们自己在校园中能做什么?
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐3】氢氧化钠是重要的化工原料。某同学对氢氧化钠的性质进行了如图1探究:______ (填“吸收”或“放出”)热量。
(2)怎样证明CO2与NaOH溶液发生了反应?
【实验设计】同学们根据碱的化学性质,推测CO2与NaOH反应的化学方程式为______ ,并从不同的角度分别设计了实验加以验证。
【实验验证】
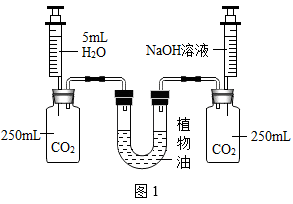
①从压强变化的角度探究。
按图1所示进行实验,将等体积水和氢氧化钠溶液同时全部注入集气瓶中,观察到U形管内左侧液面______ (填“高于”、“相平于”或“低于”)右侧液面,说明二氧化碳和氢氧化钠可以发生反应。
②利用“数字化实验”探究。______ 。
Ⅱ、实验测得烧杯中溶液的pH随时间的变化关系如图2所示,由图可推知反应过程中浓度不断减少的离子是______ (填离子符号)。
(2)怎样证明CO2与NaOH溶液发生了反应?
【实验设计】同学们根据碱的化学性质,推测CO2与NaOH反应的化学方程式为
【实验验证】
①从压强变化的角度探究。
按图1所示进行实验,将等体积水和氢氧化钠溶液同时全部注入集气瓶中,观察到U形管内左侧液面
②利用“数字化实验”探究。
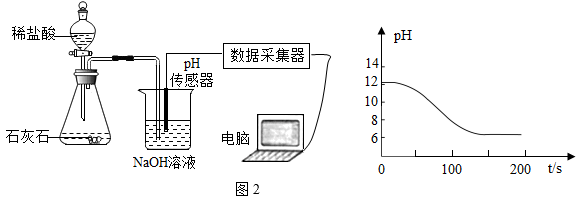
Ⅱ、实验测得烧杯中溶液的pH随时间的变化关系如图2所示,由图可推知反应过程中浓度不断减少的离子是
您最近一年使用:0次



