实验室有一份在空气中潮解变质的氢氧化钠样品,质量为1.5g。某实验小组将这份样品完全溶解,配成50g溶液。然后缓慢滴入7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液pH和溶液总质量,部分数据如下表所示:
请分析计算:
(1)第 次测量时,溶液中只有一种溶质。
(2)表中m= 。
(3)样品中碳酸钠的质量分数。(计算结果精确到0.1%)
(4)1.5g样品中氢氧化钠固体的质量。
| 测量次数 | 第1次 | 第6次 | 第16次 | 第21次 | 第26次 |
| 滴加的盐酸总质量/g | 0 | 5 | 15 | 20 | 25 |
| 溶液总质量/g | 50 | 55 | m | 69.78 | 74.78 |
| 溶液pH | 12.4 | 12.1 | 7.0 | 2.2 | 2.1 |
请分析计算:
(1)第 次测量时,溶液中只有一种溶质。
(2)表中m= 。
(3)样品中碳酸钠的质量分数。(计算结果精确到0.1%)
(4)1.5g样品中氢氧化钠固体的质量。
更新时间:2021-01-02 14:46:41
|
相似题推荐
计算题
|
较难
(0.4)
真题
解题方法
【推荐1】化肥对提高农作物的产量具有重要的作用,碳铵(碳酸氢铵)就是农民朋友经常使用的一种氮肥,碳铵易溶于水、受潮时常温分解,温度越高分解越快,遇碱时放出氨气。某校化学兴趣小组为测定某碳铵肥料样品的纯度,将8.5g样品加入足量的浓氢氧化钠溶液中共热,(碳铵中的杂质不与氢氧化钠反应,反应的方程式为NH4HCO3+2NaOH = Na2CO3+2H2O+NH3↑),把产生的所有NH3用足量的硫酸溶液吸收,同时测量两分钟内硫酸溶液增加的质量,结果如下表所示。
试回答下列问题:
(1)根据碳酸氢铵的性质,你认为在使用碳铵肥料时应注意的问题是___________________。
(2)请在坐标纸上,以反应时间为横坐标,以产生NH3质量为纵坐标,画出产生气体的质量随时间变化的关系曲线,并判断表中m约为_________________。
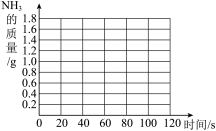
(3)试计算该样品中碳酸氢铵的质量分数(写出计算过程,计算结果保留一位小数)。
| 时间/S | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
试回答下列问题:
(1)根据碳酸氢铵的性质,你认为在使用碳铵肥料时应注意的问题是___________________。
(2)请在坐标纸上,以反应时间为横坐标,以产生NH3质量为纵坐标,画出产生气体的质量随时间变化的关系曲线,并判断表中m约为_________________。

(3)试计算该样品中碳酸氢铵的质量分数(写出计算过程,计算结果保留一位小数)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】向100 g溶质质量分数为14.6%的稀盐酸中,加入一定质量的Na2CO3溶液,充分反应后得到混合溶液200 g,该溶液中HCl的质量分数为3.65%。
(1)Na2CO3中元素质量分数最大的是_______ 。
(2)反应过程中加入Na2CO3溶液的溶质质量分数是多少(结果保留1位小数)?
(3)若要使反应后的混合溶液中HCl质量分数恢复到14.6%,需要向混合溶液中通入并溶解HCI气体的质量为多少(结果保留1位小数)?
(1)Na2CO3中元素质量分数最大的是
(2)反应过程中加入Na2CO3溶液的溶质质量分数是多少(结果保留1位小数)?
(3)若要使反应后的混合溶液中HCl质量分数恢复到14.6%,需要向混合溶液中通入并溶解HCI气体的质量为多少(结果保留1位小数)?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某工厂排放的废水中含有NaOH和Na2CO3,为了测定废水中NaOH的质量分数,取废水100g逐滴加入稀盐酸至过量,测得生成气体的质量与所加稀盐酸的质量关系如图所示。试计算:
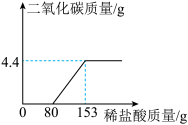
(1)当所取样品完全反应时,生成气体的质量为_____ g。
(2)恰好完全反应时所得溶液的溶质质量分数______ 。

(1)当所取样品完全反应时,生成气体的质量为
(2)恰好完全反应时所得溶液的溶质质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】鸡蛋壳的主要成分是碳酸钙(其它成分不溶于水也不与酸反应)。
化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做如下实验:
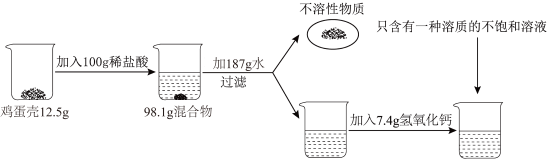
请回答下列问题:
(1)鸡蛋壳发生反应的化学方程式为___________________________;
(2)根据已知条件列出求解碳酸钙质量(X)的比例式______________;
(3)该鸡蛋壳中碳酸钙的质量分数为_______;
(4)最终所得溶液中溶质的质量分数为_______;
(5)用36.5%的浓盐酸配制上述稀盐酸需加水的质量为_______。
化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做如下实验:

请回答下列问题:
(1)鸡蛋壳发生反应的化学方程式为___________________________;
(2)根据已知条件列出求解碳酸钙质量(X)的比例式______________;
(3)该鸡蛋壳中碳酸钙的质量分数为_______;
(4)最终所得溶液中溶质的质量分数为_______;
(5)用36.5%的浓盐酸配制上述稀盐酸需加水的质量为_______。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】NaOH潮解后极易与空气中的CO2反应生成Na2CO3而变质.为测定实验室一瓶放置已久的烧碱中NaOH含量,某同学取适量的烧碱样品,溶于一定量的水得到200g溶液;再加入200g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g.请计算:
(1)反应产生的CO2的质量为___g.
(2)若所取烧碱样品为50.0g,则样品中NaOH的质量分数是_____?
(3)用同浓度的硫酸,与一瓶未变质、部分变质、或全部变质(杂质都是Na2CO3)的烧碱样品反应,需要硫酸的质量都相等.其原因是:__(从钠元素质量守恒的角度解释).
(1)反应产生的CO2的质量为___g.
(2)若所取烧碱样品为50.0g,则样品中NaOH的质量分数是_____?
(3)用同浓度的硫酸,与一瓶未变质、部分变质、或全部变质(杂质都是Na2CO3)的烧碱样品反应,需要硫酸的质量都相等.其原因是:__(从钠元素质量守恒的角度解释).
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】在我国青海湖地区有一种说法:冬天捞碱、夏天晒盐。这里的碱是指Na2CO3,盐是指NaCl,人们从盐湖中捞得的碱会含有少量NaCl。某研究性学习小组称取含NaCl的Na2CO3固体25.0g,将其配制成溶液,再向其中逐滴加入足量的7.3%的盐酸,使气体完全放出,共收集到8.8gCO2气体。
(1)计算原固体中Na2CO3的质量分数(计算结果保留一位小数);
(2)下表为研究性学习小组向上述所配制混合液中分三次逐滴滴加盐酸后,所记录的部分数据。关于Na2CO3和HCl的反应过程,经查阅资料可知:Na2CO3+HCl=NaCl+NaHCO3(Ⅰ),NaHCO3+HCl=NaCl+H2O+CO2↑(Ⅱ)。(已知反应Ⅰ完全后,反应Ⅱ才开始发生)
①请完成下列表格中未填的部分:
②根据表中数据在下面坐标系中画出CO2质量(纵坐标)与所加入盐酸质量(横坐标)的关系图______ 。
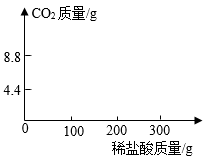
(1)计算原固体中Na2CO3的质量分数(计算结果保留一位小数);
(2)下表为研究性学习小组向上述所配制混合液中分三次逐滴滴加盐酸后,所记录的部分数据。关于Na2CO3和HCl的反应过程,经查阅资料可知:Na2CO3+HCl=NaCl+NaHCO3(Ⅰ),NaHCO3+HCl=NaCl+H2O+CO2↑(Ⅱ)。(已知反应Ⅰ完全后,反应Ⅱ才开始发生)
①请完成下列表格中未填的部分:
| 实验顺序 | 每次产生CO2气体的质量(g) |
| 第一次逐滴滴加盐酸100g | |
| 第二次逐滴滴加盐酸100g | 8.8 |
| 第三次逐滴滴加盐酸100g | 0 |

您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】某研究性学习小组在实验室发现一瓶存放多年的氢氧化钙,他们猜想可能发生了变质。为了获取数据,他们取六份该氢氧化钙样品分别与稀盐酸反应,测得部分数据用表、图所示如下,他们得出结论:氢氧化钙发生了部分变质。
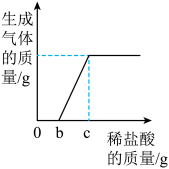
(1)氢氧化钙露置在空气中变质的原因是_____ 。
(2)a、b、c三个字母分别代表实验过程中的三个数据。实验过程中若上述三个数据均出现,你认为取用盐酸的质量至少是_______ 。请借助图像用b点数据对氢氧化钙发生部分变质给予解释_______ 。
(3)计算样品中氢氧化钙的质量分数(精确到0.1%)

| 第1份 | 第3份 | 第4份 | 第5份 | 第6份 | |
| 样品质量/g | 22.4 | 22.4 | 22.4 | 22.4 | 22.4 |
| 加入的盐酸质量/g | 40 | 120 | 160 | 200 | 240 |
| 气体的质量/g | 0 | a | 4.4 | 6.6 | 6.6 |
(1)氢氧化钙露置在空气中变质的原因是
(2)a、b、c三个字母分别代表实验过程中的三个数据。实验过程中若上述三个数据均出现,你认为取用盐酸的质量至少是
(3)计算样品中氢氧化钙的质量分数(精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】为测定一瓶久置的烧碱中氢氧化钠的含量,某同学取25.0 g样品,溶于水得到100g溶液,再加入100g稀硫酸,恰好完全反应。测得溶液质量为197.8g。请计算:
(1)NaOH中Na元素的质量分数为_____ (百分数表示)。
(2)反应产生CO2的质量为_______ 克。
(3)稀硫酸的溶质质量分数。
(1)NaOH中Na元素的质量分数为
(2)反应产生CO2的质量为
(3)稀硫酸的溶质质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】有一瓶久置的氢氧化钠固体,为测定其变质程度,某兴趣小组的同学称取了22.6g样品,溶于水配成了100g溶液,逐滴滴入某浓度的稀盐酸,产生气体的质量与加入稀盐酸的质量关系如图所示。按要求回答:

(1)样品中加入稀盐酸25g时,溶液中的溶质有NaOH和 。
(2)请列式计算样品中Na2CO3的质量分数(结果保留到0.1%);
(3)请在下图中画出生成NaCl质量与滴加稀盐酸的关系曲线,并做必要的标注。


(1)样品中加入稀盐酸25g时,溶液中的溶质有NaOH和 。
(2)请列式计算样品中Na2CO3的质量分数(结果保留到0.1%);
(3)请在下图中画出生成NaCl质量与滴加稀盐酸的关系曲线,并做必要的标注。

您最近一年使用:0次



