某兴趣小组同学去盐场参观,带回了部分粗盐样品,并对其进行了如下探究:
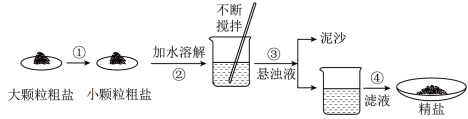
(1)操作①的作用为___________ 。操作③的名称是 ___________ 。操作④中用到玻璃棒,作用为 ___________ 。
(2)用提纯得到的“精盐”配制100g7.5%的氯化钠溶液。经检测,氯化钠的质量分数偏小,其原因可能有___________ (填序号)。
a 氯化钠固体不纯;
b 称量时精盐与砝码放反了;
c 量取水时仰视读数;
d 装瓶时,有少量溶液洒出
查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgC12一种)为了得到较纯净的氯化钠,小组同学将所得的“精盐”又作了如图处理:
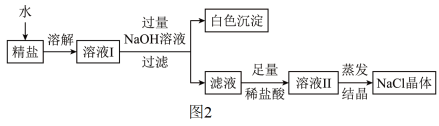
(3)往溶液Ⅰ中加入过量NaOH溶液的原因是___________ ,白色沉淀的化学式为 ___________ ,生成白色沉淀的化学方程式为 ___________ 。
(4)在得到的滤液中加入足量的稀盐酸的目的是___________ ,溶液Ⅱ中含有的离子为 ___________ (用符号表示);
(5)若实验过程中不考虑损耗,最终到的NaCl固体的质量将___________ (填“大于”“小于”或“等于”)原精盐中NaCl的质量。

(1)操作①的作用为
(2)用提纯得到的“精盐”配制100g7.5%的氯化钠溶液。经检测,氯化钠的质量分数偏小,其原因可能有
a 氯化钠固体不纯;
b 称量时精盐与砝码放反了;
c 量取水时仰视读数;
d 装瓶时,有少量溶液洒出
查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgC12一种)为了得到较纯净的氯化钠,小组同学将所得的“精盐”又作了如图处理:

(3)往溶液Ⅰ中加入过量NaOH溶液的原因是
(4)在得到的滤液中加入足量的稀盐酸的目的是
(5)若实验过程中不考虑损耗,最终到的NaCl固体的质量将
20-21九年级上·山东淄博·期中 查看更多[4]
山东省淄博市周村区(五四制)2020-2021学年九年级上学期期中化学试题(已下线)实验活动8 粗盐中难溶性杂质的去除-2020-2021学年九年级化学下册同步基础知识速练(人教版)第十一单元盐和化肥实验活动8粗盐中难溶性杂质的去除2023步步升山东省烟台市牟平区宁海中学2022-2023学年九年级上学期11月月考化学试题
更新时间:2020-12-22 10:52:38
|
相似题推荐
【推荐1】氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示
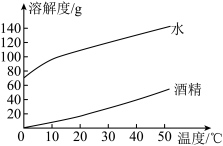
(1)上述图像表示_________ (填化学式)的溶解度曲线。
(2)40℃时,若将50g NaOH分别投入到100g水和100g酒精中,能形成饱和溶液的溶液名称是____ 。
(3)实验室要配制40℃ 100g饱和碳酸钠溶液。
①计算:需称取无水Na2CO3的质量略大于____ g 需量取水的体积是__ mL。(计算结果均保留一位小数),若称量时托盘天平指针略向右偏移,接着需进行的操作是____ 。
②将称取的Na2CO3固体和水倒入烧杯中,______ (填操作名称),直至固体完全溶解,再冷却至40℃。
③若所配溶液中碳酸钠的质量分数偏小,可能原因有_____ 。
A 用托盘天平称取时,左边放砝码右边放碳酸钠
B 烧杯用蒸馏水润洗后再配制溶液
C 用量筒取水时仰视读数
D 转移已配好的溶液时,有少量液体溅出
(4)化学兴趣小组为了证明二氧化碳能与氢氧化钠反应,根据以上溶解度数据设计了如下图实验:
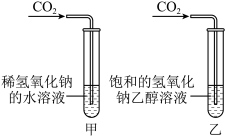
观察到的实验现象是_______ ,乙中反应化学方程是______ 。
| 氢氧化钠 | 碳酸钠 | |||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109g | 129g | 21.8g | 50g |
| 酒精 | 17.3g | 40g | <0.01g | <0.01g |

(1)上述图像表示
(2)40℃时,若将50g NaOH分别投入到100g水和100g酒精中,能形成饱和溶液的溶液名称是
(3)实验室要配制40℃ 100g饱和碳酸钠溶液。
①计算:需称取无水Na2CO3的质量略大于
②将称取的Na2CO3固体和水倒入烧杯中,
③若所配溶液中碳酸钠的质量分数偏小,可能原因有
A 用托盘天平称取时,左边放砝码右边放碳酸钠
B 烧杯用蒸馏水润洗后再配制溶液
C 用量筒取水时仰视读数
D 转移已配好的溶液时,有少量液体溅出
(4)化学兴趣小组为了证明二氧化碳能与氢氧化钠反应,根据以上溶解度数据设计了如下图实验:

观察到的实验现象是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】在化学实验考核中,两位同学用如下两种不同的方法,配制100g溶质质量分数为5%的硝酸钾溶液.
【小明用固体硝酸钾和水配制溶液】
(1)小明用到的玻璃仪器除量筒、胶头滴管、烧杯外,还有__________ ;
(2)小明实验时应进行的步骤是计算、__________ 、量取、溶解、装瓶并贴标签.
【小红用溶质质量分数为20%的硝酸钾溶液加水稀释】
(3)小红实验时应量取水的体积是__________ mL(水的密度可近似看做1g/cm3);
(4)若小红量取水时俯视读数,则所配溶液的溶质质量分数__________ 5%(选填“>”、“<”或“=”).
(5)将接近饱和的硝酸钾溶液变为饱和溶液,下列说法正确的是__________ (填序号).
①溶质质量可能不变
②溶质质量分数一定变大
③溶液质量可能变小
④该饱和溶液还能溶解氯化钠
(6)若用100g20%的氯化钠溶液、10g氯化钠固体和水可配制成5%的氯化钠溶液的质量为_______ g.
【小明用固体硝酸钾和水配制溶液】
(1)小明用到的玻璃仪器除量筒、胶头滴管、烧杯外,还有
(2)小明实验时应进行的步骤是计算、
【小红用溶质质量分数为20%的硝酸钾溶液加水稀释】
(3)小红实验时应量取水的体积是
(4)若小红量取水时俯视读数,则所配溶液的溶质质量分数
(5)将接近饱和的硝酸钾溶液变为饱和溶液,下列说法正确的是
①溶质质量可能不变
②溶质质量分数一定变大
③溶液质量可能变小
④该饱和溶液还能溶解氯化钠
(6)若用100g20%的氯化钠溶液、10g氯化钠固体和水可配制成5%的氯化钠溶液的质量为
您最近一年使用:0次
【推荐3】某化学小组需要用到质量分数为10%的氢氧化钠溶液来做实验,但实验室的氢氧化钠刚好用完。同学们提出用熟石灰与碳酸钠反应制取氢氧化钠,再配成溶液来做实验。
下表是氢氧化钙和氢氧化钠的溶解度数据
请回答问题:
(1)制备氢氧化钠。写出制取氢氧化钠反应的化学方程式______ 。反应后过滤,蒸发结晶得到固体氢氧化钠。小明提出这样制得的氢氧化钠可能含有少量杂质,其理由是______ 。
(2)提纯氢氧化钠。将上述制得的氢氧化钠(含少量氢氧化钙)在60℃时配成饱和溶液,降温、结晶、过滤,对滤渣和滤液成分的分析,正确的是______ (双选)。
A 滤渣中只有氢氧化钠
B 滤渣中主要是氢氧化钠,可能有少量氢氧化钙
C 滤液中一定有氢氧化钙,可能有氢氧化钠
D 滤液中一定有氢氧化钠和氢氧化钙
E 滤液中只有氢氧化钙
(3)配制氢氧化钠溶液。配制50克10%氢氧化钠溶液,需要氢氧化钠固体的质量为______ g,称取时必须将氢氧化钠固体放在______ 里进行称量。
(4)进行实验。完全中和40g上述配得的氢氧化钠溶液,用去了稀硫酸的质量为20克,则稀硫酸的质量分数为______ (精确到0.1%)
下表是氢氧化钙和氢氧化钠的溶解度数据
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100gH2O) | 氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| 氢氧化钠 | 31 | 90 | 111 | 129 | 313 | 336 | |
(1)制备氢氧化钠。写出制取氢氧化钠反应的化学方程式
(2)提纯氢氧化钠。将上述制得的氢氧化钠(含少量氢氧化钙)在60℃时配成饱和溶液,降温、结晶、过滤,对滤渣和滤液成分的分析,正确的是
A 滤渣中只有氢氧化钠
B 滤渣中主要是氢氧化钠,可能有少量氢氧化钙
C 滤液中一定有氢氧化钙,可能有氢氧化钠
D 滤液中一定有氢氧化钠和氢氧化钙
E 滤液中只有氢氧化钙
(3)配制氢氧化钠溶液。配制50克10%氢氧化钠溶液,需要氢氧化钠固体的质量为
(4)进行实验。完全中和40g上述配得的氢氧化钠溶液,用去了稀硫酸的质量为20克,则稀硫酸的质量分数为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D都是初中化学中的常见物质,具有如图所示的转化关系(反应条件、有些反应物或产物已略去):

(1)若A是一种白色难溶于水的钙盐,B、C均为氧化物。则A和D的化学式依次是______ 、______ 。
(2)若A是相对分子质量最小的常见氧化物,D是一种黑色固体。则C的化学式是______ 。
(3)若A是糕点的发酵粉(发酵粉受热分解生成苏打、水和一种气体氧化物),已知过量的C与D溶液反应生成A,写出B→D的化学方程式______ 。

(1)若A是一种白色难溶于水的钙盐,B、C均为氧化物。则A和D的化学式依次是
(2)若A是相对分子质量最小的常见氧化物,D是一种黑色固体。则C的化学式是
(3)若A是糕点的发酵粉(发酵粉受热分解生成苏打、水和一种气体氧化物),已知过量的C与D溶液反应生成A,写出B→D的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】A~G是初中化学常见的物质,B和D能参与光合作用,F可用于改良酸性土壤。 它们之间的关系如图所示(“-”表示相连两物质之间能发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去),每个虚线圈中各反应的基本反应类型相同.
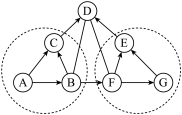
(1)写出物质的化学式:A____ ;
(2)反应F—G的基本反应类型是___ ;
(3)反应D—F的化学方程式是________ 。

(1)写出物质的化学式:A
(2)反应F—G的基本反应类型是
(3)反应D—F的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐3】亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。某研究小组采用如图实验流程用Na2CO3溶液吸收SO2制备Na2SO3。
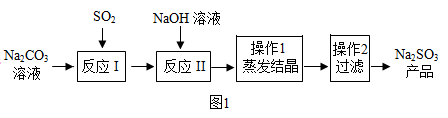
反应I中随着SO2的增加,依次发生如下化学反应:
SO2+H2O+2Na2CO3=Na2SO3+2NaHCO3
SO2+2NaHCO3=Na2SO3+2CO2↑+H2O
SO2+H2O+Na2SO3=2NaHSO3
(1)H2SO3的名称为亚硫酸,则Na2SO3的名称为_____ 。
(2)常用蒸发结晶的方法分离混合溶液得到Na2SO3,由此可知,Na2SO3的溶解度曲线是与题图2中的_____ (填A或B)物质的溶解度曲线相似。

(3)操作2得到的滤液中一定含有的溶质的化学式为_____ 。
(4)查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中,溶液中有关组分的质量分数变化如图2所示。则线1表示_____ (填化学式,下同)的质量分数的变化情况,线2表示_____ 的质量分数的变化情况。
(5)实验时,“反应Ⅱ”中加入NaOH溶液的目的是将反应1中生成的 NaHSO3转化为Na2SO3,则该化学反应方程式为_____ 。
(6)实验后,将Na2SO3样品放置在烧杯中,一段时间后,检测发现样品中出现Na2SO4杂质,且放置时间越长产生的Na2SO4越多,则Na2SO3样品变质为Na2SO4的化学反应方程式为_____ 。

反应I中随着SO2的增加,依次发生如下化学反应:
SO2+H2O+2Na2CO3=Na2SO3+2NaHCO3
SO2+2NaHCO3=Na2SO3+2CO2↑+H2O
SO2+H2O+Na2SO3=2NaHSO3
(1)H2SO3的名称为亚硫酸,则Na2SO3的名称为
(2)常用蒸发结晶的方法分离混合溶液得到Na2SO3,由此可知,Na2SO3的溶解度曲线是与题图2中的

(3)操作2得到的滤液中一定含有的溶质的化学式为
(4)查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中,溶液中有关组分的质量分数变化如图2所示。则线1表示
(5)实验时,“反应Ⅱ”中加入NaOH溶液的目的是将反应1中生成的 NaHSO3转化为Na2SO3,则该化学反应方程式为
(6)实验后,将Na2SO3样品放置在烧杯中,一段时间后,检测发现样品中出现Na2SO4杂质,且放置时间越长产生的Na2SO4越多,则Na2SO3样品变质为Na2SO4的化学反应方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】提纯含少量泥沙的粗盐样品,实验过程和氯化钠的溶解度数据如下:

(1)该实验操作Ⅰ名称是________ ;
(2)蒸发时,一般有如下操作:①放置酒精灯,②放置蒸发皿,③加热并搅拌,④固定铁圈位置,⑤停止加热,用余热蒸干。正确的操作顺序是_______________ ;
(3)经称量,未溶解的粗盐质量为1.2g,得到精盐的质量为2.7g。则粗盐的产率是________ 。(结果保留一位小数)下列因素会导致获得的精盐质量偏小的是________ (填序号)
A蒸发时液滴溅出 B过滤时,滤纸破损
(4)由于粗盐中含有少量 、
、 、
、 等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图:
等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图:
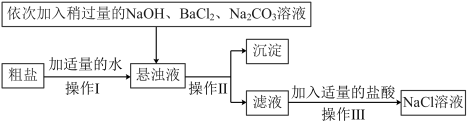
①加入稍过量的 溶液能除去粗盐中的
溶液能除去粗盐中的 ,反应的化学方程式为
,反应的化学方程式为_____________________ 。
②通过操作Ⅱ所得滤液中的溶质有____________________ (用化学式表示)。

(1)该实验操作Ⅰ名称是
(2)蒸发时,一般有如下操作:①放置酒精灯,②放置蒸发皿,③加热并搅拌,④固定铁圈位置,⑤停止加热,用余热蒸干。正确的操作顺序是
(3)经称量,未溶解的粗盐质量为1.2g,得到精盐的质量为2.7g。则粗盐的产率是
A蒸发时液滴溅出 B过滤时,滤纸破损
(4)由于粗盐中含有少量
 、
、 、
、 等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图:
等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图:
①加入稍过量的
 溶液能除去粗盐中的
溶液能除去粗盐中的 ,反应的化学方程式为
,反应的化学方程式为②通过操作Ⅱ所得滤液中的溶质有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】海水晒制得到的粗盐中除 外,还含有
外,还含有 、
、 、
、 、泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
、泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
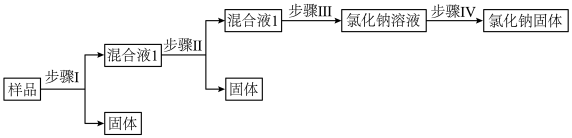
(1)步骤Ⅰ和步骤Ⅱ除加入必要的试剂之外都还涉及相同的实验操作,该操作所需的玻璃仪器是漏斗、烧杯、______ 。
(2)为了除去混合液1中的可溶性杂质 、
、 、
、 ,应按顺序依次加入过量的
,应按顺序依次加入过量的 、
、 、
、 ,分别写出除去杂质
,分别写出除去杂质 、
、 的化学方程式:
的化学方程式:______ 、______ 。
(3)步骤Ⅱ中加入过量 溶液的目的是除去
溶液的目的是除去______ 。
(4)步骤Ⅲ中应加入过量的______ (填药品名称),其目的是______ ,写出有关反应的化学方程式:______ 。
(5)若实验过程中不考虑损耗,最终得到的 固体的质量将
固体的质量将______ (选填“大于”、“小于”或“等于”)原粗盐中 的质量。
的质量。
 外,还含有
外,还含有 、
、 、
、 、泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
、泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
(1)步骤Ⅰ和步骤Ⅱ除加入必要的试剂之外都还涉及相同的实验操作,该操作所需的玻璃仪器是漏斗、烧杯、
(2)为了除去混合液1中的可溶性杂质
 、
、 、
、 ,应按顺序依次加入过量的
,应按顺序依次加入过量的 、
、 、
、 ,分别写出除去杂质
,分别写出除去杂质 、
、 的化学方程式:
的化学方程式:(3)步骤Ⅱ中加入过量
 溶液的目的是除去
溶液的目的是除去(4)步骤Ⅲ中应加入过量的
(5)若实验过程中不考虑损耗,最终得到的
 固体的质量将
固体的质量将 的质量。
的质量。
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】食盐是一种重要的化工原料。请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。

①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和_____________ .
②在蒸发过程中,待__________________________ 时,停止加热,利用余热将滤液蒸干.
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制.流程如下图。
①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是_____________________________ (用化学方程式表示)
②通过操作Ⅲ所得滤液中的溶质有____________________________ (用化学式表示).
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。

①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和
②在蒸发过程中,待
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制.流程如下图。
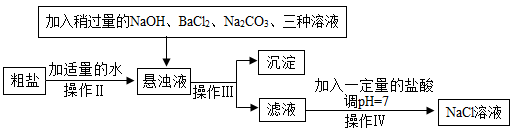
①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是
②通过操作Ⅲ所得滤液中的溶质有
您最近一年使用:0次



