取12g石灰石样品放入盛有105.4g稀盐酸溶液的烧杯中,恰好完全反应。有关实验数据如下表:( 假设石灰石样品中杂质不与稀盐酸反应也不溶于水 , 且不考虑反应过程中水分和 HCl 气体的挥发 )
(1)反应中生成二氧化碳的质量为_______g。
(2)该石灰石样品中碳酸钙的质量分数为_______(结果精确到0.1%)。
(3)反应后所得溶液中溶质质量分数是多少?(请写出计算过程)
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150 g | 12 g | 157.6 g | |
(1)反应中生成二氧化碳的质量为_______g。
(2)该石灰石样品中碳酸钙的质量分数为_______(结果精确到0.1%)。
(3)反应后所得溶液中溶质质量分数是多少?(请写出计算过程)
更新时间:2021-01-08 16:08:32
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】草酸亚铁广泛用于涂料、染料及感光材料的生产,也是合成锂离子电池正极材料磷酸亚铁锂的原料。为研究草酸亚铁晶体(FeC2O4·xH2O)的组成,称取54.0g草酸亚铁晶体在隔绝空气条件下加热,得到剩余固体的质量随温度变化曲线如图所示。

已知:温度t1℃时,草酸亚铁晶体完全脱去结晶水,发生反应:FeC2O4·xH2O FeC2O4+xH2O;温度t2℃时,草酸亚铁完全分解,发生反应: 3FeC2O4
FeC2O4+xH2O;温度t2℃时,草酸亚铁完全分解,发生反应: 3FeC2O4 Fe3O4+4CO↑+2CO2↑
Fe3O4+4CO↑+2CO2↑
(1)温度t1℃时,a点固体物质的成份是___________ (用化学式表示)。
(2)求该草酸亚铁晶体中x的值。(写出详细的计算过程)

已知:温度t1℃时,草酸亚铁晶体完全脱去结晶水,发生反应:FeC2O4·xH2O
 FeC2O4+xH2O;温度t2℃时,草酸亚铁完全分解,发生反应: 3FeC2O4
FeC2O4+xH2O;温度t2℃时,草酸亚铁完全分解,发生反应: 3FeC2O4 Fe3O4+4CO↑+2CO2↑
Fe3O4+4CO↑+2CO2↑(1)温度t1℃时,a点固体物质的成份是
(2)求该草酸亚铁晶体中x的值。(写出详细的计算过程)
您最近一年使用:0次
【推荐2】自然界存在着一种白云石的矿石,其化学式是xCaCO3·y MgCO3。(其中x、y为最小正整数比)。以它为原料,可制取耐火材料等。
(1)称取2.76g白云石,加热到质量不再变化,冷却到室温,再称量固体质量为1.44g。试通过计算写出白云石的化学式________ 。
(2)若再称取2.76g白云石,研碎后与过量炭粉混合,放在特定仪器中隔绝空气强热一段时间后,测得白云石分解率为a(设白云石CaCO3、MgCO3同比分解),生成VL一氧化碳(密度为1.25g/L)。(已知CaO+3C CaC2+CO;2MgO+5C
CaC2+CO;2MgO+5C Mg2C3+2CO)
Mg2C3+2CO)
①试计算V为______ L(用a代数式表示)。
②请在下图中画出V和a的关系图________ 。

(1)称取2.76g白云石,加热到质量不再变化,冷却到室温,再称量固体质量为1.44g。试通过计算写出白云石的化学式
(2)若再称取2.76g白云石,研碎后与过量炭粉混合,放在特定仪器中隔绝空气强热一段时间后,测得白云石分解率为a(设白云石CaCO3、MgCO3同比分解),生成VL一氧化碳(密度为1.25g/L)。(已知CaO+3C
 CaC2+CO;2MgO+5C
CaC2+CO;2MgO+5C Mg2C3+2CO)
Mg2C3+2CO)①试计算V为
②请在下图中画出V和a的关系图

您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】某补钙剂(有效成分为碳酸钙,其他成分不含钙元素)的说明书的部分信息如图所示。为了检验该产品,现将20片该药剂制成的粉末,放入40g稀盐酸中HCl与补钙品有效成分刚好完全反应(其他成分不与盐酸反应),反应后称得剩余物的质量为55.6g。试计算:

(1)生成二氧化碳气体的质量是_____;
(2)该品牌补钙剂每片含的CaCO3质量为_______;(写出计算过程)
(3)通过计算分析。该补钙剂说明书中“含钙量”的数值________(填“符合”、“不符合”)标示,若不符合,应将“含钙量”的数值修改为__________。

(1)生成二氧化碳气体的质量是_____;
(2)该品牌补钙剂每片含的CaCO3质量为_______;(写出计算过程)
(3)通过计算分析。该补钙剂说明书中“含钙量”的数值________(填“符合”、“不符合”)标示,若不符合,应将“含钙量”的数值修改为__________。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
解题方法
【推荐2】实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有100g碳酸钠溶液,将140g氯化钙溶液分四次加入,充分反应,
注:发生反应的化学方程式为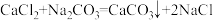
四次测量所得数据如表所示:
(1)恰好完全反应时,生成沉淀的总质量为 g。
(2)第四次测量时,所得溶液中的溶质有 (填化学式)。
(3)计算氯化钙溶液的溶质质量分数(写出计算过程,计算结果保留到0.1%)
注:发生反应的化学方程式为
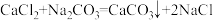
四次测量所得数据如表所示:
| 次数 | 累计加入氯化钙溶液的质量/g | 烧杯中溶液的总质量/g |
| 一 | 40 | 135 |
| 二 | 80 | 170 |
| 三 | 120 | 205 |
| 四 | 140 | 225 |
(1)恰好完全反应时,生成沉淀的总质量为 g。
(2)第四次测量时,所得溶液中的溶质有 (填化学式)。
(3)计算氯化钙溶液的溶质质量分数(写出计算过程,计算结果保留到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】小龙为了探究煅烧了一段时间的石灰石中各成分的质量(其中杂质高温不分解、不溶于水也不与酸反应),进行了如下图所示的实验:请回答下列问题:

(1)写出没有气体生成的化学反应方程式:_____;
(2)列出求解所探究的固体中碳酸钙质量(x)的比例式: _____;
(3)该煅烧后的石灰石中各物质的质量最简比是_____;
(4)最终所得的不饱和溶液中,溶质的质量分数为_____;
(5)若用 36.5%的浓盐酸配制实验所需的稀盐酸需要的仪器有量筒、玻璃棒,其中缺少的仪器有_____。

(1)写出没有气体生成的化学反应方程式:_____;
(2)列出求解所探究的固体中碳酸钙质量(x)的比例式: _____;
(3)该煅烧后的石灰石中各物质的质量最简比是_____;
(4)最终所得的不饱和溶液中,溶质的质量分数为_____;
(5)若用 36.5%的浓盐酸配制实验所需的稀盐酸需要的仪器有量筒、玻璃棒,其中缺少的仪器有_____。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】在含氯化钠杂质的纯碱13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示:

请计算:
(1)100g稀盐酸中氯化氢的质量。
(2)生成二氧化碳的质量。
(3)完全反应后,所得溶液中溶质的质量分数。

请计算:
(1)100g稀盐酸中氯化氢的质量。
(2)生成二氧化碳的质量。
(3)完全反应后,所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】工业用生石灰中常常含有石灰石。为测定某生石灰样品中氧化钙的含量,取61g样品与足量的盐酸反应,生成二氧化碳气体2.2g(假设气体无损失)。求:
(1)61g样品中氧化钙的质量是多少?
(2)该样品中钙元素的质量分数是多少?(精确到0.1%)(Ca-40 O-16 C-12)
(1)61g样品中氧化钙的质量是多少?
(2)该样品中钙元素的质量分数是多少?(精确到0.1%)(Ca-40 O-16 C-12)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】计算:
(1)CO2 和 CO 组成的混合气体,CO2 和 CO 的分子个数比为 1:2,混合气体分子中碳原子和氧原子个数比为______ ;CO2 和 CO 两种物质的质量比为______ ;混合气体中碳元素质量分数为______ 。
(2)乙酸(CH3COOH)和丙酸(CH3CH2COOH)组成的混合物的质量为 18g,经测定, 碳元素的质量为 7.2g,请回答下列问题:乙酸中碳元素的质量分数为______ ;混合物中氧元素的质量为______ 。
(1)CO2 和 CO 组成的混合气体,CO2 和 CO 的分子个数比为 1:2,混合气体分子中碳原子和氧原子个数比为
(2)乙酸(CH3COOH)和丙酸(CH3CH2COOH)组成的混合物的质量为 18g,经测定, 碳元素的质量为 7.2g,请回答下列问题:乙酸中碳元素的质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】由于高铁列车车厢是密闭的空间,因此需要提供清洁的空气和保持车厢的卫生。高铁酸钠(Na2FeOx)是高铁上常用的一种“绿色、环保、高效”的消毒剂。
(1)已知高铁酸钠的相对分子质量为 166,则铁元素的化合价为______ 。
(2)______ 克的高铁酸钠中含有 4.6 克的钠元素。
(3)C2H4和 C2H6O 的混合物中,碳元素的质量分数为 60%,则混合物中氧元素的质量分数为______ 。(保留三位有效数字)
(1)已知高铁酸钠的相对分子质量为 166,则铁元素的化合价为
(2)
(3)C2H4和 C2H6O 的混合物中,碳元素的质量分数为 60%,则混合物中氧元素的质量分数为
您最近一年使用:0次




