请根据如图所示的实验过程和提供的数据计算(铜与硫酸不发生反应)
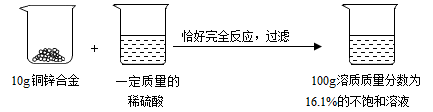
(1)生成氢气___________g;
(2)该铜锌合金中锌元素的质量分数是多少?

(1)生成氢气___________g;
(2)该铜锌合金中锌元素的质量分数是多少?
更新时间:2021-01-12 21:17:23
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】向50g石灰石样品中(其中有效成分为CaCO3)中不断地加入稀盐酸,其变化图象如图所示。请回答以下问题:
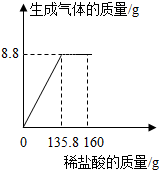
(1)产生二氧化碳的质量为_____g;
(2)求样品中CaCO3的质量分数为?

(1)产生二氧化碳的质量为_____g;
(2)求样品中CaCO3的质量分数为?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】在“新冠肺炎”防疫期间,大家都知道“84消毒液”与“洁厕灵”混合会产生有毒气体,因此不能混用。“洁厕灵”的有效成分为盐酸,有腐蚀性,单独使用也要小心,不能接触皮肤。为了对某品牌洁厕灵的有效成分的含量进行测定,小吴向一锥形瓶中加入100g该品牌的洁厕灵,再加入足量的溶质质量分数为8%的NaHCO3溶液120g,反应结束后,溶液的总质量是215.6g。试计算下列问题:
(1)产生的二氧化碳质量为______ 克。
(2)该品牌洁厕灵中HCl的质量分数是多少?(写出计算过程。)
(1)产生的二氧化碳质量为
(2)该品牌洁厕灵中HCl的质量分数是多少?(写出计算过程。)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】2021年1月26日,中国广电与中国移动签署“5G战略”合作协议,正式启动700 MHz 5G网络共建共享。5G通讯需要大量光纤连接各种基站,在光纤表面涂布Cu-Al合金层的金属涂层光纤是其中的一种。为测定Cu-Al合金层中铝的质量分数,甲、乙、丙同学分别称取一定量的样品于烧杯中,并滴加稀硫酸,充分反应后,测得实验数据如下表:
试分析并计算:
(1). 合金样品粉末与稀硫酸恰好完全反应的是______(填“甲”、“乙”或“丙”)的实验。
(2). 该合金样品中铝的质量分数。
| 实验 | 甲 | 乙 | 丙 |
| 加入合金样品粉末的质量/g | 20 | 20 | 40 |
| 加入稀硫酸的质量/g | 200 | 100 | 100 |
| 烧杯中剩余物的质量/g | 218 | 118 | 138 |
试分析并计算:
(1). 合金样品粉末与稀硫酸恰好完全反应的是______(填“甲”、“乙”或“丙”)的实验。
(2). 该合金样品中铝的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在一烧杯中盛有100gBaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入的Na2CO3溶液的质量关系图象如图所示。
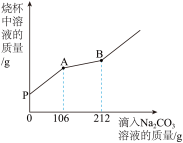
(1)在实验过程中,可以先后看到的明显实验现象是 。
(2)最终所得溶液的pH 7(填大于、小于或等于)。
(3)求原溶液中BaCl2的质量分数为 。

(1)在实验过程中,可以先后看到的明显实验现象是 。
(2)最终所得溶液的pH 7(填大于、小于或等于)。
(3)求原溶液中BaCl2的质量分数为 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】今年全国人大和政协会议使用了一种含碳酸钙的“石头纸”。为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表(假设纸张中其它成分既不溶于水,也不与盐酸反应):
(1)表中X的值为_______ ;
(2)求样品中碳酸钙的质量分数。(写出计算过程)
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
| 充分反应后生成气体的质量/g | 0.88 | 1.76 | X | 3.52 | 3.52 |
(2)求样品中碳酸钙的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】某厂为了测定一批Cu-Mg样品中铜的质量分数,取用10g样品,把200g稀盐酸分4次加入样品中(样品中除Cu-Mg外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
(1)一开始金属样品都是过量的,直到加入第______ 次,由______ 知道酸已经过量,从而可以得到铜的质量分数为______ 。
(2)加入第三次稀盐酸后,金属与酸的反应情况是______ (填“酸过量”“金属过量”或“正好反应”)。你判断的理由是______ 。
(3)计算该稀盐酸的溶质质量分数,必须使用酸完全反应时的数据。依据题中数据,算得该稀盐酸的溶质质量分数为______ (计算结果准确度0.1%)。
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 稀盐酸的用量 | 50g | 50g | 50g | 50g |
| 剩余固体的质量 | 8.8g | 7.6g | 6.4g | 6.4g |
(1)一开始金属样品都是过量的,直到加入第
(2)加入第三次稀盐酸后,金属与酸的反应情况是
(3)计算该稀盐酸的溶质质量分数,必须使用酸完全反应时的数据。依据题中数据,算得该稀盐酸的溶质质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在一烧杯中盛有22.3Na2CO3和NaCl组成的固体混合物,加水溶解配成溶液。向其中逐渐滴加10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答问题:
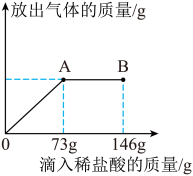
(1)当滴加稀盐酸至B点时,烧杯中溶液里的溶质是_____(写化学式),溶液PH___7(填“ 、
、 或
或 ”)。
”)。
(2)当滴加了73g稀盐酸时,放出气体的总质量为__________ 。
。
(3)当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。

(1)当滴加稀盐酸至B点时,烧杯中溶液里的溶质是_____(写化学式),溶液PH___7(填“
 、
、 或
或 ”)。
”)。(2)当滴加了73g稀盐酸时,放出气体的总质量为__________
 。
。(3)当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】13g锌与100g的稀硫酸恰好完全反应,试计算:
(1)生成氢气质量。
(2)所得溶液中溶质的质量分数。
(1)生成氢气质量。
(2)所得溶液中溶质的质量分数。
您最近一年使用:0次



