相同质量的镁、铝、锌、铁,分别和足量的盐酸反应,生成氢气质量关系是( )
| A.镁最多,铁最少 | B.镁最多,锌最少 |
| C.铝最多,铁最少 | D.铝最多,锌最少 |
更新时间:2021-01-20 19:21:19
|
【知识点】 酸过量--金属性质的计算解读
相似题推荐
选择题-单选题
|
较易
(0.85)
【推荐1】将颗粒大小相同的等质量X、Y、Z三种金属放入等浓度的稀盐酸中,产生氢气质量如图所示,下列说法正确的是
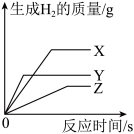

| A.金属X最活泼 |
| B.金属Y的相对原子质量一定大于X |
| C.若金属Z是Fe,则金属X一定不是Al |
| D.金属Z反应掉的稀盐酸一定最少 |
您最近一年使用:0次
选择题-单选题
|
较易
(0.85)
解题方法
【推荐2】等质量的Zn、Mg、Al分别与足量的稀盐酸反应,消耗酸的质量大小关系是( )
| A.Zn=Mg=Al | B.Zn>Mg>Al | C.Al>Zn >Mg | D.Al>Mg> Zn |
您最近一年使用:0次
选择题-单选题
|
较易
(0.85)
【推荐3】等质量的甲、乙两种金属,分别与足量等浓度的盐酸反应(已知甲、乙在生成物中化合价均为+2),生成氢气的质量和反应时间的关系如图所示,下列叙述正确的是
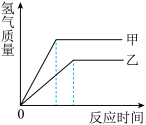

| A.甲、乙两种金属中较活泼的是乙 | B.产生氢气的速率:甲<乙 |
| C.生成氢气的质量:甲<乙 | D.相对原子质量较大的是乙 |
您最近一年使用:0次



