为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,阳阳同学取一定质量的黄铜样品放入烧杯中,再取40g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
请你计算:
(1)所用稀盐酸中溶质的质量分数。
(2)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量。
(3)黄铜样品中铜的质量分数。
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 9.10 | 8.45 | 7.80 | 7.80 |
请你计算:
(1)所用稀盐酸中溶质的质量分数。
(2)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量。
(3)黄铜样品中铜的质量分数。
20-21九年级下·全国·课时练习 查看更多[4]
(已下线)6.2 溶液组成的表示-2020-2021学年九年级化学下册课时同步练(沪教版)2021年广东省清远市佛冈县汤塘中学中考六模化学试题2022年广东省肇庆市封开县中考二模化学试题第九单元溶液课题3溶液的浓度第二课时溶质的质量分数的综合计算2023步步升
更新时间:2021-01-17 15:13:26
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】兴趣小组同学为测定某赤铁矿样品中氧化铁的含量,取10g该样品,将50g稀硫酸分五次加入样品中,使之充分反应(样品中杂质不溶于水,也不与稀硫酸反应)。实验数据记录如下表:
(1)该样品中氧化铁的质量分数为_______ 。
(2)所用稀硫酸的溶质质量分数。
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 加入稀硫酸的质量/g | 10 | l0 | 10 | 10 | 10 |
| 剩余固体质量/g | 8.4 | 6.8 | 5.2 | 3.6 | 3.6 |
(1)该样品中氧化铁的质量分数为
(2)所用稀硫酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组的同学为测定某石灰石样品中碳酸钙的含量,取50g石灰石样品,与足量稀盐酸反应,收集到二氧化碳13.2g,计算该样品中碳酸钙的含量。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐3】铝碳酸镁咀嚼片(主要成分是AlMg(OH)3CO3)可治疗胃酸过多症,反应原理可用化学方程式表示为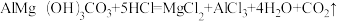 。某化学兴趣小组使用下图所示装置,对该咀嚼片中的铝碳酸镁含量进行测定。先取足量稀盐酸于烧杯中,再向其中加入20片铝碳酸镁咀嚼片,开始计时,并将电子天平的读数记录在下表中、已知AlMg(OH)3CO3的相对分子质量为162。请计算:
。某化学兴趣小组使用下图所示装置,对该咀嚼片中的铝碳酸镁含量进行测定。先取足量稀盐酸于烧杯中,再向其中加入20片铝碳酸镁咀嚼片,开始计时,并将电子天平的读数记录在下表中、已知AlMg(OH)3CO3的相对分子质量为162。请计算:

(1)生成二氧化碳______ g。
(2)每片该咀嚼片中铝碳酸镁的含量为多少(计算结果保留到0.1g)?
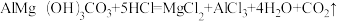 。某化学兴趣小组使用下图所示装置,对该咀嚼片中的铝碳酸镁含量进行测定。先取足量稀盐酸于烧杯中,再向其中加入20片铝碳酸镁咀嚼片,开始计时,并将电子天平的读数记录在下表中、已知AlMg(OH)3CO3的相对分子质量为162。请计算:
。某化学兴趣小组使用下图所示装置,对该咀嚼片中的铝碳酸镁含量进行测定。先取足量稀盐酸于烧杯中,再向其中加入20片铝碳酸镁咀嚼片,开始计时,并将电子天平的读数记录在下表中、已知AlMg(OH)3CO3的相对分子质量为162。请计算:
| 时间(s) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 读数(g) | 198.4 | 197.8 | 197.4 | 196.0 | 195.8 | 195.7 | 195.7 | 195.7 |
(2)每片该咀嚼片中铝碳酸镁的含量为多少(计算结果保留到0.1g)?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】将适量的铁粉放入由CuSO4和稀H2SO4组成混合溶液中,铁粉恰好完全溶解,过滤得沉淀物,经洗涤干燥,称得沉淀物的质量与所加入的铁粉的质量相等,求混合溶液中所含CuSO4与H2SO4的质量比是多少?(要求写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】欲测定某锌﹣铜合金中铜的质量分数,进行如下实验:取合金样品10克放入烧杯中,将60克稀硫酸分三次加入,充分反应后(铜和稀硫酸不反应且难溶于水),测得生成气体的质量如下:
请回答下列问题并计算:
(1)第二次实验时生成气体质量m=______ 克;样品中铜的质量为______ 克(只写答案);
(2)求所用稀硫酸的溶质质量分数。
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 20 | 20 | 20 |
| 生成气体质量/g | 0.08 | m | 0.04 |
(1)第二次实验时生成气体质量m=
(2)求所用稀硫酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】现配制50g溶质质量分数为15%的氯化钠溶液。
(1)配制50g溶质质量分数为15%的氯化钠溶液所需氯化钠的质量为______ g;
(2)操作步骤如图所示:
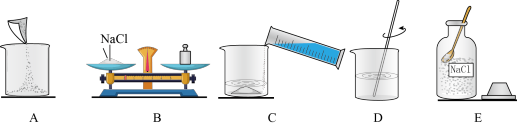
上述操作步骤的正确顺序是______ (填字母序号);
(3)若改用溶质质量分数为30%的氯化钠溶液进行稀释的方法配制该溶液,则需要30%的氯化钠溶液______ g,并加入______ g的水,请写出具体的计算步骤。
(1)配制50g溶质质量分数为15%的氯化钠溶液所需氯化钠的质量为
(2)操作步骤如图所示:

上述操作步骤的正确顺序是
(3)若改用溶质质量分数为30%的氯化钠溶液进行稀释的方法配制该溶液,则需要30%的氯化钠溶液
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】
(1)要配制5%的过氧化氢溶液240 g,需要30%的过氧化氢溶液的质量是多少?(写出解题过程)__________
(2)用配制的5%的过氧化氢溶液136g,可制得氧气的质量是多少?(写出解题过程)__________
(1)要配制5%的过氧化氢溶液240 g,需要30%的过氧化氢溶液的质量是多少?(写出解题过程)
(2)用配制的5%的过氧化氢溶液136g,可制得氧气的质量是多少?(写出解题过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某个班级做完“二氧化碳的制取和性质”实验后,废液桶中有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质)。为避免污染环境并回收利用废液,化学兴趣小组取废液桶上层清液共11.88g作为样品,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液pH与加入的碳酸钠溶液的质量关系如图所示:
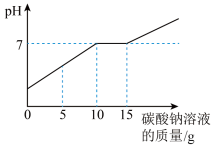
(1)该实验过程观察到的主要现象是______________ 。
(2)计算样品废液中氯化钙的溶质质量分数?

(1)该实验过程观察到的主要现象是
(2)计算样品废液中氯化钙的溶质质量分数?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】硝酸银可用于制造电影胶片、X光胶片等感光材料。兴趣小组为测定某照相馆废液中硝酸银的含量,取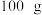 废液样品,将稀盐酸逐滴加入
废液样品,将稀盐酸逐滴加入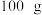 废液样品中,产生沉淀的质量与反应时间的关系如图所示。
废液样品中,产生沉淀的质量与反应时间的关系如图所示。________ g。
(2)硝酸银属于________ (选填“酸”“碱”“盐”或“氧化物”),其中氮元素的化合价为________ 。
(3)计算废液中硝酸银的质量分数。(写出计算过程)
(4)硝酸银见光易分解,实验室保存硝酸银时,应将其保存在________ (选填“无色”或“棕色”)试剂瓶中。
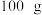 废液样品,将稀盐酸逐滴加入
废液样品,将稀盐酸逐滴加入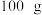 废液样品中,产生沉淀的质量与反应时间的关系如图所示。
废液样品中,产生沉淀的质量与反应时间的关系如图所示。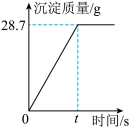
(2)硝酸银属于
(3)计算废液中硝酸银的质量分数。(写出计算过程)
(4)硝酸银见光易分解,实验室保存硝酸银时,应将其保存在
您最近一年使用:0次



