我市东临渤海,有着丰富的海洋资源。请思考下列问题:
(1)下图是利用海水提取粗盐的过程:
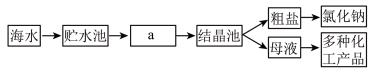
①图中a是___________ 池。(填“蒸发”或“冷却”)
②根据海水晒盐的原理,下列说法正确的是______ 。
A海水进入贮水池,海水的成分基本不变 B在a中,海水中的氯化钠的质量逐渐增加
C在a中,海水中的水的质量逐渐减少 D母液是氯化钠的不饱和溶液
③农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将300g30%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为___________ g。
(2)如图是硝酸钾和氯化钠的溶解度曲线。
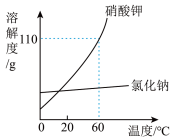
①两种物质中,溶解度受温度影响较小的是___________ (填化学式)。
②60℃时,硝酸钾饱和溶液中溶有少量的氯化钠,提纯硝酸钾应采用的方法是___________ 。
③20℃时,将不饱和氯化钠溶液,转化成该温度下的饱和溶液的一种方法是___________ ;变化过程中,溶质的质量分数___________ (选填“增大”、“减小”或“不变”)。
(3)从海水中制备金属镁的流程如下所示:
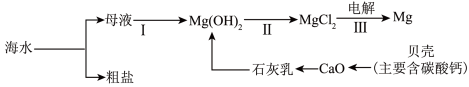
回答下列问题:
①步骤Ⅱ中所加试剂是___________ ,发生反应的方程式是___________ 。
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列物质的先后顺序为___________ (填字母序号)。
a适量的盐酸 b稍过量的Na2CO3溶液 c稍过量的Ba(OH)2溶液
③步骤Ⅲ发生反应的化学反应基本类型是___________ 。
(1)下图是利用海水提取粗盐的过程:

①图中a是
②根据海水晒盐的原理,下列说法正确的是
A海水进入贮水池,海水的成分基本不变 B在a中,海水中的氯化钠的质量逐渐增加
C在a中,海水中的水的质量逐渐减少 D母液是氯化钠的不饱和溶液
③农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将300g30%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为
(2)如图是硝酸钾和氯化钠的溶解度曲线。

①两种物质中,溶解度受温度影响较小的是
②60℃时,硝酸钾饱和溶液中溶有少量的氯化钠,提纯硝酸钾应采用的方法是
③20℃时,将不饱和氯化钠溶液,转化成该温度下的饱和溶液的一种方法是
(3)从海水中制备金属镁的流程如下所示:

回答下列问题:
①步骤Ⅱ中所加试剂是
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列物质的先后顺序为
a适量的盐酸 b稍过量的Na2CO3溶液 c稍过量的Ba(OH)2溶液
③步骤Ⅲ发生反应的化学反应基本类型是
更新时间:2021-01-31 08:24:40
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙、丙三种固体物质的溶解度曲线如图所示,试回答下列问题

(1)甲、乙、丙三种固体物质的溶解度随温度升高而增大且影响较大的是________ 。
(2)欲将t1℃时乙的不饱和溶液转化为该温度下的饱和溶液,可采取的一种方法是________ 。
(3)将等质量的甲、乙两物质的饱和溶液从t2℃降温至t1℃时,析出晶体较多的是________ 。
(4)t2℃时,将40克甲物质放入50克水中,充分溶解后所得溶液的质量是______ 克。
(5)氧气的溶解度随温度变化的规律与图中的______ 相似。

(1)甲、乙、丙三种固体物质的溶解度随温度升高而增大且影响较大的是
(2)欲将t1℃时乙的不饱和溶液转化为该温度下的饱和溶液,可采取的一种方法是
(3)将等质量的甲、乙两物质的饱和溶液从t2℃降温至t1℃时,析出晶体较多的是
(4)t2℃时,将40克甲物质放入50克水中,充分溶解后所得溶液的质量是
(5)氧气的溶解度随温度变化的规律与图中的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图1是甲、乙、丙三种物质的溶解度曲线。


(1)t2°C时,将40g乙物质放入50g水中,充分溶解后,所得溶液中溶质与溶剂的质量比为______ (填最简整数比)。
(2)欲从含有少量乙的甲的饱和溶液中提纯甲,可采用______ (填“蒸发”或“降温”)结晶的方法。
(3)t2°C时,甲、乙、丙三种物质的等质量饱和溶液中,所含溶剂质量最多的是______ 。
(4)t1°C时,取等质量的甲、丙饱和溶液分别置于a、b两支试管中,如图2所示。向大烧杯的水中加入一定质量的氢氧化钠固体溶解后,甲、丙溶液中溶质质量的大小关系是甲______ 丙(填“>”、“<”或“=”)。


(1)t2°C时,将40g乙物质放入50g水中,充分溶解后,所得溶液中溶质与溶剂的质量比为
(2)欲从含有少量乙的甲的饱和溶液中提纯甲,可采用
(3)t2°C时,甲、乙、丙三种物质的等质量饱和溶液中,所含溶剂质量最多的是
(4)t1°C时,取等质量的甲、丙饱和溶液分别置于a、b两支试管中,如图2所示。向大烧杯的水中加入一定质量的氢氧化钠固体溶解后,甲、丙溶液中溶质质量的大小关系是甲
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】魏晋左思《三都赋》中有云:“煮海为盐,采山铸钱”.海水煮盐得到的粗盐中除含泥沙等不溶性杂质外,还含有少量的可溶性杂质(如 ),工业上以粗盐为原料制取精盐的生产流程如图所示.
),工业上以粗盐为原料制取精盐的生产流程如图所示.

请回答下列问题:
(1)滤液C中含有的金属离子有哪些?(写离子符号)
(2)写出该过程中有气体生成的化学方程式.
(3)若加入的X溶液与Y溶液顺序颠倒,精盐中会含有什么杂质?
 ),工业上以粗盐为原料制取精盐的生产流程如图所示.
),工业上以粗盐为原料制取精盐的生产流程如图所示.
请回答下列问题:
(1)滤液C中含有的金属离子有哪些?(写离子符号)
(2)写出该过程中有气体生成的化学方程式.
(3)若加入的X溶液与Y溶液顺序颠倒,精盐中会含有什么杂质?
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】BaCl2广泛应用于化工领域。下图为工业上用重晶石(主要成分为BaSO4)制备BaCl2晶体的主要流程(已知该重晶石样品与无烟煤所含杂质难溶于水,不与酸反应)。

(1)重晶石与无烟煤混合后进行粉碎,其目的是_______ 。
(2)反应①为BaSO4+4C BaS+4A↑,则气体A为
BaS+4A↑,则气体A为_______ (填化学式)。
(3)反应②的化学方程式为_______ ,该反应类型为______ (填基本反应类型)。
(4)操作Ⅰ的名称为_____ ,蒸发浓缩的过程除了蒸发了部分水,还去除的物质是_____ (填化学式)。实验室进行蒸发实验操作时,需使用玻璃棒,其作用是_______ 。
(4)溶液B_______ (填“是”或“不是”)饱和溶液。

(1)重晶石与无烟煤混合后进行粉碎,其目的是
(2)反应①为BaSO4+4C
 BaS+4A↑,则气体A为
BaS+4A↑,则气体A为(3)反应②的化学方程式为
(4)操作Ⅰ的名称为
(4)溶液B
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】飞行器要飞得高、快、远,就必须靠轻、强、精的材料。
(1)稀土镁合金是最轻的金属结构材料。下列金属矿石中可用于冶炼镁的是______(填标号)。
(2)硬铝是制造飞机和宇宙飞船的常用材料。与纯铝相比,硬铝的硬度更______ (填“大”或“小”)。生活中常用铝粉作涂料保护铁制品,除此之外,防止铁制品锈蚀的方法还有______ (任写一条)。
(3)钛镍合金具有形状记忆功能,被广泛用于做人造卫星和宇宙飞船的天线。钛镍合金能被拉成丝是因为其具有______ 性。钛(Ti)在常温下能与氧气反应生成二氧化钛,该反应的化学方程式为______ 。
(4)合金M由Cu、Ag、Al、Mg中的两种或几种组成。某同学通过如下流程对该合金的成分进行探究。
已知:NaOH溶液能与Al(OH)3反应生成可溶性盐,但不能与Mg(OH)2反应。

根据回答下列问题:
①根据实验探究流程,可判断合金M中一定有______ 。
②若固体甲的质量为m1,固体乙的质量为m2,当m2的范围为______ (用含m1的式子表示),可说明合金M中一定有Ag。
(1)稀土镁合金是最轻的金属结构材料。下列金属矿石中可用于冶炼镁的是______(填标号)。
| A.铝土矿(主要成分是Al2O3) | B.菱镁矿(主要成分是MgCO3) |
| C.赤铁矿(主要成分是Fe2O3) | D.钛铁矿(主要成分是FeTiO3) |
(3)钛镍合金具有形状记忆功能,被广泛用于做人造卫星和宇宙飞船的天线。钛镍合金能被拉成丝是因为其具有
(4)合金M由Cu、Ag、Al、Mg中的两种或几种组成。某同学通过如下流程对该合金的成分进行探究。
已知:NaOH溶液能与Al(OH)3反应生成可溶性盐,但不能与Mg(OH)2反应。

根据回答下列问题:
①根据实验探究流程,可判断合金M中一定有
②若固体甲的质量为m1,固体乙的质量为m2,当m2的范围为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐1】我国制碱先驱侯德榜为纯碱和氮肥工业技术的发展做出了杰出贡献,某企业把海水的综合开发和利用与侯氏制碱法结合,实现资源利用最大化,请根据图示完成下列问题。_____ ;请写出该反应的化学方程式_____ 。
(2)已知在溶液中温度高于35℃,NH4HCO3会有分解。吸氨碳化塔内发生的反应:Ⅰ:NH3+H2O+CO2═NH4HCO3;Ⅱ:NH4HCO3+NaCl═NaHCO3↓+NH4Cl。
请结合如图分析反应Ⅱ能进行的原因_____ 。实际生产时,吸氨碳化塔内温度通常控制在不低于30℃,不高于35℃,理由是_____ 。


(2)已知在溶液中温度高于35℃,NH4HCO3会有分解。吸氨碳化塔内发生的反应:Ⅰ:NH3+H2O+CO2═NH4HCO3;Ⅱ:NH4HCO3+NaCl═NaHCO3↓+NH4Cl。
请结合如图分析反应Ⅱ能进行的原因

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海洋是一个巨大的资源宝库。海水资源综合利用的部分途径如下图:

已知:粗盐中的杂质有泥沙、MgCl2、CaCl2,流程中部分操作及试剂已省略。
(1)“操作I”中玻璃棒的作用是_______ 。
(2)滤渣中除泥沙外还有_______ (填化学式)。
(3)反应②的化学反应方程式为________ 。
(4)海水中本身就有氯化镁,请分析反应①、②转化过程的目的_________ 。

已知:粗盐中的杂质有泥沙、MgCl2、CaCl2,流程中部分操作及试剂已省略。
(1)“操作I”中玻璃棒的作用是
(2)滤渣中除泥沙外还有
(3)反应②的化学反应方程式为
(4)海水中本身就有氯化镁,请分析反应①、②转化过程的目的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】2021年6月8日是第13个“世界海洋日”。烟台有漫长的海岸线,蕴藏着丰富的海洋资源。某兴趣小组设计的综合利用海水的部分流程图如图。据如图回答:

(1)海水制镁:步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式为___________ 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是___________ 。
(2)海水晒盐:
①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是___________ (填字母序号)。
A.在蒸发池中水蒸发所需能量主要为太阳能和风能
B.在结晶池中主要通过降温结晶使氯化钠析出
C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过___________ 、过滤、蒸发结晶等操作。蒸发结晶操作中要用到玻璃棒,其作用是___________ 。通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是___________ 。
(3)海水制碱:步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质分别是___________ (写化学式)。步骤⑨中发生反应的化学方程式是___________ 。
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是___________ 。
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是___________ 。

(1)海水制镁:步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式为
(2)海水晒盐:
①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是
A.在蒸发池中水蒸发所需能量主要为太阳能和风能
B.在结晶池中主要通过降温结晶使氯化钠析出
C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过
(3)海水制碱:步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质分别是
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】联合国第63届大会的主题是“化学—人类的生活,人类的未来”,生活中“衣”,“食”、“住”、“行”等与化学密切相关。
(1)下列服装主要用有机合成材料制成的是_______ (填标号)。
A 羊毛衫 B 涤纶连衣裙 C 腈纶运动衣 D 纯棉T恤
(2)①豆腐是人们喜爱的食品,其主要成分如表所示
从上表中可知,此豆腐中含有_______ 类营养素。
②食品安全日益受到人们关注。下列食品因有毒而不能食用的是_______ (填序号)。
A 用含发酵粉(含碳酸氢钠和有机酸等)制作发面食品 B 霉变的大米 C 用亚硝酸钠(NaNO2)代替食盐烹调的食品 D 食盐腌制的咸鸭蛋
(3)氯化钠是人类不可缺少的调味品,也是重要的化工原料,由于粗盐中含有少量 MgC12、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。


①操作Ⅲ所用的玻璃仪器有:烧杯、玻璃棒和_______ 。
②在蒸发过程中,待_______ 时,停止加热,利用余热将滤液蒸干。
③加入稍过量的Na2CO3溶液除了能除去粗盐中的 CaCl2外,它还可以除去_______ 。
④通过操作Ⅲ所得滤液中的溶质有_______ (用化学式表示)。
⑤某同学配制100g质量分数为8.5%的氯化钠溶液,按要求回答问题:
【计算】需要氯化钠固体的质量为________ g;
【称量】用托盘天平称量氯化钠固体时,氯化钠固体应放在天平的_______ 盘(填“左”或“右”)。
(1)下列服装主要用有机合成材料制成的是
A 羊毛衫 B 涤纶连衣裙 C 腈纶运动衣 D 纯棉T恤
(2)①豆腐是人们喜爱的食品,其主要成分如表所示
| 项目 | 水 | 蛋白质 | 油脂 | 糖类 | 维生素B1 | 维生素B2 | 钙 | 铁 |
| 每100克 | 89.30 g | 4.70 g | 1.30g | 2.80 g | 0.06mg | 0.03mg | 0.24 g | 1.40g |
从上表中可知,此豆腐中含有
②食品安全日益受到人们关注。下列食品因有毒而不能食用的是
A 用含发酵粉(含碳酸氢钠和有机酸等)制作发面食品 B 霉变的大米 C 用亚硝酸钠(NaNO2)代替食盐烹调的食品 D 食盐腌制的咸鸭蛋
(3)氯化钠是人类不可缺少的调味品,也是重要的化工原料,由于粗盐中含有少量 MgC12、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。


①操作Ⅲ所用的玻璃仪器有:烧杯、玻璃棒和
②在蒸发过程中,待
③加入稍过量的Na2CO3溶液除了能除去粗盐中的 CaCl2外,它还可以除去
④通过操作Ⅲ所得滤液中的溶质有
⑤某同学配制100g质量分数为8.5%的氯化钠溶液,按要求回答问题:
【计算】需要氯化钠固体的质量为
【称量】用托盘天平称量氯化钠固体时,氯化钠固体应放在天平的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海水中蕴藏着丰富的资源,含有的盐类物质总量有5×1016吨(如氯化钠、氯化镁、氯化钙、氯化钾等)。某工厂对海水综合利用的主要流程如下。

(1)海水晒盐的过程实际上是_______ (填结晶的一种类型)的过程。卤水一定是______ (填名称)的饱和溶液。
(2)试剂A与固体A发生反应的化学方程式为________ 。
(3)石灰乳的主要成分是_______ (填化学式)。请写出该物质的一种重要用途________ 。
(4)由粗盐经过初步提纯(除去难溶性杂质)可得到精盐。实验的主要步骤有:①溶解;②_____ ;③蒸发。在溶解过程中用到的玻璃仪器有_______ 、玻璃棒。溶解时用玻璃棒搅拌的目的是_____ ,如果该操作不够准确,会导致得到的精盐质量_____ (填“偏大”、“偏小”、“无影响”)。最终得到的精盐属于_______ (填“混合物”、“纯净物”)。
(5)溶液A中的金属阳离子符号是________ 。

(1)海水晒盐的过程实际上是
(2)试剂A与固体A发生反应的化学方程式为
(3)石灰乳的主要成分是
(4)由粗盐经过初步提纯(除去难溶性杂质)可得到精盐。实验的主要步骤有:①溶解;②
(5)溶液A中的金属阳离子符号是
您最近一年使用:0次





