某化学兴趣小组的同学想从含有Al2(SO4)3、CuSO4的废液中回收金属铜,设计流程如图:
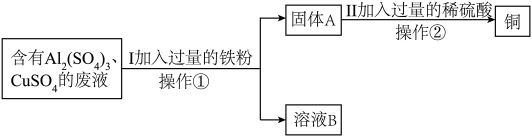
(1)操作①的名称为_______ 。
(2)Ⅰ中有关反应的化学方程式为_______ 。通过该步实验及现象得出三种金属活动性由强到弱的顺序是_______ (用化学符号表示)。
(3)固体A的成分是_______ (填化学式)。
(4)Ⅱ中加入过量的稀硫酸的目的是_______ 。

(1)操作①的名称为
(2)Ⅰ中有关反应的化学方程式为
(3)固体A的成分是
(4)Ⅱ中加入过量的稀硫酸的目的是
更新时间:2021-01-29 15:26:20
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】实验室有一包混有铁粉的铜粉,请你用以下两种方法除去铜粉中的铁粉(简述操作过程)。
(1)物理方法:___________________________ 。
(2)化学方法:____________________________ 。
(1)物理方法:
(2)化学方法:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组为探究Mg、Fe、Cu、Ag四种金属的活动性,进行如图所示实验。
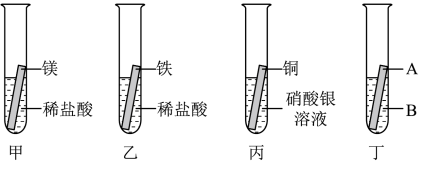
(1)丙试管中反应的化学方程式为______ 。
(2)最终得出四种金属活动性:Mg>Fe>Cu>Ag,若实验时需要用到甲、乙、丙、丁四支试管,则丁试管中的试剂A、B分别为______ 。若仅需用到其中的三支试管即可证明这四种金属的活动性,则丁试管中的试剂A、B分别为______ 。

(1)丙试管中反应的化学方程式为
(2)最终得出四种金属活动性:Mg>Fe>Cu>Ag,若实验时需要用到甲、乙、丙、丁四支试管,则丁试管中的试剂A、B分别为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】我国在商朝已制造出青铜器,春秋时期开始炼铁,而铝的利用始于100多年前。
(1)青铜是铜和锡的合金,青铜属于______ (填“混合物”或“纯净物”)。
(2)铁是应用最广泛的金属,工业上常以赤铁矿和一氧化碳为原料炼铁,该反应的化学方程式为______ ,发生还原反应的是______ 。
(3)为了证明验证铜、铁、铝的金属活动性顺序,小张设计了以下两个实验。
实验①在硫酸铝溶液中插入铁丝。
实验②______ (用化学方程式表示)。
(4)某实验室废液中含有硫酸亚铁和硫酸铜,若向其中加入一定量的铝,充分反应后过滤,向滤渣中加入盐酸,有气泡产生。则滤渣中一定含有的物质是______
(1)青铜是铜和锡的合金,青铜属于
(2)铁是应用最广泛的金属,工业上常以赤铁矿和一氧化碳为原料炼铁,该反应的化学方程式为
(3)为了证明验证铜、铁、铝的金属活动性顺序,小张设计了以下两个实验。
实验①在硫酸铝溶液中插入铁丝。
实验②
(4)某实验室废液中含有硫酸亚铁和硫酸铜,若向其中加入一定量的铝,充分反应后过滤,向滤渣中加入盐酸,有气泡产生。则滤渣中一定含有的物质是
您最近一年使用:0次
【推荐1】金属是大自然赐予人类的宝物,是现代文明不可缺少的物质基础。
(一)人类冶炼和使用金属铝的时间较晚。可能是因为______ (填字母)。
a.地壳中铝元素含量少 b.冶炼铝的技术要求高
(二)银器在使用过程中,因为发生化学反应: ,产生的Ag2S使银器渐失去光泽。已知银的化合价为+1价,则Ag2S中S的化合价为
,产生的Ag2S使银器渐失去光泽。已知银的化合价为+1价,则Ag2S中S的化合价为______ 。
(三)A是目前世界年产量最高的金属,根据下图回答下列问题:
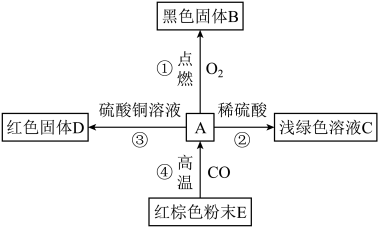
(1)B的名称是______ 。
(2)溶液C中溶质的化学式为______ 。
(3)③可证明铁的金属活动性比铜______ (填“强”或“弱”)。
(4)②的基本反应类型是______ 。
(5)④的化学方程式为______ 。
(一)人类冶炼和使用金属铝的时间较晚。可能是因为
a.地壳中铝元素含量少 b.冶炼铝的技术要求高
(二)银器在使用过程中,因为发生化学反应:
 ,产生的Ag2S使银器渐失去光泽。已知银的化合价为+1价,则Ag2S中S的化合价为
,产生的Ag2S使银器渐失去光泽。已知银的化合价为+1价,则Ag2S中S的化合价为(三)A是目前世界年产量最高的金属,根据下图回答下列问题:

(1)B的名称是
(2)溶液C中溶质的化学式为
(3)③可证明铁的金属活动性比铜
(4)②的基本反应类型是
(5)④的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】新能源汽车的研发和使用是时代发展的需要。
(1)下列能源不属于新能源的是___________(填序号)。
(2)锂(Li)的金属活泼性强于铝,它与稀硫酸反应的化学方程式为___________ ,新能源汽车除了节约化石能源外,其主要优点是___________ 。
(1)下列能源不属于新能源的是___________(填序号)。
| A.氢能 | B.核能 | C.石油 | D.风能 |
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】A—H是初中化学常见的物质,它们之间相互转化关系如图所示,其中A用于改良酸性土壤,B是人体胃液中帮助消化的物质。
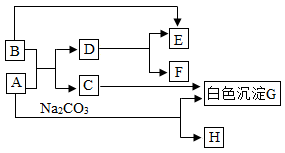
(1)C的化学式是_________________ 。
(2)写出B转化为E的一个化学方程式是_____________ ,反应类型是 ______ 。
(3)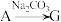 的化学方程式是
的化学方程式是 _______________________________ 。
(4)H溶液露置于空气中一会儿质量会________________ (填增重或减轻),用化学方程式解释为 ____________________ 。

(1)C的化学式是
(2)写出B转化为E的一个化学方程式是
(3)
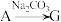 的化学方程式是
的化学方程式是 (4)H溶液露置于空气中一会儿质量会
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐1】回答下列与金属有关的问题
(1)在黄铜(铜锌合金)片和纯铜片中,硬度较大的是___________ ,将它们分别放入稀盐酸中能产生气泡的是___________ ;
(2)铁生锈是铁与空气中的___________ 发生化学反应的过程;
(3)向AgNO3和Cu(NO3)2的混合溶液中加入一定量Al粉,充分反应后过滤;取少量滤液滴加稀盐酸,产生白色沉淀.滤液中一定含有的溶质是___________ 。
(1)在黄铜(铜锌合金)片和纯铜片中,硬度较大的是
(2)铁生锈是铁与空气中的
(3)向AgNO3和Cu(NO3)2的混合溶液中加入一定量Al粉,充分反应后过滤;取少量滤液滴加稀盐酸,产生白色沉淀.滤液中一定含有的溶质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
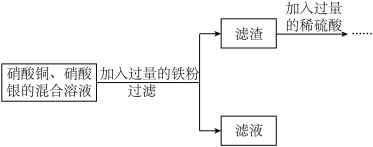
【推荐2】化学小组利用铁粉和含有硝酸铜、硝酸银的混合溶液验证铁、铜、银三种金属的活动性顺序,设计的部分实验流程如图所示。_____ 。(写一个)
(2)滤液中含有什么溶质?_____ 。
(3)向滤渣中加入过量的稀硫酸后,观察到什么现象?_____ 。
(2)滤液中含有什么溶质?
(3)向滤渣中加入过量的稀硫酸后,观察到什么现象?
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】金属资源在生产、生活中应用十分广泛,请回答下列问题。
(1)将黄铜片和纯铜片相互刻画,发现纯铜片表面留下较深的划痕。则它们的硬度大小关系是纯铜________ (选填“>”、“<”或“=”)黄铜。
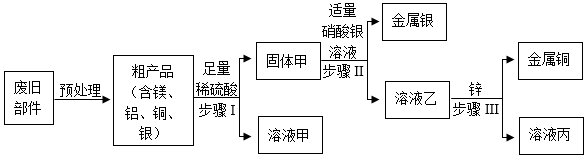
(2)废旧手机电路板中含有镁、铝、铜、银等金属,下图是将废旧手机电路板先进行预处理得到粗产品,再回收铜和银的流程。
①步骤Ⅱ中加入硝酸银溶液的作用是__________ 。
②步骤Ⅲ中发生反应的化学方程式为______ 。
(1)将黄铜片和纯铜片相互刻画,发现纯铜片表面留下较深的划痕。则它们的硬度大小关系是纯铜
(2)废旧手机电路板中含有镁、铝、铜、银等金属,下图是将废旧手机电路板先进行预处理得到粗产品,再回收铜和银的流程。

①步骤Ⅱ中加入硝酸银溶液的作用是
②步骤Ⅲ中发生反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】我国制碱工业先驱侯德榜发明了“侯氏制碱法”。其模拟流程如下:
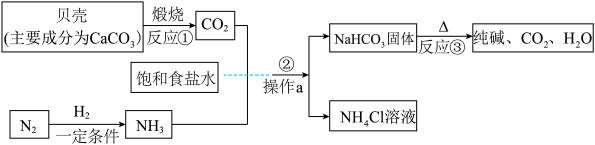
(1)工业上利用氮气和氧气的__________ 不同(填“沸点”或“熔点”),可将氮气从液态空气中分离出来。
(2)反应②的化学方程式为____________ 。
(3)操作a的名称是______ ,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、_____ 。
(4)写出NH4Cl的一种用途__________ 。

(1)工业上利用氮气和氧气的
(2)反应②的化学方程式为
(3)操作a的名称是
(4)写出NH4Cl的一种用途
您最近一年使用:0次
【推荐2】我国的茶文化历史悠久。

(1)泡茶时,茶壶中的滤网将茶水与茶叶分离。该分离方法与实验室中的_____ 操作相似。
(2)烧水的水壶使用一定时间后,内壁会出现一层水垢(主要成分为碳酸钙和氢氧化镁),可以用厨房中的_____ 浸泡后除去水垢。
(3)培植茶树需施用适量铵态氮肥。下列物质属于铵态氮肥的是_____ (填字母)。写出鉴定其为铵态氮肥的方法_____ 。
A.KNO3 B.CO(NH2)2 C.(NH4)2SO4
(4)如图为氮元素的部分价类二维图。A物质在空气中的体积分数约为_____ 。B、C、D物质的组成元素相同,但其化学性质不同的原因是_____ 。
(5)D点所示物质与水反应可生成E点所示物质,反应的化学方程式为_____ ,该反应属于_____ (填基本反应类型)。

(1)泡茶时,茶壶中的滤网将茶水与茶叶分离。该分离方法与实验室中的
(2)烧水的水壶使用一定时间后,内壁会出现一层水垢(主要成分为碳酸钙和氢氧化镁),可以用厨房中的
(3)培植茶树需施用适量铵态氮肥。下列物质属于铵态氮肥的是
A.KNO3 B.CO(NH2)2 C.(NH4)2SO4
(4)如图为氮元素的部分价类二维图。A物质在空气中的体积分数约为
(5)D点所示物质与水反应可生成E点所示物质,反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】硫酸锌可用于制造锌钡白、印染媒染剂等。用锌白矿(主要成分为ZnO,还含有FeO、CuO、SiO2等杂质)制备ZnSO4·7H2O的流程如下:
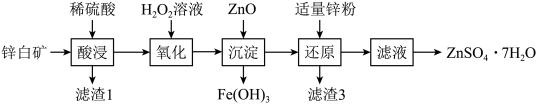
已知:相关金属离子生成氢氧化物沉淀的pH如下表:
(1)“滤渣1”的主要成分是______ (填化学式)。
(2)“酸浸”过程中,为了提高锌元素浸出速率,可采取的措施有:
①适当提高酸的浓度;
②______ (填一种)。
(3)“氧化”过程中 发生的反应方程式是______ 。
(4)“沉淀 ”过程中,加入ZnO调节溶液的pH控制在______ 之间。
(5)由滤液得到最终产品的操作依次为蒸发浓缩、______ 、过滤、洗涤、干燥。

已知:相关金属离子生成氢氧化物沉淀的pH如下表:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 6.4 | 8.0 |
(2)“酸浸”过程中,为了提高锌元素浸出速率,可采取的措施有:
①适当提高酸的浓度;
②
(3)“氧化”过程中 发生的反应方程式是
(4)“沉淀 ”过程中,加入ZnO调节溶液的pH控制在
(5)由滤液得到最终产品的操作依次为蒸发浓缩、
您最近一年使用:0次



