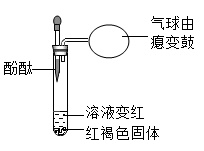
某女士因混合使用洁厕灵(含盐酸)和84消毒液(含次氯酸钠)清洁马桶,中毒死亡,其原因是2HCl+NaClO=NaCl+Cl2↑+X,产生的氯气有毒。
(1)上述反应中,氯元素化合价最高的物质是___________ (填字母)。
A 、HCl B、NaClO C、 NaCl D、 Cl2
(2)X的化学式为___________ 。
(3)《生活饮用水卫生标准》中,允许自来水厂使用氯气对天然水进行灭菌消毒,在此之前还要经过沉降、___________ 、吸附等净化操作。
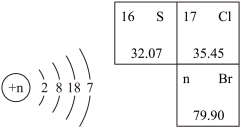
(4)已知溴元素(Br)的原子结构示意图如图,那么,溴原子核内质子数为___________ ;在化学反应中溴原子易___________ (填“得到”或“失去”)电子。___________ (填“周期”或“族”)。
(1)上述反应中,氯元素化合价最高的物质是
A 、HCl B、NaClO C、 NaCl D、 Cl2
(2)X的化学式为
(3)《生活饮用水卫生标准》中,允许自来水厂使用氯气对天然水进行灭菌消毒,在此之前还要经过沉降、
(4)已知溴元素(Br)的原子结构示意图如图,那么,溴原子核内质子数为
更新时间:2021/03/15 18:16:23
|
相似题推荐
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】“硝酸”是高中化学将要学习的物质,浓硝酸见光会发生化学变化,其化学方程式为:4HNO3═4NO2↑+2H2O+X↑
(1)X的化学式为__ 。
(2)请在硝酸的化学式中标出氮元素的化合价:__ 。
(1)X的化学式为
(2)请在硝酸的化学式中标出氮元素的化合价:
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】自来水厂净水时常使用明矾做絮凝剂。明矾是硫酸铝钾(一种盐)的结晶水合物,回答下列问题:
(1)请用化学符号表示与明矾结构中相关的下列微粒:
①两个硫原子______ 。
②十二个水分子______ 。
(2)明矾溶于水可以电离出钾离子,钾离子的符号为______ 。
(3)明矾溶于水后生成胶状氢氧化铝吸附悬浮杂质,氢氧化铝的化学式为______ 。
(4)Cl2常作自来水消毒剂,其实验室制法为:MnO2+4HCl(浓) X+Cl2↑+2H2O,X的化学式为
X+Cl2↑+2H2O,X的化学式为______ 。
(1)请用化学符号表示与明矾结构中相关的下列微粒:
①两个硫原子
②十二个水分子
(2)明矾溶于水可以电离出钾离子,钾离子的符号为
(3)明矾溶于水后生成胶状氢氧化铝吸附悬浮杂质,氢氧化铝的化学式为
(4)Cl2常作自来水消毒剂,其实验室制法为:MnO2+4HCl(浓)
 X+Cl2↑+2H2O,X的化学式为
X+Cl2↑+2H2O,X的化学式为
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
【推荐1】请用所学过的化学知识填空:
(1)人体中含量最多的物质_______ (填化学式);
(2)电解水(H2O)生成了氢气(H2)和氧气(O2),说明水是由______________ 组成的;
(3)实验室常用澄清石灰水检验二氧化碳,其原理是澄清石灰水中的氢氧化钙和二氧化碳反应生成不溶于水的白色固体碳酸钙。氢氧化钙的化学式是Ca(OH)2,其相对分子质量为_______ ;
(4)1个氟原子的质量为3.156×10-26Kg,一个碳(碳-12)原子的质量为1.993×10-26Kg,则氟的相对原子质量为______ (计算结果保留整数);
(5)若相对原子质量为M的原子,核外有N个电子,其核内中子数为是_______ 。
(1)人体中含量最多的物质
(2)电解水(H2O)生成了氢气(H2)和氧气(O2),说明水是由
(3)实验室常用澄清石灰水检验二氧化碳,其原理是澄清石灰水中的氢氧化钙和二氧化碳反应生成不溶于水的白色固体碳酸钙。氢氧化钙的化学式是Ca(OH)2,其相对分子质量为
(4)1个氟原子的质量为3.156×10-26Kg,一个碳(碳-12)原子的质量为1.993×10-26Kg,则氟的相对原子质量为
(5)若相对原子质量为M的原子,核外有N个电子,其核内中子数为是
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下图中A、B、C、D是四种粒子的结构示意图,E是银元素在元素周期表中的信息。请回答下列问题:
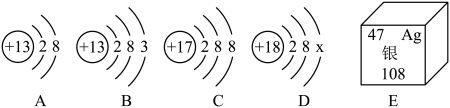
(1)图中A、B、C、D粒子共表示________ 种元素。
(2)D中x =_________ 。
(3)一个银原子的中子数为________ 个。
(4)已知铝元素的原子序数为13,氯元素的原子序数为17,请写出A、C形成的化合物的化学式__________

(1)图中A、B、C、D粒子共表示
(2)D中x =
(3)一个银原子的中子数为
(4)已知铝元素的原子序数为13,氯元素的原子序数为17,请写出A、C形成的化合物的化学式
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
【推荐3】(1)已知一个碳12原子的质量为m kg,另一个A原子的质量为n kg,且其中有a个质子。则A原子中的中子数是______ 。 用含m、n、a的代数式表示,下同
用含m、n、a的代数式表示,下同
(2)已知一个碳12原子的质量为 kg,R原子的相对原子质量是
kg,R原子的相对原子质量是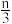 ,则一个R原子的质量是
,则一个R原子的质量是______ kg。
(3)现以一种氧原子质量的 为标准,其他原子的质量跟它相比所得的比值作为这种原子的相对原子质量。一个氧原子的质量为m kg,一个铁原子的质量是n kg,则铁原子的相对原子质量为
为标准,其他原子的质量跟它相比所得的比值作为这种原子的相对原子质量。一个氧原子的质量为m kg,一个铁原子的质量是n kg,则铁原子的相对原子质量为______ 。 用含m、n的代数式表示
用含m、n的代数式表示
 用含m、n、a的代数式表示,下同
用含m、n、a的代数式表示,下同
(2)已知一个碳12原子的质量为
 kg,R原子的相对原子质量是
kg,R原子的相对原子质量是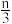 ,则一个R原子的质量是
,则一个R原子的质量是(3)现以一种氧原子质量的
 为标准,其他原子的质量跟它相比所得的比值作为这种原子的相对原子质量。一个氧原子的质量为m kg,一个铁原子的质量是n kg,则铁原子的相对原子质量为
为标准,其他原子的质量跟它相比所得的比值作为这种原子的相对原子质量。一个氧原子的质量为m kg,一个铁原子的质量是n kg,则铁原子的相对原子质量为 用含m、n的代数式表示
用含m、n的代数式表示
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】元素周期表是学习化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
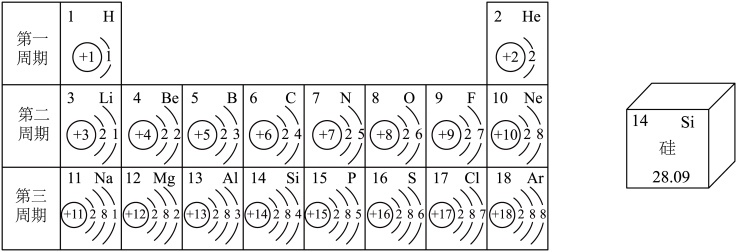
(1)写出对应化学符号:① 镁离子_____ ;② 三个五氧化二磷分子______ ;
(2)请从上面右图中写一条关于硅元素的信息:___________________________________ ;
(3)研究表明:第二周期从3~9号元素的原子电子层数相同,随着核电荷数逐渐增大,原子核对核外电子的引力逐渐增大,故原子半径逐渐减小。请分析第三周期从11~17号元素原子半径变化规律是______________ 。

(1)写出对应化学符号:① 镁离子
(2)请从上面右图中写一条关于硅元素的信息:
(3)研究表明:第二周期从3~9号元素的原子电子层数相同,随着核电荷数逐渐增大,原子核对核外电子的引力逐渐增大,故原子半径逐渐减小。请分析第三周期从11~17号元素原子半径变化规律是
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】下图是元素周期表中部分元素的信息,请回答下列问题:______ 。
(2)表中X=______ ,从分类上看它属于______ 元素。
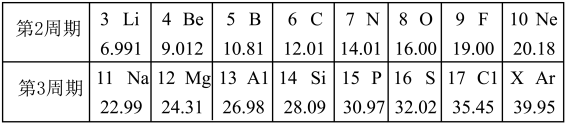
(2)表中X=
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
【推荐3】核电荷数为1﹣18的元素的原子结构示意图等信息如图,回答下列问题;

(1)俄国化学家______ 发现了元素周期律并编制出元素周期表。
(2)在第三周期中,各原子结构的共同之处是______________ ;该周期中,各原子核外电子排布的变化规律是__________________ 。
(3)在第三周期中,元素类型的变化情况是:从左到右由____ 元表过渡到____ 元素,并以稀对气体结尾。
(4)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子______ ,阴离子_________ 。

(1)俄国化学家
(2)在第三周期中,各原子结构的共同之处是
(3)在第三周期中,元素类型的变化情况是:从左到右由
(4)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
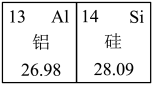
【推荐1】如图是元素周期表的部分信息,硅元素的质子数是_______ ,新型保温材料Al2SiO5中硅元素的化合价为______ ;铝原子失去电子形成离子的结构示意图为______ 。
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】用化学用语填空
(1)2个氢原子____________ ;
(2)3个硫离子____________ ;
(3)碘酒中的溶剂____________ ;
(4)标出 中磷元素的化合价
中磷元素的化合价____________ ;
(1)2个氢原子
(2)3个硫离子
(3)碘酒中的溶剂
(4)标出
 中磷元素的化合价
中磷元素的化合价
您最近一年使用:0次