解题方法
1 . 元素周期表使化学的学习变得有规律可循。元素甲、乙、丙在元素周期表中的位置如图1所示,图2为元素乙在周期表中的信息。下列说法正确的是
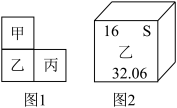
| A.甲表示碳元素 | B.元素甲与乙属于同一周期 |
| C.元素乙与丙属于同一族 | D.硫的相对原子质量为32.06 |
您最近半年使用:0次
名校
解题方法
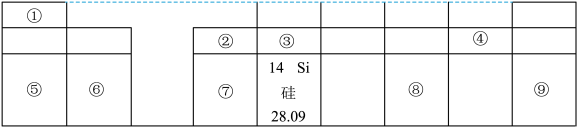
2 . 下图为元素周期表的部分结构。请按要求回答下列问题:____ 。
(2)⑤和⑥处在同一周期,原因是它们的原子的________ 相同。
(3)画出③的原子结构示意图:________ 。
(4)⑦的原子最外层电子数为3,易失电子,形成离子,其形成离子的符号为____ 。
(5)⑤和⑧形成物质的化学式为____ 。
(2)⑤和⑥处在同一周期,原因是它们的原子的
(3)画出③的原子结构示意图:
(4)⑦的原子最外层电子数为3,易失电子,形成离子,其形成离子的符号为
(5)⑤和⑧形成物质的化学式为
您最近半年使用:0次
解题方法
3 . 元素周期表是学习化学的重要工具,下表为元素周期表中部分元素的相关信息,利用下表回答相关问题。___________ (填“质子数”或“电子层数”或“最外层电子数”)相同;
(2)He和Mg的化学性质___________ (填“相似”或“不相似”);
(3)钠离子核外电子排布与___________ (填元素名称)原子核外电子排布相同;
(4)一个 含有
含有___________ 个电子;
(5)一般地说,电子层数相同的原子,原子的半径随原子序数的递增而减小(稀有气体除外);最外层电子数相同的原子,原子的半径随电子层数的增加而增大。请比较:氮原子半径___________ (填“>”或“<”)磷原子半径。

(2)He和Mg的化学性质
(3)钠离子核外电子排布与
(4)一个
 含有
含有(5)一般地说,电子层数相同的原子,原子的半径随原子序数的递增而减小(稀有气体除外);最外层电子数相同的原子,原子的半径随电子层数的增加而增大。请比较:氮原子半径
您最近半年使用:0次
解题方法
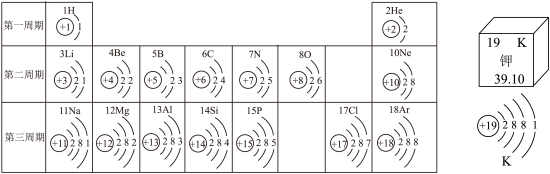
4 . 如图为元素周期表一部分和部分原子结构示意图等信息,请回答相关问题:_______ (画一个即可)。
(2)9号元素与12号元素组成化合物的化学式为_______ 。
(3)钾元素属于______ (填“金属元素”或“非金属元素”),其相对原子质量是_______ 。
(4)元素周期表中的每纵行元素属于同一族,同族元素的化学性质相似。结合原子结构示意图可知,这是由于原子的______ 相同。
(2)9号元素与12号元素组成化合物的化学式为
(3)钾元素属于
(4)元素周期表中的每纵行元素属于同一族,同族元素的化学性质相似。结合原子结构示意图可知,这是由于原子的
您最近半年使用:0次
5 . 下列说法正确的是
| A.由同一种元素组成的物质不一定是纯净物 |
| B.元素周期表中共有7个周期,18个族 |
| C.原子论和分子学说的创立奠定了现代化学的基础 |
| D.碳的单质都是由原子构成的 |
您最近半年使用:0次
6 . 锗(Ge)与镓(Ga)——高科技时代的隐形巨人,这两种材料的独特性质使它们成为许多关键技术的基础,包括通信、太空探索和夜视技术。中国在这两种材料的供应方面拥有明显的优势,这为我国在高科技领域的发展提供了坚实的基础。图1分别是锗元素在元素周期表中的信息和镓原子的原子结构示意图,图2是几种粒子的结构示意图,请回答下列问题:______ ,镓元素位于元素周期表中第______ 周期,氢氧化镓具有碱的化学性质,请写出氢氧化镓与盐酸反应的化学方程式:__________________ 。
(2)图2具有相对稳定结构的原子是______ (填字母序号);D、F 两元素组成的化合物的化学式为______ 。
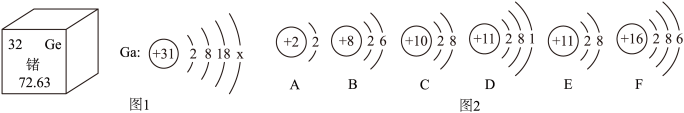
(2)图2具有相对稳定结构的原子是
您最近半年使用:0次
解题方法
7 . 下图是元素周期表中钙元素的信息和钙离子的结构示意图,下列分析错误的是
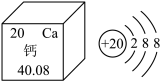
| A.钙原子的核电荷数是20 |
| B.钙的相对原子质量是40.08 |
| C.钙原子容易失去电子形成阳离子 |
| D.钙元素位于元素周期表的第三周期 |
您最近半年使用:0次
解题方法
8 . 氮化镓是制造芯片的材料之一,图1是镓元素(元素符号为:Ga)的原子结构示意图,图2是元素周期表的一部分。下列说法不正确的是
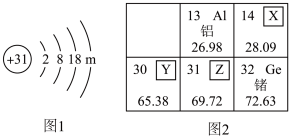
| A.图1中,m=3 | B.氢氧化镓的化学式为Ga(OH)2 |
| C.Ga与A1的化学性质相似 | D.Y、Z、Ge三原子的电子层数相同 |
您最近半年使用:0次
解题方法
9 . 门捷列夫在编制第一张元素周期表时,就预言了“类铝”元素(即后来发现的镓)的存在。铝和镓在周期表中位置如图所示,下列有关说法不正确的是

| A.铝原子的核外电子数是13 |
| B.镓的相对原子质量是69.723 |
| C.铝和镓原子的最外层电子数相同 |
| D.铝和镓在化学反应中都容易得到电子 |
您最近半年使用:0次
10 . 第二十四届冬季奥林匹克运动会处处体现“低碳环保”理念,科技感十足。
(1)能源:冬奥场馆大多采用绿色能源供电。下列不属于新能源的是______(填序号)。
(2)火炬“飞扬”:“飞扬”采用氢气作燃料比传统所用丙烷(化学式 )作燃料的优点是:
)作燃料的优点是:______ 。
(3)制冰技术:利用液态 蒸发吸热实现制冷,使水变成冰,此过程中
蒸发吸热实现制冷,使水变成冰,此过程中 的化学性质并没有改变,原因是
的化学性质并没有改变,原因是______ (从微观角度解释)。
(4)运动服:中国运动员御寒服采用新疆长绒棉面料,石墨烯发热材料里布。石墨烯发热材料在通电时产生热能,是利用了石墨烯良好的______ 性。
(5)场馆:“冰丝带”是由3360块发电玻璃拼成。发电玻璃是在普通玻璃上覆盖一层碲化镉(化学式CdTe)。碲化镉在弱光照射下也能持续发电,为冬奥场馆提供电力支持,根据如图信息填空。______ ;下列科学家对测定相对原子质量作出卓越贡献的是______ 。(填选项)
A.拉瓦锡 B.道尔顿 C.门捷列夫 D.张青莲
②镉元素位于第______ 周期。
(1)能源:冬奥场馆大多采用绿色能源供电。下列不属于新能源的是______(填序号)。
| A.太阳能 | B.核能 | C.地热能 | D.化石燃料 |
(2)火炬“飞扬”:“飞扬”采用氢气作燃料比传统所用丙烷(化学式
 )作燃料的优点是:
)作燃料的优点是:(3)制冰技术:利用液态
 蒸发吸热实现制冷,使水变成冰,此过程中
蒸发吸热实现制冷,使水变成冰,此过程中 的化学性质并没有改变,原因是
的化学性质并没有改变,原因是(4)运动服:中国运动员御寒服采用新疆长绒棉面料,石墨烯发热材料里布。石墨烯发热材料在通电时产生热能,是利用了石墨烯良好的
(5)场馆:“冰丝带”是由3360块发电玻璃拼成。发电玻璃是在普通玻璃上覆盖一层碲化镉(化学式CdTe)。碲化镉在弱光照射下也能持续发电,为冬奥场馆提供电力支持,根据如图信息填空。
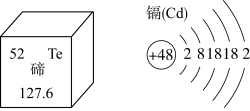
A.拉瓦锡 B.道尔顿 C.门捷列夫 D.张青莲
②镉元素位于第
您最近半年使用:0次



