名校
解题方法
1 . 我国茶文化源远流长。唐代陆羽所著的《茶经》被誉为茶界“百科全书”。
(1)煎茶:“清汤绿叶,味鲜醇,香扑鼻”。“香扑鼻”,从分子角度解释其原因是_______ 。
(2)煮茶:“其山水拣乳泉、石池漫流者上”,原因是流动的山泉水中钙、镁化合物含量少,硬度小,煮茶最好。在生活中可以通过_______ 降低水的硬度。
(3)泡茶:古代锡器(Sn)常用来泡茶,锡器表面的+4价氧化物可与稀盐酸发生复分解反应,写出化学反应方程式_______ 。
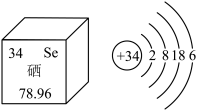
(4)饮茶:茶叶中的硒有防癌作用,硒在元素周期表中的部分信息和其原子结构示意图如图所示,该元素处于元素周期表中第______ 周期。
(1)煎茶:“清汤绿叶,味鲜醇,香扑鼻”。“香扑鼻”,从分子角度解释其原因是
(2)煮茶:“其山水拣乳泉、石池漫流者上”,原因是流动的山泉水中钙、镁化合物含量少,硬度小,煮茶最好。在生活中可以通过
(3)泡茶:古代锡器(Sn)常用来泡茶,锡器表面的+4价氧化物可与稀盐酸发生复分解反应,写出化学反应方程式

(4)饮茶:茶叶中的硒有防癌作用,硒在元素周期表中的部分信息和其原子结构示意图如图所示,该元素处于元素周期表中第
您最近半年使用:0次
解题方法
2 . 下列有关课本图表、数据使用的叙述中,不正确 的是
| A.根据元素周期表,可以直接查找某元素原子的中子数 |
| B.根据溶液的pH数值,可判断物质的酸碱性强弱 |
| C.根据常见酸碱盐溶解性表,可以帮助判断某些复分解反应能否发生 |
| D.根据物质的溶解度曲线图,可以确定该物质在不同温度时的溶解度 |
您最近半年使用:0次
名校
解题方法
3 . 科学家对人类文明和社会可持续发展作出了重要贡献,下列选项正确的是
| A.波义耳发现了酸碱指示剂 | B.门捷列夫提出了近代原子学说 |
| C.道尔顿确定了空气的组成 | D.拉瓦锡编制了元素周期表 |
您最近半年使用:0次
解题方法
4 . 元素周期表是学习化学的重要工具。
2019年是“国际化学元素周期表年”,门捷列夫制出第一张元素周期表,原子序数为1~18的元素的原子结构示意图等信息如图,请认真分析并回答下列问题。
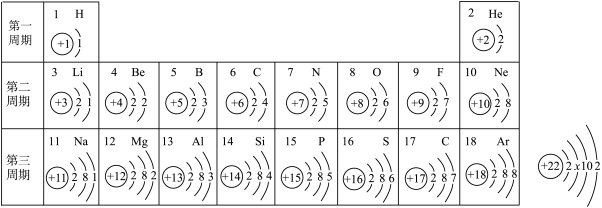
(1)通过分析图,发现表中9号和17号元素______ 相同,钛原子结构示意图如图所示,则x=_______ ;钛元素质子数为________ 。
(2)钠原子的次外层电子数为_______ 。
(3)写出9号和12号元素形成的纯净物的化学符号_______ 。
(4)如图所示,若x=17,则该粒子为_______ (填化学符号);若x=20,则该粒子为_______ (填化学符号)。

2019年是“国际化学元素周期表年”,门捷列夫制出第一张元素周期表,原子序数为1~18的元素的原子结构示意图等信息如图,请认真分析并回答下列问题。

(1)通过分析图,发现表中9号和17号元素
(2)钠原子的次外层电子数为
(3)写出9号和12号元素形成的纯净物的化学符号
(4)如图所示,若x=17,则该粒子为

您最近半年使用:0次
解题方法
5 . 如图为元素周期表的一部分,请按要求填空:

(1)表中元素①形成单质的化学式为______ ;
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的______ 相同;
(3)表中11号和9号元素组成的化合物的化学式为______ ;
(4)表中不同种元素最本质的区别是______ 。

(1)表中元素①形成单质的化学式为
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的
(3)表中11号和9号元素组成的化合物的化学式为
(4)表中不同种元素最本质的区别是
您最近半年使用:0次
解题方法
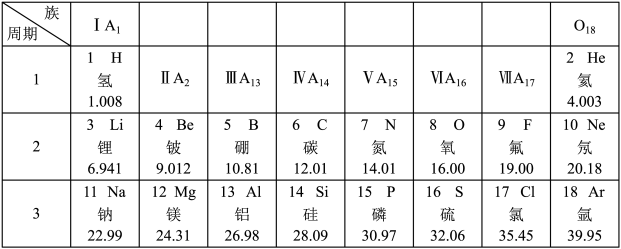
6 . 元素周期表是学习和研究化学的重要工具。下图是元素周期表部分内容,请分析表中信息回答相关问题。___________ ,它属于___________ (填“金属”或“非金属”)元素,在化学反应中容易___________ (填“得到”或“失去”)电子。
(2)不同种元素最本质的区别是___________ ;
(3)在同一族中,各元素的原子最外层电子数___________ (He除外),原子序数为3的元素与第三周期中的___________ (填名称)元素具有相似的化学性质。
(2)不同种元素最本质的区别是
(3)在同一族中,各元素的原子最外层电子数
您最近半年使用:0次
解题方法
7 . 元素周期表是学习和研究化学的重要工具。请分析下图中的信息并回答下列问题。

(1)9 号元素的元素名称为_______ ,易_______ (填“得到”或“失去”)电子。
(2)不同种元素最本质的区别是_______ 不同。
(3)在元素周期表中,同一族(行)的元素具有相似的化学性质,则下列各组元素具有相似化学性质的是______(填字母)。
(4)在元素周期表中,同一周期(横行)中的元素,除 0 族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。则钠和镁的原子半径以及失电子能力关系是:镁原子半径比钠的小,在化学反应中镁原子失电子能力比钠_______ 。(填“强”或“弱”)

(1)9 号元素的元素名称为
(2)不同种元素最本质的区别是
(3)在元素周期表中,同一族(行)的元素具有相似的化学性质,则下列各组元素具有相似化学性质的是______(填字母)。
| A.Ar 和 Ne | B.F 和 Cl | C.Be 和 Mg | D.H 和 Na |
(4)在元素周期表中,同一周期(横行)中的元素,除 0 族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。则钠和镁的原子半径以及失电子能力关系是:镁原子半径比钠的小,在化学反应中镁原子失电子能力比钠
您最近半年使用:0次
2024九年级下·全国·专题练习
解题方法
8 . 如图是元素周期表中第2、3周期的元素,请回答有关问题。
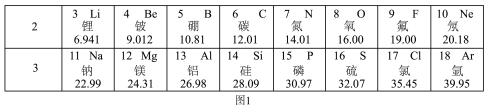
(1)下列各组具有相似化学性质的元素是______(填字母序号);
(2)写出一条第三周期元素原子的核外电子排布规律______ ;
(3)第7号元素与第12号元素的原子形成化合物的化学式为______ ;15号元素的相对原子质量为______ ;
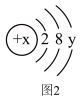
(4)某离子的结构示意图如图2所示,当x﹣y=8时,该粒子的符号为______ ;
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是______(填字母序号)。


(1)下列各组具有相似化学性质的元素是______(填字母序号);
| A.Na、Cl | B.O、S | C.F、Cl | D.Cl、Ar |
(2)写出一条第三周期元素原子的核外电子排布规律
(3)第7号元素与第12号元素的原子形成化合物的化学式为
(4)某离子的结构示意图如图2所示,当x﹣y=8时,该粒子的符号为
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是______(填字母序号)。
| A.NO和O2 | B.CO和N2 |
| C.SO2和CO2 | D. 和 和 |
您最近半年使用:0次
解题方法
9 . 元素周期表是学习化学的重要工具,如图为元素周期表中部分元素的相关信息,利用如图回答相关问题。

(1)原子序数为4的元素符号为_________ 。
(2)C、N、O排在同周期是因为_______ (选填“质子数”“电子层数”或“最外层电数”)相同。
(3)He和Mg的化学性质_______ (选填“相似”或“不相似”)。

(1)原子序数为4的元素符号为
(2)C、N、O排在同周期是因为
(3)He和Mg的化学性质
您最近半年使用:0次
名校
解题方法
10 . 目前,元素周期表的第七周期已被填满。2017年,科学家发现的第113号、115号、117号和118号元素有了中文名称。已知第113号元素与Al元素同主族,根据元素周期律知识,下列预测或说法中合理的是


| A.Nh的最高价氧化物对应的水化物可能具有两性 |
| B.Mc在元素周期表中的位置是第七周期第ⅤB族 |
| C.Ts的同位素原子具有相同的电子数 |
| D.Og在元素周期表的所有元素中非金属性最强 |
您最近半年使用:0次



